
Liên kết trong mạng tinh thể kim loại là loại liên kết nào sau đây?
Đáp án đúng là: D
Trong tinh thể kim loại, liên kết kim loại được hình thành do lực hút tĩnh điện giữa các electron hóa trị tự do với các ion dương kim loại ở các nút mạng.
Đáp án cần chọn là: D
Kim loại nào sau đây là kim loại kiềm?
Đáp án đúng là: D
Lí thuyết về kim loại kiềm.
Đáp án cần chọn là: D
Phát biểu nào sau đây về đặc điểm của nguyên tử kim loại là đúng?
Trong cùng một chu kì, so với các nguyên tử nguyên tố phi kim thì
Đáp án đúng là: D
Dựa vào đặc điểm nguyên tử kim loại.
Đáp án cần chọn là: D
Trong các kim loại sau đây, kim loại dẫn điện tốt nhất là
Đáp án đúng là: D
Lí thuyết về tính chất vật lí của kim loại.
Đáp án cần chọn là: D
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hoá - khử như sau:

Pin Galvani có sức điện động chuẩn lớn nhất là
Đáp án đúng là: C
Epin = Eanode – Ecathode
Đáp án cần chọn là: C
Một học sinh muốn thực hiện thí nghiệm mạ đồng lên trên bề mặt vật liệu bằng sắt. Cách thực hiện nào sau đây đúng?
Đáp án đúng là: A
Ứng dụng của điện phân.
- Kim loại mạ gắn với anode
- Vật cần mạ gắn với cathode
- Dung dịch mạ là dung dịch muối của kim loại mạ.
Đáp án cần chọn là: A
Một học sinh thực hiện 3 thí nghiệm ở điều kiện chuẩn và quan sát được các hiện tượng sau:
(1) Đồng (Copper) kim loại không phản ứng với dung dịch Pb(NO3)2 1 M.
(2) Chì (Lead) kim loại tan trong dung dịch AgNO3 1M và xuất hiện tinh thể Ag.
(3) Bạc (Silver) kim loại không phản ứng với dung dịch Cu(NO3)2 1 M.
Trật tự nào sau đây thể hiện đúng mức độ tính khử của ba kim loại?
Đáp án đúng là: B
Lí thuyết về phản ứng kim loại và dung dịch muối: Kim loại có tính khử mạnh hơn đẩy được kim loại có tính khử yếu hơn ra khỏi dung dịch muối.
Đáp án cần chọn là: B
Cho khối lượng riêng của các chất:
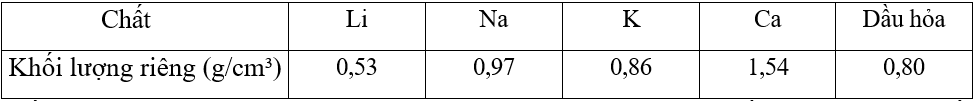
Để bảo quản một số kim loại mạnh, người ta ngâm chìm các kim loại đó vào trong dầu hỏa. Hãy cho biết kim loại nào không bảo quản được bằng cách cho vào dầu hỏa?
Đáp án đúng là: D
Tính chất vật lí của kim loại kiềm.
Chất/hợp chất nào có khối lượng riêng nhỏ hơn sẽ nổi lên trên chất có khối lượng riêng lớn.
Đáp án cần chọn là: D
Hình bên dưới mô tả quá trình mạ điện bằng phương pháp điện phân (với anode bằng kim loại cần mạ).
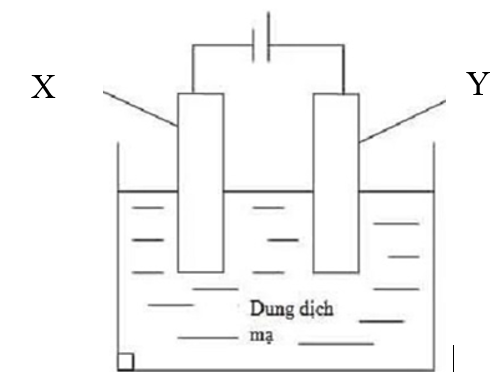
Chọn phát biểu không đúng
Đáp án đúng là: D
Quá trình xảy ra trong quá trình điện phân:
+ Ở cathode: xảy ra quá trình khử.
+ Ở anode: xảy ra quá trình oxi hóa.
Đáp án cần chọn là: D
Hình ảnh sau đây minh họa tính chất vật lí nào của kim loại?
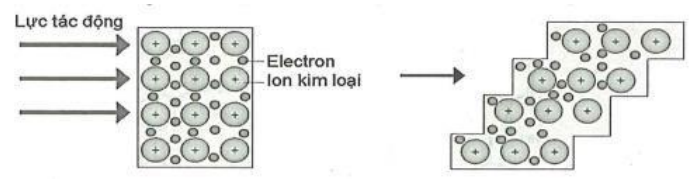
Đáp án đúng là: B
Lí thuyết về tính chất vật lí của kim loại.
Đáp án cần chọn là: B
Thế điện cực chuẩn của điện cực nào sau đây được quy ước bằng 0 và được gọi là điện cực so sánh?
Đáp án đúng là: D
Dựa vào lí thuyết thế điện cực.
Đáp án cần chọn là: D
Nhúng thanh kẽm vào dung dịch chất nào sau đây sẽ xảy ra ăn mòn điện hoá?
Đáp án đúng là: A
Lí thuyết về ăn mòn điện hóa.
Đáp án cần chọn là: A
Ở nhiệt độ thường, kim loại nào sau đây tan hết trong nước dư?
Đáp án đúng là: B
Dựa vào tính chất hoá học của kim loại.
Đáp án cần chọn là: B
Kim loại mà khi tác dụng với HCl hoặc Cl2 không cho ra cùng một muối là
Đáp án đúng là: C
Lí thuyết về tính chất hóa học của kim loại.
Đáp án cần chọn là: C
Chalcopyrite là quặng đồng phổ biến nhất có màu vàng ánh kim. Một mẫu quặng chalcopyrite có chứa 35% CuFeS2 về khối lượng. Hàm lượng đồng có trong quặng đó là
Đáp án đúng là: A
Gọi khối lượng của quặng là x.
⟹ Khối lượng của CuFeS2
⟹ Hàm lượng đồng có trong quặng
Đáp án cần chọn là: A
Cho sơ đồ thùng điện phân của aluminium oxide (Al2O3) nóng chảy:
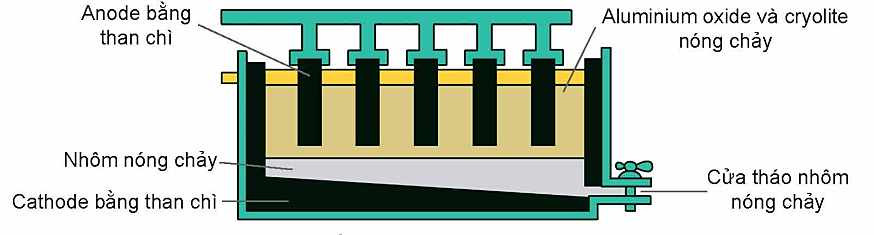
Cho các phát biểu sau:
a) Cửa tháo nhôm được bố trí ở đáy bình điện phân
b) Tại cathode xảy ra quá trình khử O2-, tại anode xảy ra quá trình oxi hóa ion Al3+.
c) Sau 1 thời gian sử dụng, phải thay thế điện cực dương.
d) Hỗn hợp aluminium oxide (Al2O3) và cryolite (Na3AlF6) nóng chảy ở nhiệt độ cao hơn aluminium oxide (Al2O3).
Các phát biểu sai là
Đáp án đúng là: B
Lí thuyết về điện phân nóng chảy.
Đáp án cần chọn là: B
Các công trình bằng thép (hợp kim của Fe và C) dễ bị ăn mòn điện hóa khi tiếp xúc với nước biển. Một trong số các phương pháp bảo vệ các công trình bằng thép khỏi sự ăn mòn điện hóa là gắn các khối nhôm (aluminium, Al), kẽm (zinc, Zn) hoặc hợp kim của chúng vào phần chìm dưới nước biển của công trình đó.
Trả lời cho các câu 17, 18 dưới đây:
Cho các phát biểu sau về ăn mòn điện hóa và phương pháp bảo vệ đối với các công trình bằng thép nêu trên:
(a) Các khối nhôm hoặc kẽm bảo vệ thép theo phương pháp điện hóa.
(b) Khi thép bị ăn mòn điện hóa, sắt trong thép bị oxi hóa.
(c) Thép bị ăn mòn điện hóa mà không cần tiếp xúc với dung dịch chất điện li.
(d) Khi được bảo vệ bằng phương pháp điện hóa, sắt đóng vai trò là anode nên không bị ăn mòn.
Số phát biểu đúng là
Đáp án đúng là: C
Dựa vào lý thuyết ăn mòn điện hoá.
Đáp án cần chọn là: C
Cho biết thế điện cực chuẩn của Ca2+/Ca và Fe2+/Fe lần lượt là –2,870 V và –0,440 V. Khi thảo luận về phương pháp bảo vệ các công trình bằng thép nêu trên khỏi sự ăn mòn điện hoá, một học sinh đề xuất: “Có thể sử dụng kim loại calcium (Ca) thay thế cho các khối nhôm hoặc kẽm để bảo vệ các công trình thép đó”. Một số nhận định đồng tình và không đồng tình với đề xuất này được nêu ra như sau:
(1) Có thể sử dụng khối kim loại calcium do kim loại này có tính khử mạnh hơn sắt.
(2) Có thể sử dụng khối kim loại calcium do kim loại này và nhôm đều có khối lượng riêng nhỏ.
(3) Không thể sử dụng khối kim loại calcium do kim loại này dễ phản ứng với nước biển.
(4) Không thể sử dụng khối kim loại calcium do kim loại này có tính khử yếu hơn sắt.
Nhận định đúng là
Đáp án đúng là: A
Dựa vào tính chất của calcium.
Đáp án cần chọn là: A
Sự ăn mòn kim loại gây tổn hại to lớn cho nền kinh tế quốc dân, do đó cần phải chống ăn mòn kim loại.
| Đúng | Sai | |
|---|---|---|
| a) Nối kim loại cần bảo vệ với một kim loại hoạt động hoá học mạnh hơn là cách chống ăn mòn kim loại theo phương pháp điện hoá. | ||
| b) Tạo ra hợp kim bền với môi trường như inox. Thành phần quan trọng của inox là sắt (iron), chromium, carbon. | ||
| c) Việc đánh giá đúng mức độ ăn mòn giúp chọn phương pháp bảo vệ phù hợp. | ||
| d) Quấn một dây kẽm quanh đinh sắt là cách để chống ăn mòn kẽm trong môi trường có chất điện li. |
Đáp án đúng là: Đ; Đ; Đ; S
* Chống ăn mòn kim loại
- Phương pháp điện hóa
+ Nguyên tắc bảo vệ kim loại khỏi bị ăn mòn bằng phương pháp điện hóa là gắn kim loại cần bảo vệ một kim loại khác hoạt động hóa học mạnh hơn. Khi đó, kim loại hoạt động hóa học mạnh hơn bị ăn mòn.
- Phương pháp phủ bề mặt
+ Phủ kim loại cần bảo vệ bằng các kim loại khác không bị gỉ như Au, Sn, Zn.
+ Phủ kim loại cần bảo vệ bằng các hợp chất vô cơ hoặc hữu cơ như sơn, dầu, mỡ,…
Đáp án cần chọn là: Đ; Đ; Đ; S
Trong công nghiệp, kim loại sodium được sản xuất bằng cách điện phân nóng chảy muối sodium chloride.
| Đúng | Sai | |
|---|---|---|
| a) Phương trình hóa học của phản ứng điện phân sodium chloride là: 2NaCl $\overset{dpnc}{\rightarrow}$ 2Na + Cl2 | ||
| b) Trong quá trình điện phân nóng chảy muối sodium chloride, tại anode xảy ra sự oxi hóa anion Cl-, cathode xảy ra sự khử cation Na+. | ||
| c) Trong quá trình điện phân, kim loại sodium sinh ra tại anode. | ||
| d) Để sản xuất được 2,3 kg kim loại sodium với hiệu suất 90% thì khối lượng NaCl tinh khiết cần dùng là 6,5 kg. |
Đáp án đúng là: Đ; Đ; S; Đ
a), b), c) Lí thuyết về điện phân.
d) Tính theo phương trình hoá học.
Đáp án cần chọn là: Đ; Đ; S; Đ
Nhúng thanh kẽm và thanh đồng (không tiếp xúc với nhau) vào cốc đựng dung dịch H2SO4 loãng. Nối thanh kẽm và thanh đồng bằng dây dẫn (có một khóa X) như hình bên.
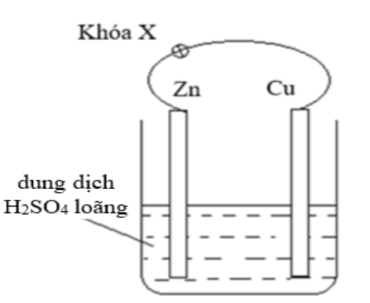
| Đúng | Sai | |
|---|---|---|
| a) Khi đóng khóa X, xảy ra ăn mòn điện hóa học và thanh Zn bị ăn mòn. | ||
| b) Tốc độ bọt khí thoát ra khi mở khóa X và khi đóng khóa X là như nhau. | ||
| c) Khi chưa đóng khóa X, xảy ra ăn mòn hóa học. | ||
| d) Khi thay thanh Cu bằng thanh Mg, thanh Zn vẫn bị ăn mòn điện hóa. |
Đáp án đúng là: Đ; S; Đ; S
Lí thuyết về ăn mòn hóa học và ăn mòn điện hóa học.
Đáp án cần chọn là: Đ; S; Đ; S
Tiến hành thí nghiệm về ăn mòn điện hoá như hình sau.
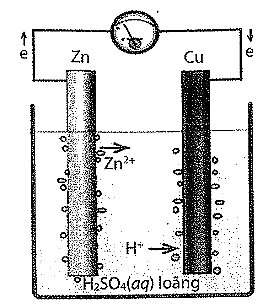
| Đúng | Sai | |
|---|---|---|
| a) Sau một thời gian tốc độ thoát khí sẽ giảm dần và màu xanh của dung dịch đậm dần. | ||
| b) Điện cực Zn là anode, điện cực Cu là cathode. | ||
| c) Khí H2 chỉ thoát ra trên bề mặt thanh Cu, trên thanh Zn không có khí thoát ra. | ||
| d) Nồng độ cation Zn2+ trong dung dịch tăng dần. |
Đáp án đúng là: S; Đ; S; Đ
Quá trình xảy ra trong pin điện hóa:
+ Anode (-): xảy ra quá trình oxi hóa.
+ Cathode (+): xảy ra quá trình khử.
Đáp án cần chọn là: S; Đ; S; Đ
Cho biết giá trị thế điện cực chuẩn của các cặp oxi hoá - khử sau:

Cho các kim loại Zn, Fe, Cu, Au. Ở điều kiện chuẩn, số kim loại (trong dãy trên) phản ứng được với dung dịch HCl 1,0 M là bao nhiêu?
Đáp án đúng là:
Dựa vào giá trị thế điện cực chuẩn của các cặp oxi hóa – khử.
Đáp án cần điền là: 2
Cho các tên sau: Đồng thau; tecmit; inox; duralumin (dural); thép 304; gang; đồng thanh. Có bao nhiêu tên là hợp kim?
Đáp án đúng là:
Lý thuyết về khái niệm hợp kim.
Đáp án cần điền là: 6
Tiến hành các thí nghiệm sau:
(1) Đốt dây nhôm trong bình khí oxygen.
(2) Cho đinh thép sạch vào dung dịch H2SO4 loãng.
(3) Cho lá Al nguyên chất vào dung dịch CuSO4.
(4) Để thanh thép trong không khí ẩm lâu ngày.
Có bao nhiêu thí nghiệm có xảy ra ăn mòn điện hóa học?
Đáp án đúng là:
Điều kiện xảy ra ăn mòn điện hóa học:
+ Có hai điện cực khác nhau về bản chất.
+ Hai điện cực tiếp xúc với nhau
+ Cùng tiếp xúc với dung dịch điện li (hoặc môi trường không khí ẩm).
Đáp án cần điền là: 3
Hợp kim duralumin có thể bị phá hủy trong dung dịch kiềm do xảy ra phản ứng:
2Al + 2NaOH + 2H2O ⟶ 2NaAlO2 + 3H2
Để xác định hàm lượng Al trong duralumin, người ta ngâm 10 gam mẫu hợp kim trong dung dịch kiềm dư, sau khi phản ứng xảy ra hoàn toàn, lọc lấy chất rắn, làm khô, cần lại thấy còn 0,8 gam chất rắn không tan. Trong hợp kim trên, Al chiếm bao nhiêu phần trăm về khối lượng?
Đáp án đúng là:
Ngâm hợp kim trong dung dịch kiềm ⟶ Chỉ có Al tham gia phản ứng
⟹ Khối lượng hợp kim giảm = Khối lượng Al có trong hợp kim
Đáp án cần điền là: 92
Cho thế điện cực chuẩn của Al3+/Al và Fe2+/Fe lần lượt bằng -1,676 V và -0,440 V. Sức điện động chuẩn của pin Al-Fe bằng bao nhiêu? (Làm tròn kết quả đến hàng phần trăm)
Đáp án đúng là:
$E_{pin} = E_{cathode}^{0} - E_{{}_{anode}}^{0}$
Đáp án cần điền là: 1,24
Luyện thép từ gang là quá trình làm giảm hàm lượng carbon và một số nguyên tố khác có trong gang. Một nhà máy luyện thép sử dụng loại gang nguyên liệu trong đó carbon chiếm 4,20% về khối lượng, còn lại là sắt (coi hàm lượng các nguyên tố khác không đáng kể). Khi tiến hành luyện thép, một lượng 1,44 tấn khí oxygen được thổi vào 22,5 tấn gang nguyên liệu nóng chảy để oxi hóa carbon thành CO và CO2. Hỗn hợp khí thu được chỉ chứa CO và CO2 với số mol bằng nhau. Phần trăm khối lượng carbon trong thép là w%, còn lại là săt. Coi sắt không bị mất đi trong quá trình luyện thép. Giá trị của w là bao nhiêu? (kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến hàng phần trăm).
Đáp án đúng là:
22,5 tấn gang $\left\{ \begin{array}{l} {C:0,945} \\ {Fe:21,555} \end{array} \right.\overset{+ O_{2}}{\rightarrow}\left\{ \begin{array}{l} {CO} \\ {CO_{2}} \end{array} \right.$+ C (w%) + Fe
BTNT(O)
BTNT (C)
Đáp án cần điền là: 1,03


