
Cho dãy các kim loại: Na, Cu, Al, Cr. Kim loại mềm nhất trong dãy là
Đáp án đúng là: C
Tính chất vật lí của kim loại kiềm.
Đáp án cần chọn là: C
Tính dẻo, tính dẫn điện, tính dẫn nhiệt và ánh kim của kim loại đều do thành phần nào sau đây gây ra?
Đáp án đúng là: B
Dựa vào mô hình liên kết kim loại.
Đáp án cần chọn là: B
Để mạ vàng, tiến hành điện phân dung dịch chứa muối K[Au(CN)2]. Tại cathode xảy ra quá trình nào?
Đáp án đúng là: B
Quá trình điện phân:
+) Cathode: xảy ra quá trình khử
+) Anode: xảy ra quá trình oxi hoá
Đáp án cần chọn là: B
Thép là vật liệu kim loại có thành phần chính là
Đáp án đúng là: B
Lí thuyết về hợp kim.
Đáp án cần chọn là: B
Kim loại nào sau đây có nhiệt độ nóng chảy cao nhất?
Đáp án đúng là: D
Lí thuyết về tính chất vật lí của kim loại.
Đáp án cần chọn là: D
Phản ứng nào sau đây không điều chế được kim loại Cu?
Đáp án đúng là: B
Dựa vào lí thuyết điều chế kim loại.
Đáp án cần chọn là: B
Nhôm được sản xuất bằng phương pháp điện phân nóng chảy aluminium oxide (Al2O3). Phương trình hoá học của phản ứng điện phân là
Đáp án đúng là: A
Phương pháp điện phân nóng chảy.
Đáp án cần chọn là: A
Nguyên tố kim loại nào sau đây tạo nên thành phần chính của đá vôi?
Đáp án đúng là: C
Lí thuyết về trạng thái tự nhiên của nguyên tố nhóm IIA.
Đáp án cần chọn là: C
Ở điều kiện thường, dãy các đơn chất kim loại có khối lượng riêng tăng dần từ trái sang phải là
Đáp án đúng là: B
Dựa vào tính chất vật lí của kim loại chuyển tiếp.
Đáp án cần chọn là: B
Cho các cặp oxi hoá − khử của các kim loại và thế điện cực chuẩn tương ứng:
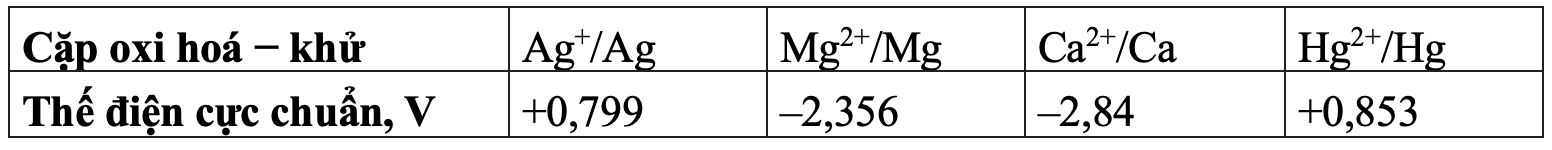
Trong số các kim loại trên, kim loại có tính khử mạnh nhất là
Đáp án đúng là: C
Dựa vào ý nghĩa của thế điện cực chuẩn.
Đáp án cần chọn là: C
Trong công nghiệp, dãy kim loại nào sau đây chỉ được sản xuất chủ yếu bằng phương pháp điện phân nóng chảy?
Đáp án đúng là: B
Nguyên tắc điều chế kim loại: Khử các ion kim loại trong hợp chất thành kim loại.
+) Phương pháp thuỷ luyên: điều chế kim loại hoạt động trung bình và yếu
+) Phương pháp nhiệt luyện: điều chế kim loại hoạt động trung bình và yếu
+) Phương pháp điện phân nóng chảy: điều chế kim loại hoạt động mạnh
Đáp án cần chọn là: B
Ion kim loại nào sau đây bị điện phân trong dung dịch (với điện cực graphite)?
Đáp án đúng là: B
Điện phân dung dịch:
Cathode:
Khử cation (sau Al): Mn+ + ne ⟶ M
Có mặt cation K+, Na+, Ca2+, Ba2+, Mg2+, Al3+ thì nước bị điện phân: 2H2O + 2e ⟶ H2 + 2OH-
Anode:
Oxi hóa anion: Xn- ⟶ X + ne
Các gốc acid chứa oxygen không tham gia điện phân dung dịch, nước bị điện phân: 2H2O ⟶ O2 + 4H+ + 4e
Đáp án cần chọn là: B
Trong công nghiệp, điện phân dung dịch NaCl bão hòa không có màng ngăn để điều chế nước Javel. Chọn phát biểu đúng.
Đáp án đúng là: C
Quá trình xảy ra trong điện phân:
+ Cathode (cực âm): xảy ra quá trình khử.
+ Anode (cực dương): xảy ra quá trình oxi hóa.
Khi không có màng ngăn, chất tạo ra từ cathode và anode sẽ tiếp xúc với nhau.
Đáp án cần chọn là: C
Cho các phát biểu về tách kim loại:
(1) Đồng có thể được tách từ copper(II) oxide bằng cách nung nóng.
(2) Điện phân nóng chảy aluminium oxide, thu được nhôm nóng chảy ở cực âm của bình điện phân.
(3) Kẽm có thể được tách từ zinc oxide bằng cách nung nóng zinc oxide với carbon.
Các phát biểu đúng là
Đáp án đúng là: C
Phương pháp điều chế kim loại:
+) Điện phân nóng chảy: điều chế kim loại hoạt động mạnh
+) Nhiệt luyện, thuỷ luyện: điều chế kim loại hoạt động trung bình, yếu.
Đáp án cần chọn là: C
Cho biết: $E_{Na^{+}/Na} = - 2,713V$, $E_{Mg^{2 +}/Mg} = - 2,356V$, $E_{Cu^{2 +}/Cu} = 0,340V$,$E_{2H_{2}O/OH^{-} + H_{2}} = - 0,413V$ Cho các nhận định sau:
(a) $E_{Mg^{2 +}/Mg} < E_{2H_{2}O/OH^{-} + H_{2}} = - 0,413V$, nên kim loại Mg có thể tác dụng được với H2O tạo base và H2
(b) Khi cho dung dịch CuSO4 vào dung dịch NaOH xuất hiện kết tủa Cu màu đỏ.
(c) Cho băng magnesium vào ống nghiệm chứa dung dịch copper(II) sulfate (màu xanh), thấy màu xanh của dung dịch nhạt dần.
(d) Khi cho mẩu Na vào dung dịch chứa đồng thời MgSO4 1M và CuSO4 1M thì Cu2+ phản ứng với kim loại Na trước.
Số nhận định đúng là:
Đáp án đúng là: A
Dựa vào lý thuyết về thế điện cực chuẩn.
Đáp án cần chọn là: A
Điện phân nóng chảy hoàn toàn 2,98 gam MCln, thu được 0,02 mol Cl2. Kim loại M là
Đáp án đúng là: D
Tính theo PTHH: 2MCln → 2M + nCl2
Đáp án cần chọn là: D
Sắp xếp nào dưới đây đúng theo thứ tự giảm dần tính khử của X, Y, Z, W? Biết khi thực hiện phản ứng kim loại tác dụng với muối, thu được kết quả như sau:
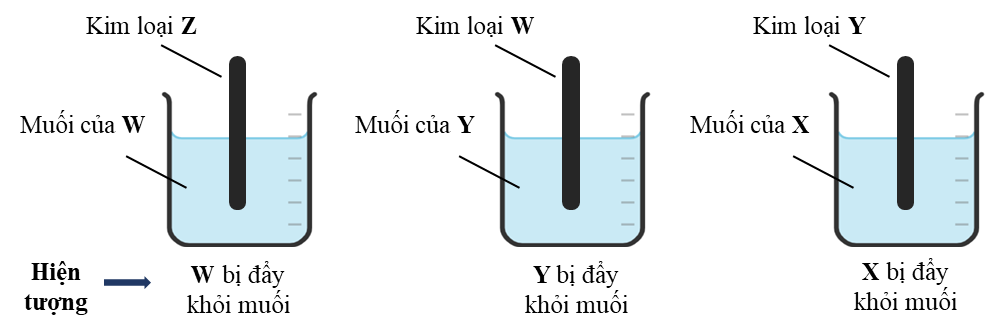
Đáp án đúng là: C
Tính chất hóa học của kim loại: Kim loại có tính khử mạnh hơn đẩy được kim loại yếu hơn ra khỏi muối của nó.
Đáp án cần chọn là: C
Cho các phát biểu sau:
(a) Điện phân dung dịch NaCl (với điện cực trơ), thu được khí H2 ở cathode
(b) Cho CO dư qua hỗn hợp Al2O3 và CuO đun nóng thu được Al và Cu.
(c) Nhúng thanh Zn vào dung dịch chứa CuSO4 và H2SO4, có xuất hiện ăn mòn điện hóa.
(d) Kim loại có nhiệt độ nóng chảy thấp nhất là Hg, kim loại dẫn điện tốt nhất là Ag.
(e) Cho dung dịch AgNO3 dư vào dung dịch FeCl2, thu được chất rắn gồm Ag và AgCl.
Số phát biểu đúng là
Đáp án đúng là: A
Tính chất của các chất.
Đáp án cần chọn là: A
Nhóm IIA gồm các nguyên tố: Be, Mg, Ca, Sr, Ba. Thực hiện thí nghiệm đốt cháy kim loại nhóm IIA (M) trong khí oxygen: cho mỗi mẩu kim loại Mg, Ca và Ba vào các muôi sắt, hơ nóng trên ngọn lửa đèn cồn, sau đó đưa nhanh vào các bình tam giác chịu nhiệt chứa khí oxygen.
| Đúng | Sai | |
|---|---|---|
| a) Các phản ứng trên xảy ra theo phương trình hoá học có dạng: 2M + O2 → 2MO. | ||
| b) Các kim loại khử oxygen với mức độ tăng dần: Mg, Ca và Ba. | ||
| c) Các kim loại đều cháy mạnh tạo ngọn lửa sáng chói. | ||
| d) Trong các hợp chất, các nguyên tố nhóm IIA có mức oxi hóa là +2 hoặc +1 |
Đáp án đúng là: Đ; Đ; Đ; S
Tính chất hóa học của nguyên tố nhóm IIA.
Đáp án cần chọn là: Đ; Đ; Đ; S
Hai kim loại Cu, Zn có $\text{E}_{\text{Cu}^{\text{2+}}\text{/Cu}}^{\text{o}}$ = 0,34 V, $\text{E}_{\text{Zn}^{\text{2+}}\text{/Zn}}^{\text{o}}$= –0,76V và một pin Galvani Zn-Cu được thiết lập như hình vẽ ở 25°C. Khi pin hoạt động:
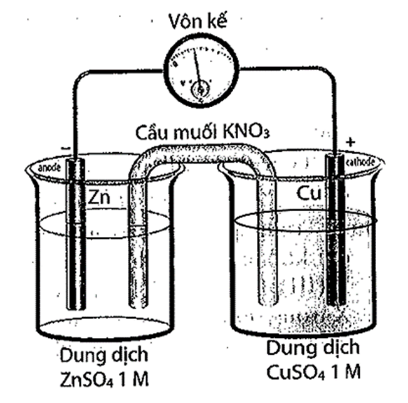
| Đúng | Sai | |
|---|---|---|
| a) Sức điện động của pin là 0,42V. | ||
| b) Nồng độ Zn2+ trong dung dịch ZnSO4 sẽ tăng lên, còn nồng độ Cu2+ trong dung dịch CuSO4 sẽ giảm xuống. | ||
| c) Trong cầu muối ion K+ sẽ di chuyển vào dung dịch ZnSO4 còn ion NO3– sẽ di chuyển vào dung dịch CuSO4. | ||
| d) Phản ứng hóa học xảy ra trong pin là: Zn2+ + Cu → Cu2+ + Zn. |
Đáp án đúng là: S; Đ; Đ; S
Dựa vào lý thuyết pin điện.
Đáp án cần chọn là: S; Đ; Đ; S
Điện phân có nhiều ứng dụng trong thực tiễn sản xuất và đời sống như luyện kim, tinh chế kim loại, mạ điện, sản xuất hóa chất…
| Đúng | Sai | |
|---|---|---|
| a) Để ngăn chặn hiện tượng gỉ sét và mài mòn của một chi tiết máy, người ta phủ lớp đồng (Cu) dày 0,2 mm lên bề mặt của chi tiết máy bằng phương pháp mạ điện. Dung dịch điện phân chứa CuSO4, cực dương là Cu kim loại, cực âm là chi tiết máy có hình trụ (r = 1,7 cm và h = 10 cm). Sự điện phân với dòng điện một chiều I = 6A. Biết hiệu suất điện phân đạt 100%; khối lượng riêng của Cu là 8,96 g/cm³, π = 3,14, F = 96500 C/mol. Thời gian của quá trình mạ điện là 4,12 giờ (kết quả làm tròn đến phần trăm). | ||
| b) Điện phân dung dịch muối NaCl với điện cực trơ, không có màng ngăn xốp thì thu được sản phẩm lànước Javel và khí H2. | ||
| c) Muốn tinh luyện Cu bằng phương pháp điện phân thì khối Cu không tinh khiết phải được nối vào cathode, còn thanh Cu tinh khiết được nối vào anode, khi đó khối lượng Cu tan ra từ anode bằng khối lượng Cu bám vào cathode. | ||
| d) Điện phân nóng chảy hỗn hợp gồm aluminium oxide (Al2O3) và cryolite (Na3AlF6) để sản xuất nhôm (Al) trong công nghiệp. Để điều chế khoảng 400 kg Al cần dùng khoảng 1,7094 tấn quặng bauxite (chứa 52% Al2O3, phần còn lại là Fe2O3, SiO2 và tạp chất trơ) với hiệu suất cả quá trình đạt 85%. |
Đáp án đúng là: S; Đ; S; Đ
a) Độ dày lớp phủ $\delta$ = 0,2 (mm) = 0,02 (cm)
Bán kính r’ = r + $\delta$; h’ = h + 2$\delta$
Thể tích lớp đồng mạ: Vphủ = πr′2h′ − πr2h
Khối lượng đồng bám lên chi tiết: mCu = DVphủ
Áp dụng định luật Faraday để tính thời gian:$t = \dfrac{n_{e}F}{I}$
b) Điện phân dung dịch NaCl không màng ngăn.
c) Tinh luyện kim loại thô bằng phương pháp điện phân dung dịch.
d) $\left. 2Al_{2}O_{3}\underset{cryolite}{\overset{dpnc}{\rightarrow}}4Al + 3O_{2}\uparrow \right.$
$n_{Al_{2}O_{3}} = \dfrac{1}{2}n_{Al}$ ⟹ khối lượng quặng.
Đáp án cần chọn là: S; Đ; S; Đ
Một nhóm học sinh tiến hành thí nghiệm về ăn mòn của kim loại (đinh thép). Nhóm học sinh đưa ra giả thuyết: “Sự ăn mòn kim loại không xảy ra hoặc xảy ra nhanh hay chậm chỉ phụ thuộc vào các chất có trong môi trường”
Thí nghiệm được tiến hành theo các bước sau:
- Rót dung dịch sodium chloride (NaCl) bão hòa vào cốc 1, cốc 2, cốc 3, dầu nhờn (bản chất là hỗn hợp các hydrocarbon) vào cốc 4.
- Cho một đinh thép vào cốc 1 và cốc 4, cho đinh thép được quấn bởi dây kẽm (Zn) vào cốc 2, cho đinh thép được quấn dây đồng (Cu) vào cốc 3 (các đinh thép là thép carbon thường và đã được làm sạch bề mặt).
Các bước được minh họa như hình vẽ dưới đây:
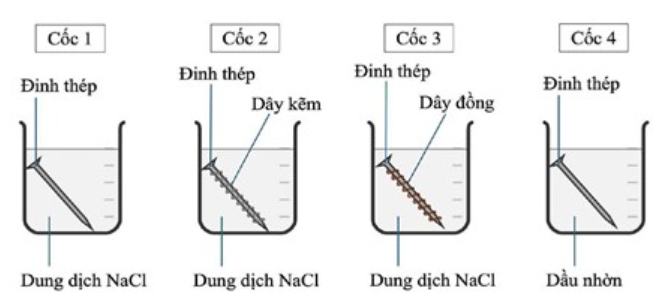
Để 4 cốc trong không khí sau 5 ngày, kết quả thí nghiệm được nhóm học sinh ghi lại theo bảng sau:

| Đúng | Sai | |
|---|---|---|
| a) Ở cốc 1, khi nhúng đinh vào nước muối, sắt bị ăn mòn hóa học. | ||
| b) Ở cốc 2, khi quấn kẽm vào đinh thép rồi ngâm chúng trong dung dịch NaCl, xuất hiện hiện tượng ăn mòn điện hóa, kẽm có tính khử mạnh hơn sắt nên kẽm bị ăn mòn, do đó đinh thép được bảo vệ. | ||
| c) Quấn một dây đồng quanh đinh thép là cách để chống ăn mòn đinh thép trong môi trường có chất điện li. | ||
| d) Với kết quả thí nghiệm như trên, giả thuyết của nhóm học sinh là đúng. |
Đáp án đúng là: S; Đ; S; S
a), c) Điều kiện xảy ra ăn mòn điện hoá.
b) Chống ăn mòn kim loại.
d) Phân tích thí nghiệm để kết luận giả thiết.
Đáp án cần chọn là: S; Đ; S; S
Cho các phát biểu về các nguyên tố kim loại nhóm IA.
(a) Có cấu hình electron lớp ngoài cùng là ns1 (n > 1).
(b) Có số oxi hóa là +1 hoặc +2 trong các hợp chất.
(c) Có tính khử mạnh.
(d) Có bán kính nguyên tử nhỏ.
(e) Tác dụng tốt với dung dịch acid.
Có bao nhiêu phát biểu đúng?
Đáp án đúng là:
Lí thuyết về nguyên tố kim loại nhóm IA.
Đáp án cần điền là: 3
Tiến hành các thí nghiệm sau:
(1) Cho Zn vào dung dịch AgNO3.
(2) Cho Fe vào dung dịch Fe2(SO4)3.
(3) Cho K vào dung dịch MgSO4.
(4) Dẫn khí CO (dư) qua ống nghiệm có bột CuO, nung nóng.
Hãy liệt kê các thí nghiệm có sự tạo thành đơn chất kim loại theo thứ tự tăng dần? (ví dụ 12, 134, …)
Đáp án đúng là:
Dựa vào tính chất hoá học của kim loại.
Đáp án cần điền là: 14
Cho nhiệt độ nóng chảy của một số kim loại như sau: 1330oC; 774oC; 890oC và 688oC. Hãy gán nhiệt độ sôi trên cho các kim loại sau:
(1) Lithium (Li).
(2) Sodium (Na).
(3) Potassium (K).
(4) Rubidium (Rb).
(Ví dụ kết quả gán nhiệt độ sôi là (1); (2); (3); (4) thì điền đáp án là 1234)
Đáp án đúng là:
Trong nhóm IA, theo chiều tăng dần điện tích hạt nhân, nhiệt độ nóng chảy kim loại tăng dần.
Đáp án cần điền là: 4231
Trên nhãn chai dịch truyền tĩnh mạch sodium chloride và glucose (dung dịch X) ghi các thông tin như hình bên.

Nếu thêm b (L) dung dịch HCl a (M) vào 500 mL dung dịch X thu được dung dịch Y (trong đó nồng độ của HCl là 0,01M, biết nồng độ ion Cl- trong X và Y bằng nhau). Thể tích dung dịch HCl đã dùng (mL) là bao nhiêu? (làm tròn đến hàng phần mười).
Đáp án đúng là:
Tính nồng độ ion Cl- trong dung dịch X.
b là thể tích dung dịch HCl thêm vào, lập biểu thức nồng độ HCl trong dung dịch Y bằng 0,01 M.
Lập biểu thức nồng độ Cl- trong dung dịch Y.
Dùng điều nồng độ ion Cl- trong X và Y bằng nhau để lập phương trình.
Giải hệ phương trình ⇒ tính được b.
Đáp án cần điền là: 3,48
Để tìm hiểu về sự ăn mòn kim loại. Một nhóm học sinh đã thực hiện 5 thí nghiệm sau :
Thí nghiệm 1: Cho một dây Zinc (Zn) sạch vào ống nghiệm chứa 2 mL dung dịch HCl 0,2 M.
Thí nghiệm 2: Cho một dây Zinc (Zn) sạch vào ống nghiệm chứa 2 mL dung dịch HCl 0,2 M nhỏ thêm vài giọt dung dịch CuSO4.
Thí nghiệm 3: Cho một dây bạc sạch vào ống nghiệm chứa 2 mL dung dịch HCl 0,2 M.
Thí nghiệm 4: Cho một dây Cu được quấn bởi dây Zinc (Zn) vào ống nghiệm chứa 2 mL dung dịch HCl 0,2 M.
Thí nghiệm 5: Cho một dây Zinc (Zn) sạch vào ống nghiệm chứa 2 mL dung dịch CuSO4 0,2 M.
Liệt kê các thí nghiệm xuất hiện ăn mòn điện hóa theo thứ tự tăng dần? (Ví dụ 123,1234,.)
Đáp án đúng là:
Điều kiện xảy ra ăn mòn điện hóa học:
+ 2 điện cực khác nhau về bản chất (kim loại + kim loại; kim loại + phi kim; kim loại + hợp chất).
+ 2 điện cực phải được tiếp xúc điện với nhau.
+ 2 điện cực cùng được tiếp xúc với dung dịch chất điện li (không khí ẩm).
Đáp án cần điền là: 245
Để mạ đồng một vật dụng kim loại có tổng diện tích bề mặt là 10 cm², người ta tiến hành điện phân dung dịch CuSO4 với cực âm là vật dụng cần mạ và cực dương là lá đồng thô. Biết cường độ dòng điện không đổi là 2 A, hiệu suất điện phân là 90%, khối lượng riêng của tỉnh thể Cu là 8,94 g/cm³ và lượng đồng tạo ra được tính theo công thức Faraday là m =A.I.t/nF (với A là nguyên tử khối của Cu = 64; I là cường độ dòng điện, F là hằng số Faraday = 96485 C/mol, n là số electron mà 1 ion Cu2+ nhận, t là thời gian điện phân tính bằng giây). Thời gian điện phân để lớp mạ có độ dày đồng nhất 0,1 mm là bao nhiêu phút?(Làm tròn kết quả đến hàng đơn vị)
Đáp án đúng là:
VCu = Sbề mặt x Độ dày
mCu = VCu. DCu
H = 90% $\Rightarrow$ mCu (lt) = mCu : H
Theo công thức Faraday: mCu (lt) = $\dfrac{A.I.t}{n.F}$
$\Rightarrow$ t = $\dfrac{m_{Cu{({lt})}.}.n.F}{A.I}$ = $\dfrac{m_{Cu{({lt})}.}.n.F}{A.I}$
Đáp án cần điền là: 25


