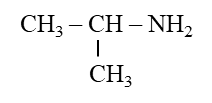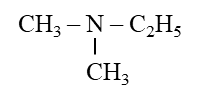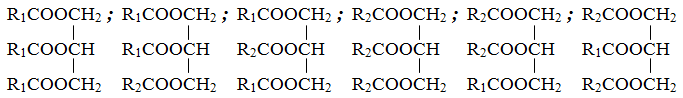Acid béo omega-3 và omega-6 đều có vai trò quan trọng đối với cơ thể, giúp phòng ngừa nhiều loại bệnh. Chất nào sau đây thuộc loại acid béo omega-3 ?
Đáp án đúng là: A
Dựa vào vị trí liên kết C=C tính từ đầu nhóm methyl
Đáp án cần chọn là: A
Ruộng lúa mới cấy được một tháng. Lúa đã cứng cây và đang phát triển cần được bón thúc bằng phân đạm urea để lúa phát triển tốt hơn. Nhưng rêu xanh đang phủ kín mặt ruộng, cần phải bón vôi toả Ca(OH)2 để diệt rêu. Biết rằng trong nước urea có thể chuyển hoá thành (NH4)2CO3. Phương án tối ưu để giải quyết đồng thời hai vấn đề trên là
Đáp án đúng là: A
Lí thuyết về phân bón hoá học.
Đáp án cần chọn là: A
Với nhu cầu chế tạo vật liệu an toàn với môi trường, năm 2005 sản phẩm "hộp bã mía" - bao bì từ thực vật và an toàn cho sức khoẻ với nhiều tính năng vượt trội so với hộp xốp đã ra đời. Đây là loại bao bì có thành phần hoàn toàn tự nhiên, phần lớn là sợi bã mía từ nhà máy đường, với khả năng chịu nhiệt rộng từ -40 đến 200 0C, bền nhiệt trong lò vi sóng, lò nướng nên an toàn với sức khoẻ con người. Trong khi đó hộp xốp đựng thức ăn nhanh được làm từ chất dẻo PS, có nhiệt độ nóng chảy 70 - 80 0C.
Cho các phát biểu sau:
a) Thành phần chính của hộp bã mía là cellulose.
b) Hộp bã mía phân huỷ sinh học được nên thân thiện với môi trường.
c) Hộp xốp đựng thức ăn nhanh có thể sử dụng trong lò vi sóng và là vật liệu khó phân huỷ sinh học.
d) Hộp bã mía có thành phần chính là polymer thiên nhiên, hộp xốp từ chất dẻo là polymer tổng hợp.
Các phát biểu đúng là
Đáp án đúng là: B
Lí thuyết về polymer.
Đáp án cần chọn là: B
Calcium là nguyên tố kim loại đóng góp vai trò thiết yếu cho việc phát triển cơ thể động vật, đồng thời góp phần duy trì hoạt động của cơ bắp, truyền dẫn thần kinh, tăng cường khả năng miễn dịch,…Trong cơ thể con người, phần lớn calcium tập trung ở
Đáp án đúng là: D
Dựa vào ứng dụng của kim loại kiềm thổ.
Đáp án cần chọn là: D
Số đồng vị bền của nguyên tố neon (Ne) được suy ra từ phổ khối lượng ở hình bên là
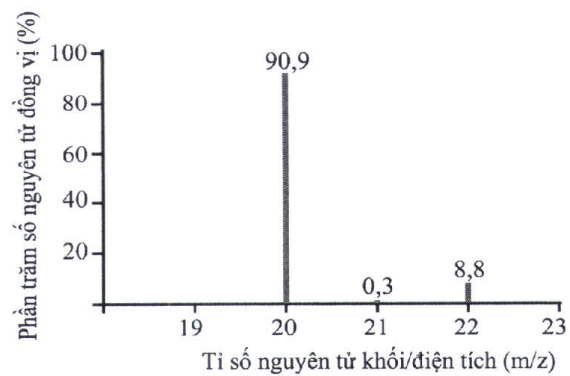
Đáp án đúng là: C
Quan sát phổ khối lượng.
Đáp án cần chọn là: C
Trong phân tử amylose, các gốc …(1)… liên kết với nhau bằng liên kết …(2)… Các cụm từ thích hợp điền vào chỗ trống (1) và (2) là
Đáp án đúng là: A
Lí thuyết về đặc điểm cấu tạo của amylose.
Đáp án cần chọn là: A
Trong phức chất [Fe(OH2)]2+, mỗi phân tử nước sử dụng bao nhiêu electron để tạo liên kết phối trí với AO trống của ion Fe2+?
Đáp án đúng là: B
Lí thuyết về phức chất.
Đáp án cần chọn là: B
Phản ứng chlorine hóa methane khi chiếu sáng xảy ra theo cơ chế gốc gồm ba giai đoạn: khơi mào, phát triển mạch và tắt mạch. Trong đó, giai đoạn phát triển mạch diễn ra như sau:
Cl• + CH4 → HCl + •CH3
•CH3 + Cl2 → CH3Cl + Cl•
Nhận định nào sau đây không đúng về giai đoạn này ?
Đáp án đúng là: D
Dựa vào cơ chế phản ứng chlorine hóa methane.
Đáp án cần chọn là: D
Để tách curcumin từ củ nghệ Curcuma longa, người ta nghiền nhỏ củ nghệ tươi rồi ngâm trong cồn 90%, đun nóng, sau đó lọc bỏ phần bã, lấy phần nước lọc, loại bớt dung môi, làm lạnh và để yên một thời gian rồi lọc lấy kết tủa màu vàng là curcumin. Hãy cho biết trong các quá trình trên người ta đã sử dụng kĩ thuật nào để lấy được curcumin từ củ nghệ tươi.
Đáp án đúng là: C
Lý thuyết về một số phương pháp tách chất.
Đáp án cần chọn là: C
Phản ứng hóa học nào dưới đây mô tả quá trình sodium hydrogencarbonate trung hòa lượng hydrochloric acid dư trong dạ dày?
Đáp án đúng là: A
Ứng dụng, cơ chế hoạt động của một số hợp chất nhóm IA.
Đáp án cần chọn là: A
Phản ứng phân hủy polystyrene xảy ra theo phương trình hóa học sau:
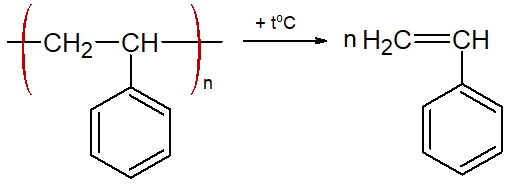
Phản ứng trên thuộc loại phản ứng
Đáp án đúng là: A
Tính chất hoá học của polymer.
Đáp án cần chọn là: A
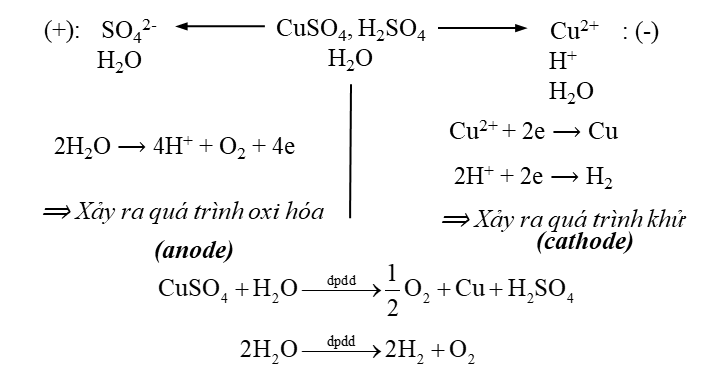
Để mạ đồng Cu cho một vật, người ta điện phân dung dịch chứa CuSO4 và H2SO4 với một điện cực là vật cần mạ. Khi đó ngoài kim loại đồng sinh ra và phủ lên bề mặt vật cần mạ còn thu được các khí H2 và O2. Trong các sản phẩm Cu, H2 và O2 sản phẩm nào thu được tại anode?
Đáp án đúng là: C
Nguyên tắc, thứ tự điện phân:
(-) Cathode: xảy ra quá trình khử, chất có tính oxi hóa mạnh hơn điện phân trước
(+) Anode: xảy ra quá tình oxi hóa, chất có tính khử mạnh hơn điện phân trước
Đáp án cần chọn là: C
Tiến hành thí nghiệm của glucose với thuốc thử Tollens theo các bước sau đây:
Bước 1: Cho vào ống nghiệm sạch 1 mL dung dịch AgNO3 1%, cho thêm một vài giọt dung dịch NaOH 10%, sau đó thêm từng giọt dung dịch NH3 5% và lắc đều cho đến khi kết tủa tan hết.
Bước 2: Thêm tiếp 1 mL dung dịch glucose,ngâm ống nghiệm vào cốc nước nóng.
Nhận định nào sau đây là sai?
Đáp án đúng là: B
Tính chất hóa học glucose.
Đáp án cần chọn là: B
X, Y, Z là ba chất hữu cơ được kí hiệu ngẫu nhiên trong các chất HCOOCH3, CH3COOH và CH3CH2CH2OH. Nhiệt độ sôi của X, Y, Z được cho trong bảng sau:

Các chất X và Y lần lượt là
Đáp án đúng là: D
Đối với các hợp chất hữu cơ có phân tử khối tương đương, nhiệt độ sôi: carboxylic acid > alcohol >ester.
Đáp án cần chọn là: D
Một học sinh sử dụng các thanh kim loại, dây dẫn, bóng đèn nhỏ và các quả chanh để lắp ráp các hệ thống như hình dưới đây:
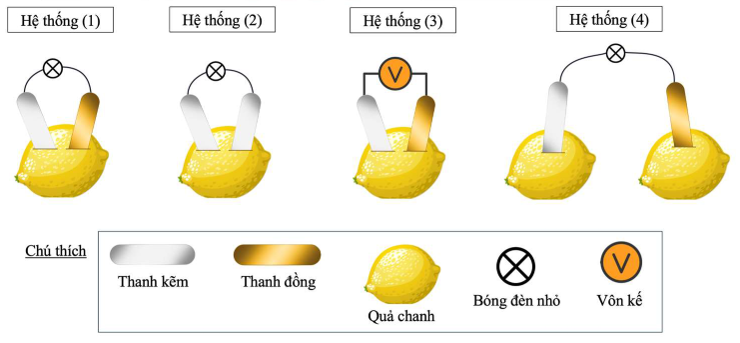
Ở các hệ thống (1), (2), (3), khi lắp ráp không để hai thanh kim loại chạm nhau. Cho các phát biểu sau:
(1) Các bóng đèn ở hệ thống (1) và (2) đều phát sáng do có dòng điện chạy qua.
(2) Ở hệ thống (2), nếu thay hai thanh kẽm bằng hai thanh đồng (Cu) thì đèn vẫn sáng.
(3) Ở hệ thống (3), giá trị đọc được trên vôn kế chính là sức điện động của pin Zn-Cu.
(4) Bóng đèn ở hệ thống (4) sáng hơn đèn ở hệ thống (1) do sử dụng nhiều chất điện li hơn.
(5) Ở hệ thống (3), giá trị đọc được trên vôn kế sẽ giảm theo thời gian.
Các phát biểu đúng là
Đáp án đúng là: B
Pin điện hoá.
Đáp án cần chọn là: B
Kim loại kiềm thuộc kim loại nhẹ và có khối lượng riêng nhỏ là do nguyên nhân nào sau đây?
Đáp án đúng là: B
Lí thuyết về kim loại kiềm.
Đáp án cần chọn là: B
Đốt cháy kim loại magnesium trong bình chứa khí oxygen, thu được oxide có công thức hóa học là
Đáp án đúng là: A
Tính chất hóa học của kim loại.
Phản ứng oxi hóa kim loại bởi oxygen: $4M + n{O_2}\xrightarrow{{{t^o}}}2{M_2}{O_n}$
Đáp án cần chọn là: A
Trong các hợp chất hữu cơ dưới đây, chất nào là amine bậc 2?
Đáp án đúng là: B
Amine bậc 2 là những amine khi thay thế 2 nguyên tử hydrogen trong ammonia bằng gốc hydrocarbon.
Đáp án cần chọn là: B
Trên thế giới, zinc (kẽm) được sản xuất chủ yếu từ quặng zinc blende có thành phần chính là ZnS. Một nhà máy luyện kim sản xuất Zn từ 60 tấn quặng zinc blend (chứa 80% ZnS, còn lại là tạp chất không chứa kẽm) với hiệu suất cả quá trình đạt 90% theo các giai đoạn:
+ Đốt quặng zinc blende:2ZnS(s) + 3O2(g) ⟶ 2ZnO(s) + 2SO2(g) (1)
+ Khử zinc oxide ở nhiệt độ cao bằng than cốc: ZnO(s) + C(s) ⟶ Zn(g) + CO(g) (2)
Toàn bộ lượng kẽm tạo ra được đúc thành k thanh kẽm hình hộp chữ nhật: chiều dài 120 cm, chiều rộng 25 cm và chiều cao 15 cm. Biết khối lượng riêng của kẽm là 7,14 g/cm³.
| Đúng | Sai | |
|---|---|---|
| a) Trong phản ứng (2), kẽm sinh ra ở thể rắn. | ||
| b) Theo sơ đồ trên, quặng sphalerite được nghiền, tuyển… sau đó được chuyển hoá thành zinc oxide, cuối cùng tách được kim loại kẽm bằng phương pháp thuỷ luyện. | ||
| c) Trong phản ứng (1), chất khử là ZnS và chất oxi hóa là O2. | ||
| d) Giá trị k bằng 90 (kết quả làm tròn đến hàng đơn vị). |
Đáp án đúng là: S; S; Đ; Đ
a), b): Dựa vào phương trình điều chế Zn từ ZnS.
c): Chất khử là chất nhường electron; chất oxi hóa là chất nhận electron.
d) \({{\rm{m}}_{{\rm{ZnS}}}} = {{\rm{m}}_{{\rm{zinc blende}}}}.80\% \)⟶ nZnS
H = 90% nên \({{\rm{n}}_{{\rm{Zn}}}} = {{\rm{n}}_{{\rm{ZnS}}}}.90\% \) ⟶ mZn
Khỗi lượng mỗi thanh kẽm: m = V.D
Số thanh kẽm: k = \(\dfrac{{{{\rm{m}}_{{\rm{Zn}}}}}}{{\rm{m}}}\)
Đáp án cần chọn là: S; S; Đ; Đ
Máy tạo nhịp tim là một thiết bị nhỏ dùng để điều trị một số chứng rối loạn nhịp tim. Khi bị rối loạn nhịp tim, tim có thể đập quá nhanh, quá chậm hoặc nhịp tim không đều. Máy tạo nhịp tim gửi các xung điện để giúp tim đập ở tốc độ và nhịp điệu bình thường. Máy tạo nhịp tim gồm có 2 phần chính: máy tạo nhịp (Pacemaker) và dây điện cực (Electrode). Bộ phận quan trọng nhất của máy tạo nhịp tim là một hệ pin điện hóa lithium – iodine (gồm hai cặp oxi hóa khử Li+/Li và I2/2I-). Hai điện cực được đặt vào tim, phát sinh dòng điện nhỏ kích thích tim đập ổn định. Cho biết: E°Li+/Li = -3,04V; E°I2/2I- = +0,54V; Nguyên tử khối của Li = 6,9; điện tích của 1 mol electron là 96500 C/mol; q = I.t, trong đó q là điện tích (C), I là cường độ dòng điện (A), t là thời gian (s), 1 năm = 365 ngày.
q = I.t, trong đó q là điện tích (C), I là cường độ dòng điện (A), t là thời gian (s), 1 năm = 365 ngày.
| Đúng | Sai | |
|---|---|---|
| a) Máy tạo nhịp tim có thể được đặt tạm thời hay vĩnh viễn trong cơ thể tùy theo tình trạng sức khỏe và các bệnh lý kèm theo của bệnh nhân. | ||
| b) Khi pin hoạt động lithium đóng vai trò là anode, tại anode xảy ra quá trình khử. | ||
| c) Sức điện động chuẩn của pin E°pin = 3,58V. | ||
| d) Nếu pin tạo ra một dòng điện ổn định bằng 2,5.10-5 A thì một pin được chế tạo bởi 0,5 gam lithium có thể hoạt động tối đa trong thời gian 8 năm. |
Đáp án đúng là: Đ; S; Đ; S
Lí thuyết về pin điện hoá.
Đáp án cần chọn là: Đ; S; Đ; S
Isoamyl acetate thường được sử dụng làm chất phụ gia để tạo mùi chuối trong thực phẩm hoặc được dùng làm hương liệu nhân tạo. Một học sinh tiến hành điều chế isoamyl acetate theo các bước sau:
Bước 1: Cho vào bình cầu 26,4 mL isoamyl alcohol (d = 0,81 g/mL), 40 mL acetic acid (d =1,049 g/mL) và 2,5 mL H2SO4 đậm đặc, cho thêm vào bình vài viên đá bọt. Lắp ống sinh hàn hồi lưu thẳng đứng vào miệng bình cầu. Sau đó đun nóng bình cầu trong khoảng 1,5 giờ.
Bước 2: Sau khi đun, để nguội rồi rót sản phẩm vào phễu chiết, thêm 50 mL nước cất vào phiễu, lắc đều rồi để yên khoảng 5 phút, lúc đó chất lỏng tách thành hai lớp, loại bỏ phần chất lỏng phía dưới, lấy phần chất lỏng phía trên.
Bước 3: Cho từ từ dung dịch Na2CO3 10% vào phần chất lỏng thu lấy ở bước 2 và lắc đều cho đến khi không còn khí thoát ra, thêm tiếp 20 mL dung dịch NaCl bão hòa rồi để yên khi đó chất lỏng tách thành hai lớp. Chiết lấy phần chất lỏng phía trên, thu được 26,0 mL isoamyl acetate (d = 0,876 g/mL).
| Đúng | Sai | |
|---|---|---|
| a) Biết tổng lượng isoamyl acetate bị thất thoát ở bước 2 và 3 là 5% so với lượng thu được ở trên, hiệu suất phản ứng ester hóa ở bước 1 bằng 72,1 %. | ||
| b) Việc lắp ống sinh hàn ở bước 1 nhằm mục đích hạn chế sự thất thoát chất lỏng ra khỏi bình cầu. | ||
| c) Tiến hành đo phổ khối lượng (MS) của isoamyl acetate sẽ xuất hiện peak ion phân tử có m/z=130 | ||
| d) Thêm dung dịch Na2CO3 ở bước 3 nhằm mục đích loại bỏ acid lẫn trong isoamyl acetate. |
Đáp án đúng là: S; Đ; Đ; Đ
a) misoamyl alcohol = Visoamyl alcohol.Disoamyl alcohol $\rightarrow$ nisoamyl alcohol
$\text{m}_{\text{CH}_{3}\text{COOH}} = \text{V}_{\text{CH}_{3}\text{COOH}}.\text{D}_{\text{CH}_{3}\text{COOH}}$ $\left. \rightarrow\text{n}_{\text{CH}_{3}\text{COOH}} \right.$
Nếu không thất thoát ở bước 2 và 3 thì lượng ester thu được: Vester = Vester + 5%Vester
$\rightarrow$ mester = Vester. Dester$\rightarrow$ nester
H = $\dfrac{\text{n}_{\text{ester}}}{\text{n}_{\text{isoamyl~alcohol}}}.100\%$
b), c), d): Lí thuyết về điều chế ester.
Đáp án cần chọn là: S; Đ; Đ; Đ
Hoạt tính xúc tác của enzyme càng cao, tốc độ thủy phân protein càng lớn. Hoạt tính enzyme phụ thuộc vào các yếu tố như nhiệt độ, pH. Một nhóm học sinh đã khảo sát ảnh hưởng của pH đến hoạt tính của enzyme tiêu hoá protein ở người. Nhóm tiến hành thí nghiệm thuỷ phân albumin (protein có trong lòng trắng trứng) bằng enzyme pepsin ở nhiệt độ không đổi nhưng thay đổi pH của môi trường. Kết quả thu được như sau:

Sau đó, nhóm học sinh tiến hành thí nghiệm tương tự với enzyme chymotrypsin, thu được đồ thị như hình bên. Từ kết quả thí nghiệm, nhóm học sinh đã đưa ra các nhận định sau:
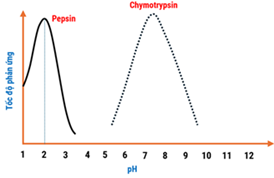
| Đúng | Sai | |
|---|---|---|
| a) Pepsin hoạt động tốt nhất ở pH = 2. | ||
| b) Albumin là protein dạng sợi, không tan trong nước nên ban đầu dung dịch bị đục. | ||
| c) Ở ống nghiệm 3, nếu thay Pepsin thành Chymotrypsin thì hiện tượng quan sát được là “từ đục thành trong” sau thí nghiệm. | ||
| d) Từ kết quả thí nghiệm thì enzyme pepsin và chymotrypsin đều hoạt động tốt trong môi trường acid. |
Đáp án đúng là: Đ; S; Đ; S
a): Lí thuyết về tính chất vật lí của protein.
b), c), d): Dựa vào kết quả thí nghiệm thu được và đồ thị tốc độ phản ứng với enzyme pepsin và chymotrypsin.
Đáp án cần chọn là: Đ; S; Đ; S
Cho glycerol phản ứng với hỗn hợp acid béo gồm C17H35COOH và C15H31COOH trong điều kiện thích hợp. Số triester được tạo ra tối đa thu được là bao nhiêu?
Đáp án đúng là:
* Cách 1: Dựa vào phản ứng ester hóa để xác định sản phẩm triester được tạo thành.
* Cách 2: Áp dụng công thức: Số loại triester được tạo = $\dfrac{{{n^2}(n + 1)}}{2}$ với n: số acid béo.
Đáp án cần điền là: 6
Cho các chất: alanine (1), aminoacetic acid (2), methylamine (3), aniline (4), glutamic acid (5). Chất nào trong số các chất trên tan tốt trong nước? Liệt kê đáp án theo dãy số thứ tự tăng dần (ví dụ: 1234, 235,…).
Đáp án đúng là:
Lý thuyết về tính chất vật lí về amine và amino acid.
Đáp án cần điền là: 1235
PBS - Poly(butylene succinate), có tên thương mại Bionolle, là một polymer phân huỷ sinh học có tính dẻo và bền nhiệt tương tự polyethylene (PE). Nhờ cấu trúc mạch chính chứa các nhóm ester dễ bị thủy phân, PBS có khả năng phân rã trong môi trường tự nhiên. Với đặc tính này, PBS được ứng dụng rộng rãi trong sản xuất bao bì và túi nylon thân thiện với môi trường, trở thành giải pháp tiềm năng thay thế các loại nhựa truyền thống khó phân huỷ. PBS được tổng hợp bằng phản ứng trùng ngưng giữa 2 monomer sau:
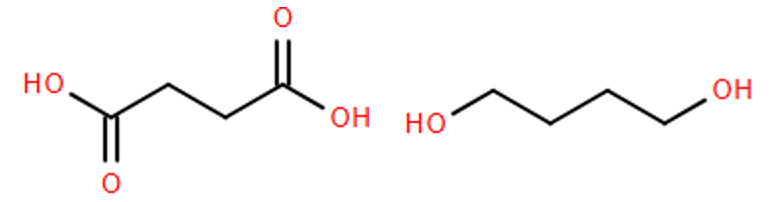
Tính khối lượng của một mắt xích polymer PBS theo đơn vị amu.
Đáp án đúng là:
Xác định công thức cấu tạo mắt xích của PBS ⟶ tính khối lượng phân tử.
Đáp án cần điền là: 172
Nước cứng gây nhiều trở ngại cho đời sống thường ngày. Các nguồn nước ngầm hoặc nước ở các ao hồ, sông suối thường có độ cứng cao bởi quá trình hòa tan các ion Ca2+, Mg2+ có trong thành phần của lớp trầm tích đá vôi… Dựa vào chỉ số tổng nồng độ của các ion Ca2+ và Mg2+ để phân chia độ cứng thành các cấp độ khác nhau như hình
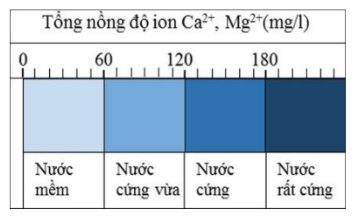
Cho các phát biểu sau:
(1) Có thể dùng Na2CO3 để làm mềm nước có tính cứng toàn phần.
(2) Nước có tổng nồng độ ion Ca2+, Mg2+ bằng 150 mg/L thuộc loại nước cứng.
(3) Nước cứng làm cho xà phòng có ít bọt, giảm khả năng tẩy rửa của xà phòng.
(4) Nước tự nhiên có chứa các ion $\text{Ca}^{2 +},\text{Mg}^{2 +},\text{Cl}^{-},\text{HCO}_{3}^{-}$ gọi là nước có tính vĩnh cửu.
(5) Để loại bỏ lớp cặn trong ấm đun nước lâu ngày có thể dùng dung dịch giấm ăn.
Liệt kê các phát biểu đúng theo số thứ tự tăng dần.
Đáp án đúng là:
Nước cứng là nước có chứa nhiều ion Ca2+ và Mg2+.
Nước mền là nước chứa ít hoặc không chứa ion Ca2+ và Mg2+.
Phân loại nước cứng
+) Nước cứng tạm thời: Mg(HCO3)2, Ca(HCO3)2
+) Nước cứng vĩnh cửu: MgCl2, MgSO4, CaCl2, CaSO4
+) Nước cứng toàn phần: nước cứng tạm thời + nước cứng vĩnh cửu
Phương pháp làm mềm nước cứng.
Đáp án cần điền là: 1235
Để xác định hàm lượng oxygen (O2) tan trong nước, người ta lấy 100,0 mL nước rồi cho ngay manganese sulphate (MnSO4, dư) và sodium hydroxide (NaOH) vào nước. Sau khi lắc kĩ (không cho tiếp xúc với không khí), manganese(II) hydroxide (Mn(OH)2) bị O2 oxi hóa thành manganese oxohydroxide (MnO(OH)2). Thêm acid (dư) và cho tiếp potassium iodide (KI, dư) vào hỗn hợp, thì ion idodine (I-) bị MnO(OH)2 oxi hóa thành ioddine (I2). Lượng I2 sinh ra phản ứng vừa đủ với 10,5 mL dung dịch Na2S2O3 0,01M (sodium thiosulphate). Biết các phản ứng xảy ra như sau:
\({\rm{M}}{{\rm{n}}^{2 + }} + {\rm{O}}{{\rm{H}}^ - } \to {\rm{Mn}}{({\rm{OH)}}_2}\) (1)
\({\rm{Mn}}{({\rm{OH)}}_2} + {{\rm{O}}_2} \to {\rm{MnO}}{({\rm{OH)}}_2}\)(2)
\({\rm{MnO}}{({\rm{OH)}}_2} + {{\rm{I}}^ - } + {{\rm{H}}^ + } \to {\rm{M}}{{\rm{n}}^{2 + }} + {{\rm{I}}_2} + {{\rm{H}}_2}{\rm{O}}\)(3)
\({{\rm{I}}_2} + {\rm{N}}{{\rm{a}}_2}{{\rm{S}}_2}{{\rm{O}}_3} \to {\rm{N}}{{\rm{a}}_2}{{\rm{S}}_4}{{\rm{O}}_6} + {\rm{NaI}}\)(4)
Hàm lượng O2 tan trong nước (tính theo mg O2/1L) là a. Giá trị của a là bao nhiêu? (Làm tròn kết quả đến hàng phần mười)
Đáp án đúng là:
\({{\rm{n}}_{{\rm{N}}{{\rm{a}}_2}{{\rm{S}}_2}{{\rm{O}}_3}}} = {\rm{V}}{\rm{.}}{{\rm{C}}_{\rm{M}}}\)
Theo PTHH (2)(3)(4) → \({{\rm{n}}_{{{\rm{O}}_2}}} = \dfrac{1}{4}{{\rm{n}}_{{\rm{N}}{{\rm{a}}_2}{{\rm{S}}_2}{{\rm{O}}_3}}}\) \( \to {{\rm{n}}_{{{\rm{O}}_2}}}\)
Hàm lượng O2 tan trong nước là a = \(\dfrac{{{{\rm{m}}_{{{\rm{O}}_2}}}}}{{{{\rm{V}}_{{\rm{dd}}}}}}\)
Đáp án cần điền là: 8,4
Nung 25 gam một mẫu quặng malachite có thành phần chính là Cu(OH)2.CuCO3 (còn lại là tạp chất trơ) trong không khí đến khối lượng không đổi, theo sơ đồ phản ứng:
$Cu{(OH)}_{2}.CuCO_{3}\overset{t^{o}}{\rightarrow}CuO + H_{2}O + CO_{2}$
Cho toàn bộ lượng chất rắn thu được (gồm CuO và tạp chất trơ) vào cốc thủy tinh, sau đó cho từ từ dung dịch H2SO4 19,6% vào cốc cho đến khi chất rắn không tan thêm được nữa thì dừng lại, lọc bỏ tạp chất trơ thu được dung dịch X. Làm lạnh toàn bộ dung dịch X xuống 10oC thu được dung dịch Y có nồng độ 14,16% và tách ra 25 gam tinh thể CuSO4.5H2O. Biết x% là phần trăm theo khối lượng của Cu trong 25 gam mẫu quặng malachite trên. Tính giá trị của x. (Làm tròn kết quả đến hàng đơn vị).
Đáp án đúng là:
Đặt nCu = a (mol)
Phản ứng hoà tan CuO:
$CuO + H_{2}SO_{4}\overset{}{\rightarrow}CuSO_{4} + H_{2}O$
Dung dịch X là dung dịch CuSO4
mdd X = mCuO + mdd H2SO4
Làm lạnh dung dịch X ⟶ Dung dịch Y + 25 gam tinh thể CuSO4.5H2O
⟹ mdd Y = mdd X – 25
⟹ Số mol CuSO4 trong dung dịch Y
Hàm lượng Cu trong quặng: $x = \dfrac{m_{Cu}}{25}.100\%$
Đáp án cần điền là: 41