
Phản ứng giải phóng năng lượng dưới dạng nhiệt gọi là
Đáp án đúng là: A
Khái niệm về phản ứng toả nhiệt.
Đáp án cần chọn là: A
Trong phản ứng oxi hoá – khử, chất oxi hoá là chất
Đáp án đúng là: A
Khái niệm về chất oxi hoá trong phản ứng oxi hoá khử.
Đáp án cần chọn là: A
Phương trình hóa học nào dưới đây biểu thị enthalpy tạo thành chuẩn của CO (g)?
Đáp án đúng là: D
Enthalpy tạo thành của chất.
Đáp án cần chọn là: D
Khi xảy ra phản ứng hóa học H2 + Br2 → 2HBr, lượng chất của Br2 thay đổi như thế nào theo thời gian?
Đáp án đúng là: A
Dựa vào lí thuyết về tốc độ phản ứng.
Đáp án cần chọn là: A
Trong phản ứng Zn + 2HCl $\overset{}{\rightarrow}$ ZnCl2 + H2. Chất oxi hóa là
Đáp án đúng là: D
Chất oxi hoá là chất nhận electron.
Chất khử là chất nhường electron.
Đáp án cần chọn là: D
Cho phương trình nhiệt hóa học của phản ứng:
2H2(g) + O2(g) → 2H2O(l) $\Delta_{r}H_{298}^{0}$= −571,68 kJ
Phản ứng trên là phản ứng
Đáp án đúng là: B
$\Delta_{r}H_{298}^{0}$ > 0 ⟹ phản ứng thu nhiệt
$\Delta_{r}H_{298}^{0}$ < 0 ⟹ phản ứng toả nhiệt
Đáp án cần chọn là: B
Yếu tố nào ảnh hưởng đến tốc độ phản ứng của phản ứng hóa học sau: Phản ứng cháy diễn ra mạnh và nhanh hơn khi đưa lưu huỳnh đang cháy ngoài không khí vào lọ đựng khí oxygen.
Đáp án đúng là: B
Các yếu tố ảnh hưởng đến tốc độ phản ứng.
Đáp án cần chọn là: B
Cho các phản ứng dưới đây:
(1) CO(g) + ½ O2 (g) → CO2(g) $\Delta_{r}H_{298}^{0}$= - 283 kJ
(2) C(s) + H2O(g) → CO(g) + H2(g) $\Delta_{r}H_{298}^{0}$= + 131,25 kJ
(3) H2(g) + F2(g) → 2HF(g) $\Delta_{r}H_{298}^{0}$= - 546 kJ
(4) H2(g) + Cl2(g) → 2HCl(g) $\Delta_{r}H_{298}^{0}$= - 184,62 kJ
Phản ứng xảy ra thuận lợi nhất là
Đáp án đúng là: C
$\Delta_{r}H_{298}^{0}$ càng âm thì phản ứng càng diễn ra thuận lợi.
Đáp án cần chọn là: C
Xét phản ứng: H2 + Cl2 ⟶ 2HCl
Nghiên cứu sự thay đổi nồng độ một chất trong phản ứng theo thời gian, thu được đồ thị hình bên.
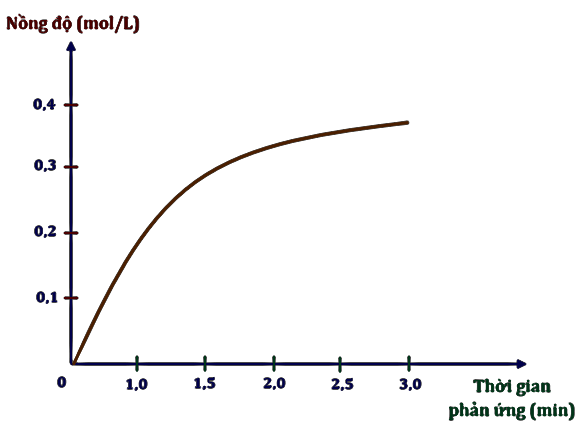
Đồ thị mô tả sự thay đổi nồng độ theo thời gian của chất nào?
Đáp án đúng là: B
Khi tham gia phản ứng, nồng độ chất tham gia giảm dần, nồng độ chất sản phẩm tăng dần theo thời gian.
Đáp án cần chọn là: B
Số oxi hóa của nguyên tố hydrogen trong hầu hết các hợp chất bằng
Đáp án đúng là: B
Số oxi hoá của các nguyên tố trong hợp chất.
Đáp án cần chọn là: B
Một phản ứng hóa học xảy ra theo phương trình: $\left. \text{A} + \text{B}\rightarrow\text{C} \right.$ Nồng độ ban đầu của chất A là 0,8M, chất B là 1 M . Sau 20 phút, nồng độ chất A giảm xuống còn 0,78M.
Trả lời cho các câu 11, 12 dưới đây:
Sau 20 phút, nồng độ mol của chất B là
Đáp án đúng là: B
CB phản ứng = CA phản ứng = CA ban đầu – CA sau phản ứng
CB phản ứng = CB ban đầu – CB sau phản ứng
Đáp án cần chọn là: B
Tốc độ trung bình của phản ứng trong khoảng thời gian nói trên.
Đáp án đúng là: B
Tốc độ trung bình của phản ứng: $\overline{v} = - \dfrac{\text{ΔC}_{\text{A}}}{\text{Δt}}$
Đáp án cần chọn là: B
Sulfur dioxide là một chất có nhiều ứng dụng trong công nghiệp (dùng để sản xuất sulfuric acid, tẩy trắng bột giấy trong công nghiệp giấy, tẩy trắng dung dịch đường trong sản xuất đường tinh luyện..) và giúp ngăn cản sự phát triển của một số vi khuẩn và nấm gây hại cho thực phẩm. Ở áp suất 1 bar và nhiệt độ 25°C, phản ứng giữa mol sulfur với oxygen xảy ra theo phương trình "$\left. S(s) + O_{2}(g)\rightarrow SO_{2}(g) \right.$” và tỏa ra một lượng nhiệt là 296,9kJ.
| Đúng | Sai | |
|---|---|---|
| a) Biến thiên enthalpy chuẩn của phản ứng là 296,9 kJ mol-1 | ||
| b) Enthalpy tạo thành chuẩn của sulfur dioxide bằng -296,9 kJ. | ||
| c) Sulfur dioxide vừa có thể là chất khử vừa có thể là chất oxi hóa, tùy thuộc vào phản ứng mà nó tham gia. | ||
| d) 0,5 mol sulfur tác dụng hết với oxygen giải phóng 148,45kJ năng lượng dưới dạng nhiệt. |
Đáp án đúng là: S; Đ; Đ; Đ
a) Biến thiên enthalpy của phản ứng.
b) Enthaloy tạo thành của phản ứng.
c) Phản ứng oxi hóa khử.
d) Năng lượng của phản ứng hóa học.
Đáp án cần chọn là: S; Đ; Đ; Đ
Phản ứng xảy ra khi cho magnesium (Mg) vào dung dịch hydrochloric acid (HCl) là Mg(s) + 2HCl(aq) → MgCl2(aq) + H2(g) Một nhóm học sinh thực hiện các thí nghiệm như sau:
Thí nghiệm 1: Cho m gam Mg (dạng viên) vào V mL dung dịch HCl dư, nồng độ 0,5M.
Thí nghiệm 2: Cho m gam Mg (dạng viên) vào V mL dung dịch HCl dư, nồng độ 1,5M.
Thí nghiệm 3: Cho m gam Mg (dạng bột) vào V mL dung dịch HCl dư, nồng độ 1,5M.
| Đúng | Sai | |
|---|---|---|
| a) Phản ứng xảy ra trong thí nghiệm trên là phản ứng oxi hóa khử. | ||
| b) Bọt khí H2 thoát ra ở thí nghiệm 1 nhanh hơn thí nghiệm 2. | ||
| c) Tốc độ tan hết của Mg ở thí nghiệm 3 nhanh hơn thí nghiệm 2. | ||
| d) Nếu m = 4,8 gam, sau khi phản ứng xảy ra hoàn toàn thì thể tích khí H2 thu được (đo ở điều kiện chuẩn) là 4,958 lít. |
Đáp án đúng là: Đ; S; Đ; Đ
a) Phản ứng oxi hóa – khử là phản ứng hóa học trong đó có sự thay đổi số oxi hóa của ít nhất một nguyên tố hóa học.
b), c) Các yếu tố ảnh hưởng đến tốc độ phản ứng.
+ Khi tăng nồng độ, nhiệt độ, áp suất thì tốc độ phản ứng tăng
+ Diện tích bề mặt càng lớn thì tốc độ phản ứng càng lớn
+ Chất xúc tác làm tăng tốc độ phản ứng nhưng không bị thay đổi cả về lượng và chất sau phản ứng.
d) Tính theo phương trình hoá học.
Đáp án cần chọn là: Đ; S; Đ; Đ
Số oxi hóa cao nhất mà nguyên tử chlorine thể hiện được trong các hợp chất là +a. Giá trị của a là bao nhiêu?
Đáp án đúng là:
Dựa vào lý thuyết về halogen.
Đáp án cần điền là: 7
Xét phản ứng nhiệt hóa học sau:
$\left. \text{NaOH}\left( \text{aq} \right) + \text{HCl}\left( \text{aq} \right)\rightarrow\text{NaCl}\left( \text{aq} \right) + \text{H}_{2}\text{O}\left( \text{l} \right) \right.$ $\Delta_{\text{r}}\text{H}_{298}^{{^\circ}} = - 57,3\mspace{6mu}\text{kJ}$
Nhiệt lượng tỏa ra cần để trung hòa hết 40 g NaOH là bao nhiêu?
Đáp án đúng là:
Q= nNaOH . 57,3
Đáp án cần điền là: 57,3
Tiến hành thí nghiệm xác định hàm lượng FeO2.Cr2O3 trong quặng sắt chromite (chứa tạp chất trơ) theo các bước sau:
Bước 1: nung nóng 5,6 gam quặng iron chromite với lượng dư KOH nóng chảy có mặt khí O2 thu được K2CrO4.Fe2O3 và H2O.
Bước 2: để nguội, chuyển toàn bộ sản phẩm vào cốc đựng nước, khuấy đều, lọc lấy phần dung dịch (X). Cho H2SO4 loãng, dư vào X, thêm nước thu được 1 L dung dịch (Y).
Bước 3: nhỏ từ từ Y trên buret vào bình tam giác chứa 6,6 mL dung dịch FeSO4 0,1M trong môi trường H2SO4 dư đến khi kết thúc chuẩn độ thì hết 5,0mL.
(Ở điểm cuối chuẩn độ, chỉ thị diphenylamine chuyển từ không màu sang màu tím).
Tính hàm lượng FeO.Cr2O3 trong quặng.
Đáp án đúng là:
Sơ đồ chuyển hoá các hợp chất chứa chromium:
$\text{FeO}\cdot \text{C}{{\text{r}}_{2}}{{\text{O}}_{3}}\to 2~{{\text{K}}_{2}}\text{Cr}{{\text{O}}_{4}}\to {{\text{K}}_{2}}\text{C}{{\text{r}}_{2}}{{\text{O}}_{7}}\to \text{C}{{\text{r}}_{2}}{{\left( \text{S}{{\text{O}}_{4}} \right)}_{3}}$
=> nFe(CrO2)2
Đáp án cần điền là: 88
Để hòa tan một mẫu zinc trong dung dịch hydrochloric acid ở 20oC cần 27 phút. Cũng mẫu zinc đó tan hết trong dung dịch acid trên ở nhiệt độ 40oC trong 3 phút. Hỏi để tan hết mẫu zinc đó trong dung dịch acid trên ở nhiệt độ 55oC cần thời gian là bao nhiêu phút?
Đáp án đúng là:
Áp dụng công thức: $\dfrac{\text{T}_{1}}{\text{T}_{2}} = \dfrac{v_{\text{t}_{2}}}{v_{\text{t}_{1}}} = \gamma^{\dfrac{\text{t}_{2} - \text{t}_{1}}{10}}$ .
Đáp án cần điền là: 0,58
Hãy giải thích những hiện tượng sau:
a) Bột sắt tan tốt trong acid HCl ở nhiệt độ phòng nhưng thanh sắt tan rất chậm.
b) Ngâm miếng chromium vào dung dịch acid loãng không thấy khí thoát ra, khi dùng HCl đặc và đun nóng thì thấy khí thoát ra.
c) Than đá để trong không khí không bị cháy, khi có mối lửa, phản ứng xảy ra mãnh liệt.
Các yếu tố ảnh hưởng tới tốc độ phản ứng.
a) Hoàn thành các quá trình sau:
(1) Mg $\rightarrow$ Mg2+ + ....?.....e
(2) Cl + .....?....e $\rightarrow$ Cl-
(3) O + .....?.....e $\rightarrow$ O2-
b) Viết công thức phân tử của hợp chất ion tạo bởi các cặp ion sau:
(1) Cation Mg2+ với anion Cl-
(2) Cation Mg2+ với anion O2-.
a) - Trong quá trình hình thành liên kết hoá học, các nguyên tử có xu hướng nhường, nhận hoặc góp chung electron để đạt được cấu hình electron bền vững như của khí hiếm với 8 electron lớp ngoài cùng (hoặc 2 electron ở lớp ngoài cùng như helium).
- Nguyên tử kim loại có xu hướng nhường electron để hình thành ion dương (cation).
- Nguyên tử phi kim có xu hướng nhận electron để hình thành ion âm (anion).
b) Viết công thức phân tử của hợp chất ion tạo bởi các cặp ion.
Cho các phương trình nhiệt hóa học sau:
$\left. \text{CaCO}_{3}\left( \text{s} \right)\rightarrow\text{CaO}\left( \text{s} \right) + \text{CO}_{2}\left( \text{g} \right) \right.$ $\Delta_{\text{r}}\text{H}_{298}^{{^\circ}} = + 178,49\mspace{6mu}\text{kJ}$
$\left. \text{C}_{2}\text{H}_{5}\text{OH}\left( \text{l} \right) + 3\text{O}_{2}\left( \text{g} \right)\rightarrow 2\text{CO}_{2}\left( \text{g} \right) + 3\text{H}_{2}\text{O}\left( \text{l} \right) \right.$ $\Delta_{\text{r}}\text{H}_{298}^{{^\circ}} = - 1370,70\mspace{6mu}\text{kJ}$
$\left. \text{C}\left( {\text{graphite},\text{s}} \right) + \text{O}_{2}\left( \text{g} \right)\rightarrow\text{CO}_{2}\left( \text{g} \right) \right.$ $\Delta_{\text{r}}\text{H}_{298}^{{^\circ}} = - 393,5\mspace{6mu}\text{kJ}$
a) Phản ứng nào có thể tự xảy ra (sau giai đoạn khơi mào ban đầu), phản ứng nào không thể tự xảy ra?
b) Tính khối lượng ethanol hay graphite cần dùng khi đốt cháy hoàn toàn đủ tạo lượng nhiệt cho quá trình nhiệt phân hoàn toàn 15 gam CaCO3. Cho hiệu suất các phản ứng đều là 100%.
a) $\Delta_{\text{r}}\text{H}_{298}^{{^\circ}} > 0$: phản ứng không tự xảy ra được.
$\Delta_{\text{r}}\text{H}_{298}^{{^\circ}} < 0$: phản ứng tự xảy ra được
b) Q = $\Delta_{\text{f}}\text{H}_{298}^{{^\circ}}$. n


