Phân đạm là tên gọi chung của các loại phân bón cung cấp nitrogen cho cây trồng, thúc đẩy quá trình tăng trưởng của cây, làm tăng năng suất cây trồng. Chất nào sau đây dùng làm phân đạm?
Đáp án đúng là: A
Lí thuyết về phân bón hóa học.
Đáp án cần chọn là: A
Có 4 ester no, đơn chức, mạch hở đều có công thức cấu tạo dạng R-COO-C2H5 được kí hiệu ngẫu nhiên là X, Y, Z, T. Độ tan của 4 ester được cho ở bảng sau:
![]()
Trong số 4 ester trên, ester có nhiều nguyên tử carbon nhất trong phân tử là
Đáp án đúng là: A
Lí thuyết về tính chất vật lí của ester.
Đáp án cần chọn là: A
Loại nguồn điện nào sau đây có thể tái sử dụng nhiều lần bằng cách sạc điện?
Đáp án đúng là: D
Lí thuyết về một số loại pin trong thực tiễn.
Đáp án cần chọn là: D
Xà phòng là muối sodium hoặc potassium của
Đáp án đúng là: B
Lí thuyết về tính chất hóa học của chất béo.
Đáp án cần chọn là: B
Kí hiệu nào dưới đây biểu diễn không đúng với cặp oxi hoá – khử?
Đáp án đúng là: B
Cách biểu diễn cặp oix hóa – khử: Dạng oxi hóa/ Dạng khử.
Đáp án cần chọn là: B
Phản ứng xảy ra trong pin Galvani Zn – Cu là: $\left. \text{Zn(s)} + \text{Cu}^{2 +}\text{(aq)}\rightarrow\text{Zn}^{2 +}\text{(aq)} + \text{Cu(s)} \right.$. Quá trình xảy ra tại anode (hay cực âm) của pin là
Đáp án đúng là: A
Trong pin điện hóa, tại anode xảy ra quá trình oxi hóa.
Đáp án cần chọn là: A
Phát biểu nào không đúng về chất béo?
Đáp án đúng là: A
Lí thuyết về chất béo.
Đáp án cần chọn là: A
Curcumin được tách ra từ củ nghệ bằng phương pháp chiết và kết tinh là curcumin thô. Trong curcumin thô có chứa ba loại curcuminoid là curcumin (CUR), demethoxycurcumin (DMC) và bisdemethoxycurcumin (BDMC). Từ curcumin thô có thể tách riêng 3 loại trên bằng phương pháp sắc kí cột với pha tĩnh là silicagel và pha động là hỗn hợp của chloroform và methanol. Sơ đồ tách của ba loại curcuminoid tách ra từ một mẫu được cho dưới đây:
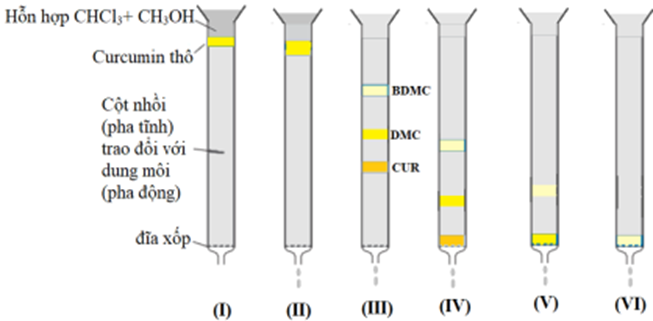
Cho các phát biểu sau:
(1) Thứ tự giảm dần độ hấp phụ bởi pha tĩnh là CUR, DMC, BDMC.
(2) CUR tan kém trong hỗn hợp chloroform và methanol hơn DMC.
(3) Có thể thay hỗn hợp chloroform và methanol bởi hỗn hợp benzene và nước.
(4) Khoảng cách giữa các chất trong cột tỉ lệ thuận với hàm lượng các chất trong mẫu.
Số phát biểu không đúng là
Đáp án đúng là: B
Dựa vào đoạn thông tin trên và sơ đồ tách của ba loại curcuminoid.
Đáp án cần chọn là: B
Nổ bụi là vụ nổ gây ra bởi quá trình bốc cháy nhanh của các hạt bụi mịn phân tán trong không khí bên trong một không gian hạn chế, tạo ra sóng nổ. Nổ bụi xảy ra khi có đủ 5 yếu tố: nguồn oxygen, nguồn nhiệt, nhiên liệu (bụi có thể cháy được), nồng độ bụi mịn đủ lớn và không gian đủ kín. Năm 2007, một vụ nổ bụi xảy ra khi các công nhân hàn bảo trì bể chứa bột mì tại phân xưởng sản xuất bột mì ở tỉnh Bình Dương khiến 5 công nhân bị bỏng nặng.
Cho các phát biểu sau:
(a) Nổ bụi là một vụ nổ vật lí.
(b) Vụ nổ bụi xảy ra khi có đủ các yếu tố: nguồn oxygen, nguồn nhiệt, không gian đủ kín.
(c) Nhiên liệu trong vụ nổ bụi tại phân xưởng bột mì ở Bình Dương là bụi bột mì.
(d) Bụi càng mịn khả năng gây nổ càng cao do phát tán nhanh và dễ lơ lửng trong không khí.
Các phát biểu đúng là
Đáp án đúng là: D
Dựa vào đoạn thông tin tên và lí thuyết về phản ứng nổ bụi.
Đáp án cần chọn là: D
Cho dãy các chất sau: (1) methane, (2) ethylene, (3) polystyrene, (4) ethyl acetate, (5) methylamine. Những hợp chất nào trong dãy là dẫn xuất hydrocarbon?
Đáp án đúng là: A
Dẫn xuất của hydrocarbon là hợp chất chứa một số nguyên tố khác ngoài C và H.
Đáp án cần chọn là: A
Khi đun nóng ester của acetic acid trong dung dịch NaOH xảy ra phản ứng hoá học sau:
$\text{CH}_{3}\text{COOR} + \text{NaOH}\overset{\text{t}^{o}}{\rightarrow}\text{CH}_{3}\text{COONa} + \text{ROH}$ (*)
Cơ chế của phản ứng xảy ra như sau:
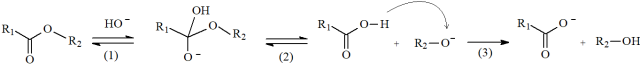
Nhận định nào sau đây không đúng?
Đáp án đúng là: A
(a), (b), (d): Dựa vào cơ chế của phản ứng giữa acetic acid và NaOH.
(c) Theo thuyết Bronsted – Lowry:
+ Chất cho proton là acid.
+ Chất nhận proton là base.
Đáp án cần chọn là: A
Ứng dụng nào sau đây không phải là ứng dụng của glucose?
Đáp án đúng là: C
Lí thuyết về ứng dụng của glucose.
Đáp án cần chọn là: C
Một người thợ sơn cần lựa chọn một dung môi dễ bay hơi và có độ phân cực kém. Người thợ sơn nên chọn chất nào sau đây?
Đáp án đúng là: C
Lí thuyết về tính chất vật lí của nước, alcohol, carboxylic acid và ester.
Đáp án cần chọn là: C
Các amine CH3NH2, CH3NHCH3, CH3CH2NH2 tan nhiều trong nước. Nguyên nhân là do các amine
Đáp án đúng là: C
Lí thuyết về tính chất vật lí của amine.
Đáp án cần chọn là: C
Số nguyên tử carbon trong phân tử valine là
Đáp án đúng là: B
Đặc điểm cấu tạo amino acid.
Đáp án cần chọn là: B
“… (1)… là vật liệu được tổ hợp từ hai hay nhiều vật liệu khác nhau, tạo nên vật liệu mới có tính chất vượt trội so với các vật liệu thành phần. Trong đó vật liệu. …(2)… có vai trò đảm bảo cho các thành phần cốt của composite liên kết với nhau nhằm tạo ra tính nguyên khối và thống nhất”. Nội dung phù hợp trong các ô trống (1), (2) lần lượt là
Đáp án đúng là: B
Lí thuyết về khái niệm vật liệu composite.
Đáp án cần chọn là: B
Chất nào dưới đây không phản ứng với dung dịch NaOH trong điều kiện thích hợp?
Đáp án đúng là: C
Lí thuyết về tính chất hóa học của alcohol, carboxylic acid, phenol và ester.
Đáp án cần chọn là: C
Cho cấu tạo của một đoạn mạch trong phân tử polymer X:
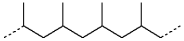
Tên gọi của polymer X là
Đáp án đúng là: A
Lí thuyết về polymer
Đáp án cần chọn là: A
Phức chất [Fe(OH2)6]3+ có cấu tạo như hình bên. Số liên kết cho - nhận mà nguyên tử trung tâm iron tạo được với các phối từ OH2 là
![Phức chất [ F e ( O H 2 ) 6 ] 3 + có cấu tạo như hình bên. Có bao nhiêu liên kết sigma ( σ ) có trong phức chất đó?](https://video.vietjack.com/upload2/quiz_source1/2024/09/blobid5-1727367146.png)
Đáp án đúng là: D
Phân tích công thức của phức chất
- Liên kết hóa học giữa nguyên tử trung tâm M và phối tử L trong phức chất là liên kết cho – nhận, được hình thành nhờ sự cho cặp electron chưa liên kết của phối tử vào orbital trống của nguyên tử trung tâm.
Đáp án cần chọn là: D
Các muối carbonate của kim loại nhóm IIA đều bị phân hủy bởi nhiệt theo phương trình tổng quát sau:
$MC{O_3}(s)\xrightarrow{{}}MO(s) + C{O_2}(g)\,\,\,\,\,\,\,\,{\Delta _r}H_{298}^o$
Biến thiên enthalpy chuẩn của quá trình trên được cho trong bảng sau:
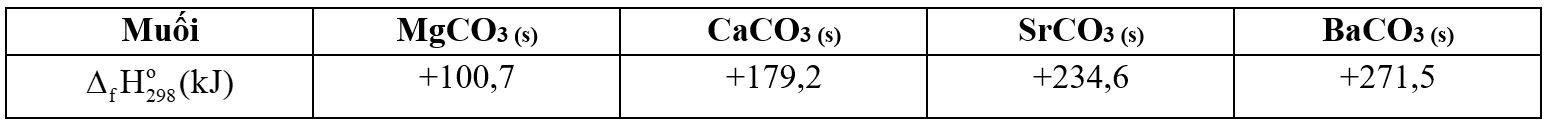
Phát biểu nào dưới đây đúng?
Đáp án đúng là: D
Ý nghía giá trị biến thiên enthalpy của phản ứng.
Đáp án cần chọn là: D
Điều chế ethyl acetate trong phòng thí nghiệm được tiến hành như sau :
Bước 1: Cho khoảng 5 mL ethanol và 5 mL acetic acid tuyệt đối vào ống nghiệm, lắc đều hỗn hợp.
Bước 2: Thêm khoảng 2 mL dung dịch H2SO4 đặc, lắc nhẹ để các chất trộn đều với nhau.
Bước 3: Đặt ống nghiệm vào cốc nước nóng (khoảng 60°C – 70°C) trong khoảng 5 phút, thỉnh thoảng lắc đều hỗn hợp.
Bước 4: Lấy ống nghiệm ra khỏi cốc nước nóng, để nguội hỗn hợp rồi rót sang ống nghiệm khác chứa 10 mL dung dịch muối ăn bão hòa thì thấy chất lỏng trong ống nghiệm tách thành hai lớp, lớp trên có mùi thơm đặc trưng.
Bước 5: Đem đo phổ hồng ngoại (IR) của chất lỏng có mùi thơm đặc trưng.
Cho biết số sóng hấp thụ đặc trưng của một số liên kết trên phổ hồng ngoại như sau :
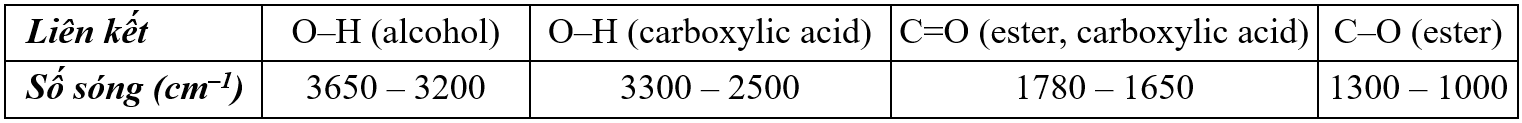
| Đúng | Sai | |
|---|---|---|
| a) Phản ứng xảy ra trong bước 3 theo phương trình:CH3COOH(l) + C2H5OH(l) ⟶ CH3COOC2H5(l) + H2O(l). | ||
| b) Sulfuric acid đặc vừa là chất xúc tác, vừa có tác dụng hút nước, làm tăng hiệu suất tạo ester. | ||
| c) Trên phổ hồng ngoại của chất mùi thơm xuất hiện peak có số sóng 3500 cm-1 chứng tỏ sản phẩm chưa tinh khiết. | ||
| d) Dung dịch NaCl bão hoà làm giảm độ tan của ester trong nước để ester dễ dàng tách lớp nổi lên trên tốt hơn. |
Đáp án đúng là: S; Đ; Đ; Đ
Lí thuyết về phản ứng ester hóa số sóng đặc trưng của các nhóm chức.
Đáp án cần chọn là: S; Đ; Đ; Đ
Chlorine và sodium hydroxide là hoá chất được sử dụng để sản xuất nhiều chất trung gian trong các ngành công nghiệp hoá học (polymer, bột giấy, giấy), dược phẩm, thuốc bảo vệ thực vật, sản xuất xà phòng, luyện kim,…. Công nghệ sử dụng phổ biến để điều chế Cl2 và NaOH là điện phân dung dịch NaCl có màng ngăn. Mô hình thiết bị điện phân được thể hiện trong hình bên.
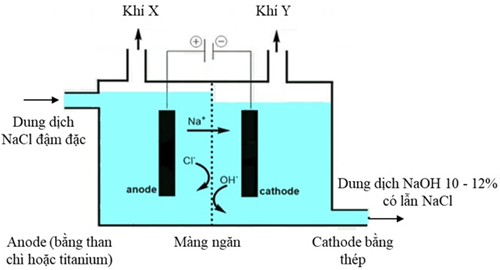
Cathode được làm bằng thép và anode làm bằng than chì hoặc titanium. Dung dịch NaCl được đưa vào từ anode và được duy trì ở mức cao hơn bên cathode giúp chất lỏng chảy từ trái sang phải, ngăn không cho dung dịch NaOH chảy sang ngăn anode. NaCl trong dung dịch sau điện phân được tách khỏi NaOH phần lớn bởi quá trình cô đặc dung dịch.
| Đúng | Sai | |
|---|---|---|
| a) Ở cathode, nước bị khử do thế điện cực chuẩn của cặp $\text{2H}_{2}\text{O/H}_{2} + \text{OH}^{-}$ cao hơn $\text{Na}^{+}/\text{Na}$. | ||
| b) Do độ tan của NaOH lớn hơn NaCl nên khi cô đặc dung dịch, một lượng lớn NaCl sẽ bị kết tinh. | ||
| c) Ở anode, Cl- bị oxi hóa trước do thể điện cực chuẩn của cặp $\text{Cl}_{2}\text{/Cl}^{-}$ nhỏ hơn của $\text{O}_{2}/\text{H}_{2}\text{O}$. | ||
| d) Khí X là chlorine và khí Y là hydrogen. |
Đáp án đúng là: Đ; Đ; S; Đ
Lí thuyết về phản ứng điện phân dung dịch NaCl có màng ngăn.
Đáp án cần chọn là: Đ; Đ; S; Đ
Khi phân tích thành phần của hợp chất hữu cơ X thấy có chứa 62,07% C; 10,34% H còn lại là oxygen. Trên phổ MS của X thấy có peak ion phân tử [M+] có giá trị bằng 58. Trên phổ IR của X thấy xuất hiện peak trong vùng 1670 – 1740 cm-1 đồng thời X không tham gia phản ứng với Cu(OH)2/OH-. Xác định công thức cấu tạo của X.
C : H : O = \(\dfrac{{\% C}}{{12}}:\dfrac{{\% H}}{1}:\dfrac{{\% O}}{{16}}\)
⟶ CTPT: (CTĐGN)n
Peak trong vùng 1670 – 1740 cm-1 ⟶ Có nhóm chức C = O.
Khi làm thí nghiệm với H2SO4 đặc, nóng thường sinh ra khí SO2. Để hạn chế tốt nhất khí SO2 thoát ra gây ô nhiễm môi trường, người ta nút ống nghiệm bằng bông tẩm xút. Hãy viết các phản ứng hoá học giải thích cách làm trên.
Tính chất hoá học của SO2.
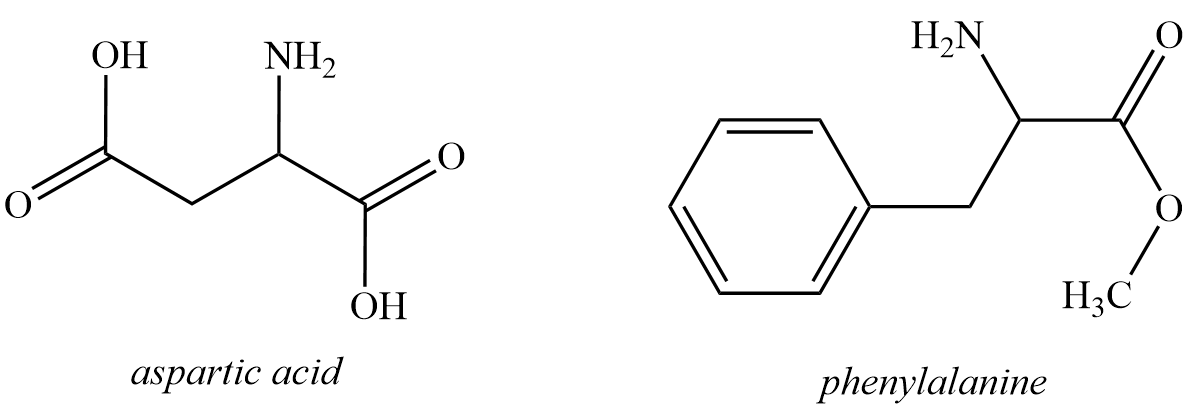
Sự kết hợp giữa aspartic acid và phenylalanine tạo thành peptide, peptide này có thể được chuyển đổi thành methyl ester gọi là aspartame (như hình dưới).
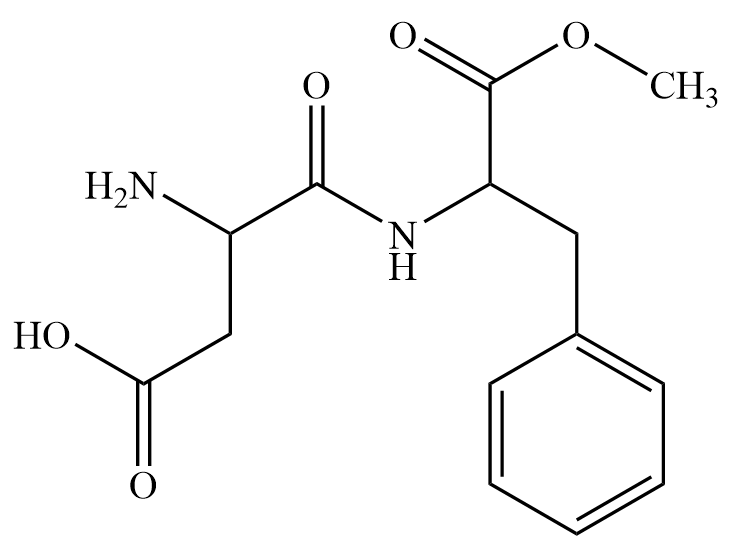
Aspartame có vị ngọt nên được sử dụng trong thực phẩm không đường dành cho người bị tiểu đường. Ở nhiệt độ cao aspartame bị phân hủy tạo các amino acid tự do không có vị ngọt. Viết công thức cấu tạo phù hợp các amino acid aspartic acid và phenylalanine.
Dựa vào công thức cấu tạo của aspartic acid, phenylalanine và aspartame.
Formaldehyde là một hoá chất quan trọng, điều chế bằng phương pháp dehydrogen hoá methanol:
$\text{CH}_{3}\text{OH(g)}\overset{700^{\text{o}}\text{C,xt}}{\rightarrow}\text{HCHO(g)} + \text{H}_{2}(\text{g)}$(1) $\Delta_{\text{r}}\text{H}_{298}^{o}$ = 84,2 kJ
Nhiệt để duy trì phản ứng (1) được lấy từ phản ứng giữa H2 với O2 của không khí theo phản ứng:
$\left. \text{H}_{2}\text{(g)} + \dfrac{1}{2}\text{O}_{2}\text{(g)}\rightarrow\text{H}_{2}\text{O(g)} \right.$ (2) $\Delta_{\text{r}}\text{H}_{298}^{o}$= -241,8 kJ
Tính % thể tích methanol trong hỗn hợp methanol và không khí đưa vào để phản ứng (1) tự duy trì ở 700°C. Biết rằng oxygen chiếm 21% thể tích không khí và phản ứng hết; lượng nhiệt mà nitrogen đã hấp thụ chiếm 35% lượng của phản ứng (2). (Làm tròn kết quả đến hàng phần mười).
Q1 = $\text{n}_{\text{CH}_{3}\text{OH}}.\left| {\Delta_{\text{r}}\text{H}_{298}^{o}(1)} \right|$ = $\text{n}_{\text{CH}_{3}\text{OH}}$.84,2 (kJ)
Q2 = $\text{2n}_{\text{O}_{2}}.\left| {\Delta_{\text{r}}\text{H}_{298}^{o}(2)} \right|$ = $\text{2n}_{\text{O}_{2}}$.241,8 (kJ)
Do N2 hấp thụ 35% nhiệt nên chỉ còn 65% nhiệt của (2) cung cấp cho (1) nên : Q1 = 65%Q2.
Mà O2 chiếm 21% không khí $\rightarrow$$\text{n}_{\text{O}_{2}} = \dfrac{21}{100}$nkhông khí $\left. \rightarrow\dfrac{\text{n}_{\text{CH}_{3}\text{OH}}}{\text{n}_{\text{KK}}} \right.$ $\left. \rightarrow\%\text{V}_{\text{CH}_{3}\text{OH}} \right.$
Hydrogen là nhiên liệu xanh và thân thiện với môi trường nhất, được đánh giá có tiềm năng cung cấp phần lớn năng lượng cho thế giới trong tương lai, thay thế cơ sở hạ tầng năng lượng hiện tại dựa trên nhiên liệu hóa thạch. Hydrogen được kỳ vọng sẽ giải quyết vấn đề thiếu hụt năng lượng trong tương lai gần, đặc biệt là ở các khu vực địa lý phức tạp (đồi núi, cao nguyên khô cằn, v.v.) và khí hậu khắc nghiệt. Hiện nay, việc sản xuất hydrogen công nghiệp chủ yếu thông qua quá trình oxi hóa – khử như reforming CH₄ hoặc điện phân nước. Vì vậy, cần đánh giá lợi ích – rủi ro khi sử dụng H₂.
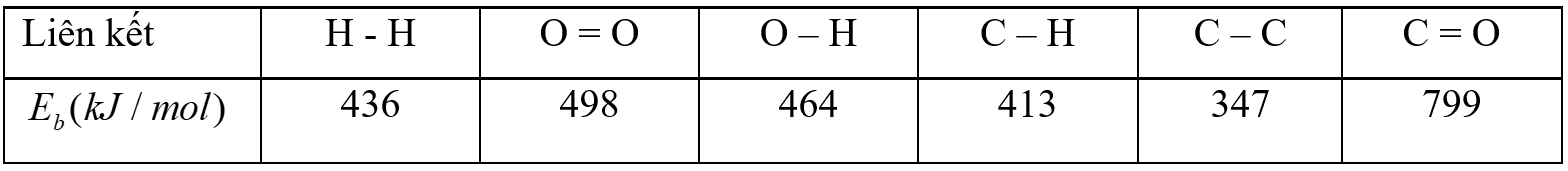
Biết khối lượng riêng xăng (xấp xỉ C₈H₁₈) là 0,703 g·cm⁻³
a) Viết phương trình phản ứng xảy ra đốt cháy hoàn toàn nhiên liệu hydrogen và xăng (thành phần chính (thành phần chính là C8H18).
b) Gọi k là phần trăm năng lượng tỏa ra khi đốt cháy hoàn toàn 1 L khí H₂ (dkc) so với 1 lít xăng. Giá trị của k bằng bao nhiêu? Làm tròn kết quả đến hai chữ số sau dấu phẩy.
c) Tại sao hydrogen được dùng làm nhiên liệu phải được nén ở áp suất cao hoặc hoá lỏng?
a) Viết phương trình phản ứng chảy của H2 và C8H18.
b) Biến thiên enthalpy của phản ứng theo năng lượng liên kết.
$\Delta_{r}H_{298}^{o} = {\sum{E_{b}(cd)}} - {\sum{E_{b}(sp)}}$
Khối lượng riêng: $d = \dfrac{m}{V}$
c) Hoá học và vấn đề môi trường.