Đề thi học kì I môn hóa 11 trường THPT Đa Phúc mã 102 năm 2012-2013
Thời gian thi : 45 phút - Số câu hỏi : 9 câu - Số lượt thi : 2250
Chú ý: Để xem lời giải chi tiết vui lòng chọn "Click vào đề thi"
Một số câu hỏi trong đề thi
Câu 1: Trường THPT Đa Phúc - cơ bản - năm 2012-2013
Mã đề 102
Câu1: Để điều chế HNO3 trong phòng thí nghiệm, các hóa chất cần sử dụng là:
Câu 2: Cho các chất sau: Cu(OH)2, FeCl3, BaCO3, Zn, Au, S. Số chất tác dụng được với dung dịch HNO3 loãng là:
Câu 3: Hấp thụ hết 3,36 lớt khớ CO2 (đktc) vào 200ml dung dịch NaOH 2M. Dung dịch thu được sau phản ứng chứa chất nào sau đây :
Câu 4:
Trộn 200 ml dung dịch chứa hỗn hợp HCl 0,1M và H 2SO4 0,1M với 200 ml dung dịch NaOH 0,1M. Giá trị pH của dung dịch sau phản ứng là:
Câu 5: Chọn những chất điện li yếu trong số các chất sau:
a. KNO3 b. CH3COOH c. HNO3 d. Mg(OH)2 e. H3PO4 f. CuSO4
Câu 6: Chất nào sau đây là nguyên nhân chính gây ra hiệu ứng nhà kính:
Câu 7: Viết các phương trình hóa học của các phản ứng sau (ghi rõ điều kiện phản ứng nếu có): (2,5 đ)
a) Na2SO4 + Ba(NO3)2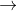
b) Zn(OH)2 + KOH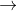
c) C + CO2 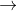
d) Al + HNO3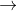 tỉ lệ mol N2: NO = 3:2
tỉ lệ mol N2: NO = 3:2
Câu 8: Trình bày phương pháp hoá học phân biệt các dung dịch đựng trong các lọ mất nhãn riêng biệt sau (Viết các PTHH xảy ra nếu có): (1,5 đ)
K2CO3, NH4NO3, BaCl2, Na2SO4
Câu 9: Hòa tan hoàn toàn 16,6 gam hỗn hợp X gồm Al và Fe vào dung dịch HNO3 lõang vừa đủ. Sau phản ứng thu được dung dịch Y và 8,96 lít khí NO (đktc, là sản phẩm khử duy nhất).
a) Tính % khối lượng mỗi kim loại trong hỗn hợp X. (1,5 đ)
b) Cô cạn dung dịch Y rồi nung đến khối lượng không đổi thu được m gam chất rắn. Tính giá trị của m. (1,0 đ)
c) Trộn ½ lượng hỗn hợp X với bột lưu huỳnh vừa đủ nung nóng đến phản ứng hoàn toàn thu được hỗn hợp Z. Hòa tan hết Z vào dung dịch chứa lượng dư hỗn hợp NaNO3 và HCl. Sau phản ứng thu được V lít khí NO duy nhất. Tính V. (0,5 đ)