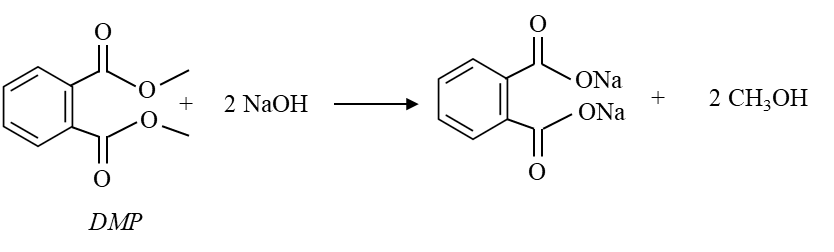
4 ester no, đơn chức, mạch hở kí hiệu ngẫu nhiên lần lượt là X, Y, Z, T. Mỗi ester trên đều tạo bởi các carboxylic acid mạch không phân nhánh và ethyl alcohol. Độ tan của 4 ester như sau:
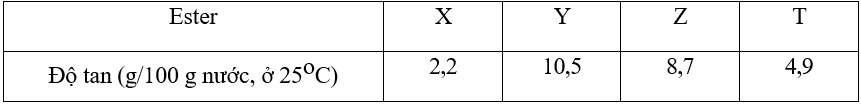
Trong số 4 ester trên, ester nào có nhiều nguyên tử carbon nhất trong phân tử?
Đáp án đúng là: A
Ester có mạch carbon càng lớn thì độ tan càng nhỏ.
Đáp án cần chọn là: A
Trong các chất dưới đây, hợp chất nào thuộc loại arylamine?
Đáp án đúng là: B
Arylamine là những amine có nguyên tử N liên kết trực tiếp với vòng thơm.
Đáp án cần chọn là: B
Iodine phản ứng màu với carbohydrate nào dưới đây?
Đáp án đúng là: D
Tính chất hoá học của tinh bột.
Đáp án cần chọn là: D
Chất nào sau đây là thành phần chính của chất giặt rửa tổng hợp?
Đáp án đúng là: B
Chất giặt rửa tổng hợp là muối sodium của dodeylbenzensulfonic acid.
Đáp án cần chọn là: B
Quặng nào sau đây được dùng làm nguyên liệu chính để tách kim loại sắt trong ngành luyện kim?
Đáp án đúng là: B
Trạng thái tự nhiên của kim loại.
Đáp án cần chọn là: B
Chất X được sử dụng chủ yếu sản xuất phân đạm, làm nhiên liệu tên lửa, được dùng làm chất gây lạnh trong thiết bị lạnh ở dạng lỏng. Chất X là chất nào sau đây?
Đáp án đúng là: B
Ứng dụng của ammonia.
Đáp án cần chọn là: B
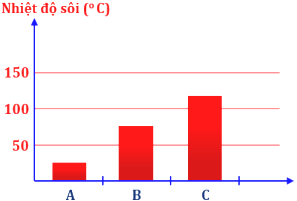
Ba chất A, B, C có nhiệt độ sôi được biểu thị như hình sau: Các chất A, B, C lần lượt là
Đáp án đúng là: B
Tính chất vật lí của các chất.
Các chất có khả năng tạo liên kết hydrogen liên phân tử sẽ có nhiệt độ sôi cao hơn hợp chất không có khả năng tạo liên kết hydrogen.
Đáp án cần chọn là: B
Muối carbonate nào sau đây khó bị nhiệt phân huỷ nhất?
Đáp án đúng là: C
Năng lượng của phản ứng hoá học.
Giá trị enthalpy càng lớn, phản ứng càng cần cung nhiều nhiệt.
Đáp án cần chọn là: C
Trong quá trình điện phân KBr nóng chảy, dương cực (anode) xảy ra quá trình
Đáp án đúng là: C
Quá trình xảy ra trong bình điện phân:
+) Cathode (-): xảy ra quá trình khử
+) Anode (+): xảy ra quá trình oxi hoá
Đáp án cần chọn là: C
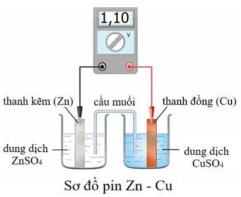
Cho pin Galvani Zn – Cu có cấu tạo như hình sau, ở 25 oC. Đóng kín mạch bằng cầu muối chứa dung dịch bão hoà KNO3. (Biết $E_{Zn^{2 +}/Zn}^{0}$ = - 0, 76 V). Chọn phát biểu đúng?
Đáp án đúng là: B
Các quá trình xảy ra trong pin điện:
+) Cathode (+): xảy ra quá trình khử
+) Anode (-): xảy ra quá trình oxi hoá
Sức điện động của pin: $E_{pin}^{o} = E_{cathode}^{o} - E_{anode}^{o}$
Đáp án cần chọn là: B
Cho phản ứng hoá học: (CH3)3CBr + NaOH xảy ra theo cơ chế gồm hai giai đoạn:
(CH3)3CBr + NaOH $\xrightarrow{{{t^0}}}$ (CH3)3 C-OH + NaBr (*)
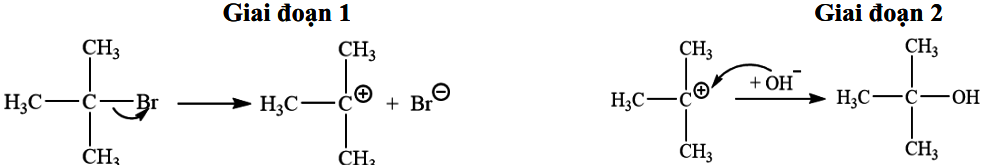
Nhận định nào sau đây đúng?
Đáp án đúng là: B
Cơ chế phản ứng hoá học.
Đáp án cần chọn là: B
Một số loại sắn có chứa cyanhydric acid (HCN), đây là một chất gây độc cho người. Cách đơn giản để chuyển hóa HCN thành một chất khác không độc, là cho HCN kết hợp nhóm carbonyl (C=O) để chuyển thành hợp chất chứa nhóm -C(OH)CN. Loại thực phẩm nào sau đây có thể cung cấp nhóm carbonyl để giải độc nhanh nhất cho người ngộ độc?
Đáp án đúng là: B
Trạng thái tự nhiên, tính chất hoá học của một số hợp chất aldehyde.
Đáp án cần chọn là: B
Cho khối lượng riêng của các chất:
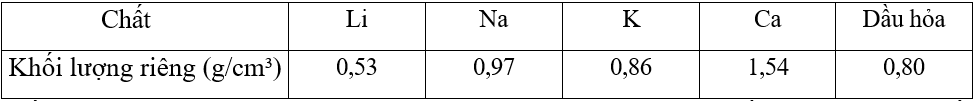
Để bảo quản một số kim loại mạnh, người ta ngâm chìm các kim loại đó vào trong dầu hỏa. Hãy cho biết kim loại nào không bảo quản được bằng cách cho vào dầu hỏa?
Đáp án đúng là: D
Tính chất vật lí của kim loại kiềm.
Chất/hợp chất nào có khối lượng riêng nhỏ hơn sẽ nổi lên trên chất có khối lượng riêng lớn.
Đáp án cần chọn là: D
Charles Goodyear khám phá ra phương pháp kết hợp giữa nguyên tố sulfur (S) với cao su thiên nhiên để tạo ra một loại cao su có cấu trúc dạng mạch không gian, làm tăng cao tính bền cơ học, khả năng chịu được sự ma sát, va chạm. Loại cao su này có tên là
Đáp án đúng là: C
Lí thuyết về cao su.
Đáp án cần chọn là: C
Cấu hình electron nào sau đây là của kim loại chuyển tiếp dãy thứ nhất?
Đáp án đúng là: C
Đặc điểm của kim loại chuyển tiếp dãy thứ nhất.
Đáp án cần chọn là: C
Cho các cặp oxi hóa – khử và thế điện cực chuẩn tương ứng:

Khi điện phân dung dịch chứa đồng thời bốn loại cation ở trên với nồng độ mol bằng nhau, cation đầu tiên bị điện phân đầu tiên ở cathode là
Đáp án đúng là: D
Ion có tính oxi hoá mạnh hơn thì sẽ bị điện phân trước ở cathode.
Đáp án cần chọn là: D
Kim loại tungsten (W) được dùng làm dây tóc trong bóng đèn chủ yếu nhờ vào đặc điểm nào sau đây?
Đáp án đúng là: A
Tính chất vật lí chung của kim loại.
Đáp án cần chọn là: A
Cho một số thông tin về chất lỏng hexane (C6H14):

Điểm chớp cháy là nhiệt độ thấp nhất mà một chất lỏng hoặc vật liệu dễ bay hơi tạo thành lượng hơi đủ để bốc cháy trong không khí khi tiếp xúc nguồn lửa. Chất lỏng có điểm chớp cháy nhỏ hơn 37,8°C là chất lỏng dễ cháy. Nhiệt độ tự bốc cháy là nhiệt độ mà tại đó chất cháy tự bốc cháy mà không cần nguồn lửa. Nhiệt độ ngọn lửa là nhiệt độ cao nhất có thể tạo ra bởi chất cháy. Áp suất đều bằng áp suất khí quyển.
Cho các phát biểu dưới đây (ở áp suất khí quyển):
(a) Hexane là chất lỏng dễ cháy.
(b) Ở 100oC, hexane tự bốc cháy mà không cần nguồn lửa.
(c) Có thể dùng hexane để nấu chảy chì (lead, nhiệt độ nóng chảy là 328oC).
(d) Khi xảy ra đám cháy với lượng lớn hexane không thể dùng nước để dập tắt đám cháy.
Trong các phát biểu trên, có bao nhiêu phát biểu đúng?
Đáp án đúng là: D
Phân tích dữ liệu đoạn văn.
Đáp án cần chọn là: D
Trong cơ thể người, ion Mg2+ (Z = 12) tham gia cấu trúc tế bào, tổng hợp protein và tổng hợp chất sinh năng lượng ATP. Tổng số hạt proton và electron của ion Mg2+ là
Đáp án đúng là: A
Điện tích hạt nhân (Z) = Số proton.
Ion Mg2+ có số electron = số proton - 2
Đáp án cần chọn là: A
Cho các cặp oxi hoá - khừ và thế điện cực chuẩn tương ứng:
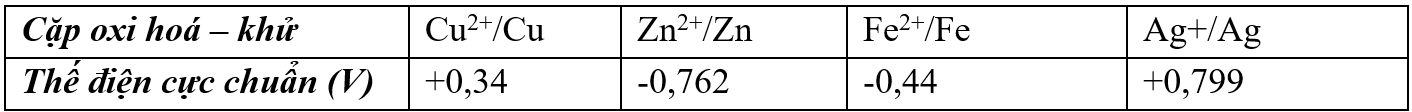
Pin có sức điện động chuẩn lớn nhất là
Đáp án đúng là: A
$\text{E}_{\text{pin}}^{o} = \text{E}_{\text{cathode}}^{o} - \text{E}_{\text{anode}}^{o}$
Đáp án cần chọn là: A
Mỗi năm, lượng dầu ăn phế thải từ các nhà hàng, quán ăn thải ra môi trường gây ô nhiễm, làm lãng phí tài nguyên. Xuất phát từ thực trạng đó, một nhóm nghiên cứu khoa học đã sử dụng dầu ăn thải để tổng hợp nhiên liệu sinh học biodiesel. Biodiesel được sản xuất thông qua phản ứng giữa chất béo và các alcohol mạch ngắn (thường là methanol – CH3OH) với xúc tác kiềm (thường dùng NaOH), thu được biodiesel (dạng methyl ester) và glycerol.
Phản ứng tổng quát như sau:
${(RCOO)_3}{C_3}{H_5} + 3C{H_3}OH\xrightarrow{{NaOH}}3RCOOC{H_3} + {C_3}{H_5}{(OH)_3}$
Nhóm học sinh đưa ra giả thuyết: “Xúc tác NaOH không gây phản ứng phụ trong quá trình sản xuất biodiesel, do đó dùng lượng xúc tác càng nhiều sẽ cho hiệu suất thu hồi biodiesel càng cao.”
Để kiểm chứng, nhóm này tiến hành phản ứng ở cùng điều kiện nhiệt độ và cố định tỷ lệ mol dầu: methanol, chỉ thay đổi lượng xúc tác NaOH (0,5 g → 2,5 g). Kết quả được ghi lại như sau:

Chọn các phát biểu đúng.
Đáp án đúng là: A; B
1. Tính chất hoá học của chất béo.
2., 3. Phân tích kết quả trong bảng.
4. Bảo toàn khối lượng.
Đáp án cần chọn là: A; B
Một nhóm học sinh tiến hành thí nghiệm mạ đồng (copper) lên chiếc chìa khoá. Giả thuyết được nhóm học sinh này đưa ra là: “Nồng độ của dung dịch CuSO4 trước và sau quá trình mạ là không đổi”.
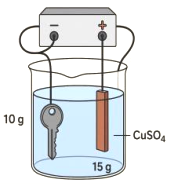
Để kiểm chứng giả thuyết, nhóm học sinh tiến hành các bước như sau:
Bước 1: Cân để xác định khối lượng ban đầu của chiếc chìa khoá là 10 gam và của thanh đồng nguyên chất là 15 gam.
Bước 2: Nối chiếc chìa khoá với 1 điện cực và thanh đồng với điện cực còn lại của nguồn điện một chiều rồi nhúng vào cốc chứa dung dịch CuSO4 để tiến hành mạ với hiệu điện thế thích hợp (như hình vẽ):
Bước 3: Sau thời gian 15 phút điện phân, lấy chiếc chìa khoá và thanh đồng ra khỏi cốc, làm khô cẩn thận, đem cân thì thấy khối lượng của chiếc chìa khoá là 10,32 gam, của thanh đồng là 14,68 gam. Biết hiệu suất của quá trình đạt 100%.
Chọn các phát biểu đúng.
Đáp án đúng là: B; D
1. Mạ điện.
2. Lí thuyết về điện phân.
3., 4. Tính toán theo dữ liệu đề bài cho.
Đáp án cần chọn là: B; D
Các phát biểu nào sau đây về vật liệu composite là đúng?
Đáp án đúng là: A; B; C
Đặc điểm cấu tạo của vật liệu composite.
Đáp án cần chọn là: A; B; C
Một thí nghiệm được thực hiện bằng các hoá chất phổ thông để xác định thành phần của một dung dịch X không màu. Biết rằng X có thể là glucose hoặc fructose. Các cách làm nào sau đây không giúp xác định được chất X?
Đáp án đúng là: B; C; D; E
Phương pháp phân biệt glucose và fructose.
1. Các nhóm chức làm mất màu nước bromine: liên kết π (C=C, C≡C), phenol, aniline, aldehyde.
2. Các nhóm chức tác dụng với thuốc thử Tollens tạo kết tủa bạc: aldehyde.
3. Các nhóm chức tác dụng Cu(OH)2/to tạo kết tủa đỏ gạch: aldehyde.
4. Các nhóm chức tác dụng Cu(OH)2/OH- tạo dung dịch xanh lam: polyalcohol.
5. Quỳ tím chuyển đỏ: carboxylic acid.
Đáp án cần chọn là: B; C; D; E
Một học sinh thực hiện chuỗi thí nghiệm nhằm khảo sát tính chất hoá học của một số amine, gồm:
Thí nghiệm 1: Nhỏ vài giọt dung dịch methylamine 5% vào giấy quỳ tím ẩm.
Thí nghiệm 2: Nhỏ vài giọt dung dịch phenolphthalein vào ống nghiệm chứa methylamine 5%, sau đó cho dung dịch HCl 5% đến dư vào ống nghiệm.
Thí nghiệm 3: Nhỏ vài giọt dung dịch FeCl3 3% vào dung dịch methylamine.
Thí nghiệm 4: Nhỏ từ từ đến dư dung dịch methylamine 5% vào dung dịch CuSO4 1%, lắc nhẹ.
Thí nghiệm 5: Nhỏ vài giọt dung dịch nước bromine vào dung dịch methylamine.
Thí nghiệm 6: Nhỏ vài giọt dung dịch nước bromine vào dung dịch aniline.
Các phát biểu nào sau đây là đúng?
Đáp án đúng là: A; D
1, 2 tính base của amine.
3. Tính chất hoá học riêng biệt của aniline.
4. Phenolphthalein chuyển hồng trong dung dịch có môi trường base.
5. Điều kiện xảy ra phản ứng thế hydrogen trong vòng benzene của aniline.
Đáp án cần chọn là: A; D
RGD là một peptide được tổng hợp từ các amino acid: Asp (phân tử có 1 nhóm –NH2 và 2 nhóm –COOH), Arg và amino acid X. Hình dưới đây minh họa cấu trúc của phân tử RGD:
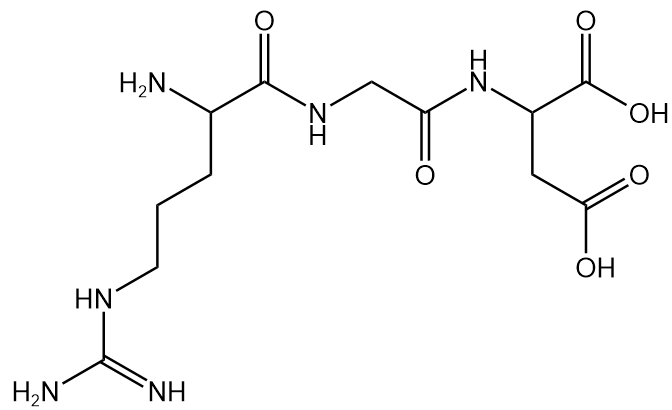
Trả lời cho các câu 26, 27 dưới đây:
Phát biểu nào sau đây không đúng về cấu tạo của RGD?
Đáp án đúng là: C
Quan sát cấu trúc của RGD.
Đáp án cần chọn là: C
Trong các phát biểu sau đây, có bao nhiêu phát biểu đúng khi nói về tính chất hoá học của RGD?
(a) RGD có thể bị thủy phân tạo thành ba amino acid riêng biệt.
(b) Khi thuỷ phân không hoàn toàn X, trong các dipeptide thu được có Arg – Asp.
(c) RGD có phản ứng với dung dịch NaOH.
(d) RGD có khả năng hoà tan Cu(OH)2 trong môi trường kiềm.
Đáp án đúng là: C
Dựa vào tính chất hoá học của RGD.
Đáp án cần chọn là: C
Dimethyl phthalate (DMP) là một chất thường được sử dụng làm chất hóa dẻo trong nhựa và có thể xuất hiện trong bao bì thực phẩm, mĩ phẩm hoặc thuốc trừ sâu. Công thức cấu tạo của DMP như sau:
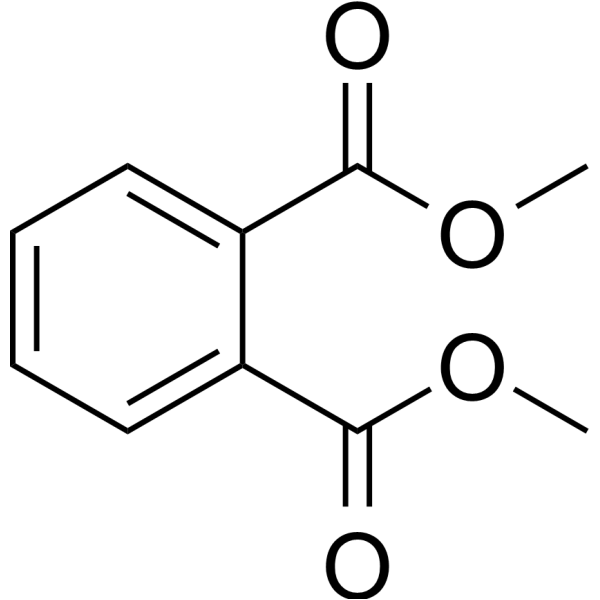
Để xác định hàm lượng DMP trong mẫu chất rắn (chứa DMP và các thành phần không phản ứng), một thí nghiệm được tiến hành như sau:
Bước 1: Cân khối lượng mẫu rắn, kết quả thu được là 0,9700 gam.
Bước 2: Đun hồi lưu với 50,00 mL dung dịch NaOH 0,1000 M.
Bước 3: Sau khi phản ứng xảy ra hoàn toàn, lượng NaOH dư được chuẩn độ bằng dung dịch HCl 0,1000 M. Lượng HCl sử dụng là 36,80 mL.
Bước 4: Tính toán để xác định phần trăm khối lượng của DMP trong mẫu ban đầu.
Trả lời cho các câu 28, 29, 30 dưới đây:
Phát biểu nào sau đây về DMP là đúng?
Đáp án đúng là: C
Hợp chất hữu cơ đa chức là có nhiều 1 loại nhóm chức trong phân tử.
Xác định công thức phân tử từ công thức cấu tạo đơn giản nhất.
Đáp án cần chọn là: C
Sau bước 2, muối được tạo thành có công thức phân tử là
Đáp án đúng là: A
Từ công thức cấu tạo ester ⟶ Công thức cấu tạo muối ⟶ Công thức phân tử muối.
Đáp án cần chọn là: A
Cho các phát biểu sau đây:
(a) Thí nghiệm này có thể được thực hiện với dung dịch HCl ở bước 2 và chuẩn độ bằng dung dịch NaOH ở bước 3.
(b) Thí nghiệm này có thể thực hiện ở nhiệt độ phòng, không cần gia nhiệt.
(c) Kết thúc bước 2, nếu dùng giấy quỳ tím để thử dung dịch trong bình, quỳ tím chuyển sang màu xanh.
(d) Nếu thực hiện bước 2 không đủ lâu, kết quả phần trăm khối lượng DMP sẽ cao hơn thực tế.
(e) Theo kết quả thí nghiệm, phần trăm khối lượng của DMP trong mẫu ban đầu là 26,1%.
Số phát biểu đúng là
Đáp án đúng là: A
Phản ứng thuỷ phân ester trong môi trường kiềm
Mol NaOH phản ứng với DMP = Tổng NaOH ban đầu – NaOH phản ứng với HCl
Đáp án cần chọn là: A
Methyl 4-hydroxybenzoate là ester được sử dụng làm chất bảo quản thực phẩm hoặc mĩ phẩm để ngăn chặn sự phát triển của nấm mốc, vi khuẩn có hại. Thuỷ phân methyl 4-hydroxybenzoate trong môi trường acid thu được chất hữu cơ X và một alcohol. Phân tử khối của X bằng bao nhiêu?
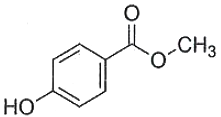
Đáp án đúng là: 138
Tính chất hoá học của ester.
Đáp án cần điền là: 138
Cho các hiện tượng sau:
(1) Bức tượng bằng đồng chuyển sang màu xanh (CuCO3.Cu(OH)2) khi để lâu ngoài không khí.
(2) Giấy "bạc" được sản xuất bằng cách cho các thỏi nhôm chuyển thành dạng lỏng ở nhiệt độ cao sau đó đổ vào khuôn tạo thành phôi nhôm rồi đưa qua máy cán mỏng.
(3) Cánh cửa bằng thép lâu ngày chuyển từ màu xám thành màu nâu.
(4) Miếng Ag sử dụng khi đánh cảm chuyển từ màu sáng sang màu đen.
(5) Khi mài dao trên đá mài thì tại chỗ mài chuyển từ màu tối sang màu sáng.
Liệt kê các phát biểu đúng tương ứng với quá trình ăn mòn kim loại theo kí hiệu số tăng dần.
Đáp án đúng là: 134
Lí thuyết về ăn mòn kim loại.
Đáp án cần điền là: 134
Một nghiên cứu phân tích hàm lượng glutamic acid có trong mẫu nước mắm được thực hiện bởi phương pháp sắc ký lỏng hiệu năng cao (HPLC) với độ nhạy cao, độ chính xác tốt.
Bước 1: Xây dựng đường tuyến tính từ các mẫu chuẩn giữa y (là diện tích peak trên phổ HPLC (đơn vị mAU*min)) và x (là nồng độ glutamic acid (đơn vị mg/L)) được kết quả như sau: y = 0,029x + 0,0202.
Bước 2: Cân chính xác 0,4329 gam một mẫu nước mắm hòa tan trong các dung môi thích hợp trong 24h, lọc loại bã thu được 10 mL dung dịch gốc.
Bước 3: Lấy 0,05 mL dung dịch gốc này, thêm nước cất để pha loãng thành 1 mL dung dịch phân tích rồi tiến hành đo HPLC. Ghi nhận được giá trị diện tích peak ứng với glutamic acid là 0,8467 mAU*min.
Xác định thành phần % về khối lượng của glutamic acid trong mẫu nước mắm trên. (đơn vị %, làm tròn đến hàng phần trăm)
Đáp án đúng là: 1,32
Phân tích dữ liệu đề bài.
Đối với 0,05 mL dung dịch gốc thì 0,8467 = 0,029x + 0,0202 ⟹ x
⟹ Nồng độ glutamic acid trong mẫu dung dịch
Đáp án cần điền là: 1,32
Trong một nhà máy hoá chất, vôi sống (CaO) được sản xuất bằng cách nung đá vôi (CaCO₃) theo phương trình hoá học (1) như sau: CaCO3(s) ⟶ CaO(s) + CO2(g) (1)
Lượng nhiệt phản ứng (1) được cung cấp từ quá trình đốt cháy hoàn toàn carbon trong lò nung theo phương trình hoá học (2): C(graphite) + O2(g) ⟶ CO2(g) (2)
Hiệu suất chuyển hóa CaCO3 thành CaO đạt 100%.
Than dùng làm nhiên liệu chứa 80% C (graphite) về khối lượng, phần còn lại là tạp chất.
Chỉ 50% nhiệt lượng sinh ra từ phản ứng (2) được sử dụng cho phản ứng (1).
Giá trị nhiệt tạo thành ($\Delta_{f}H_{298}^{0}$ ) của các chất ở điều kiện chuẩn được cho trong bảng sau:
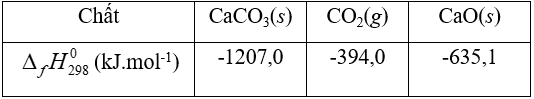
Tính khối lượng than (theo kg, làm tròn đến hàng đơn vị) cần thiết để sản xuất 2000 kg vôi sống theo phương pháp trên.
Đáp án đúng là: 484
Năng lượng của phản ứng hoá học.
$\Delta_{r}H_{298}^{o} = {\sum{\Delta_{f}H_{298}^{o}(sp)}} - {\sum{\Delta_{f}H_{298}^{o}(cd)}}$
⟹ Lượng nhiệt cần cung cấp cho phản ứng (1)
⟹ Lượng nhiệt sinh ra phản ứng (2)
Số mol C tham gia phản ứng
⟹ Khối lượng than cần dùng
Đáp án cần điền là: 484
Trong một nghiên cứu phân tích thành phần hợp kim từ huy chương đồng của Thế vận hội London 2012, người ta đã thực hiện quy trình định lượng như sau:
Hòa tan 0,800 g mẫu huy chương đồng vào dung dịch nitric acid (HNO3) đậm đặc, nóng.
Sau khi làm nguội và pha loãng, thêm một lượng dư dung dịch potassium iodide vào rồi tiếp tục pha loãng dung dịch đến 250,0 mL.
Biết 25,00 mL mẫu dung dịch này phản ứng vừa đủ với 12,20 mL dung dịch sodium thiosulfate 0,100 Μ.
Cho các phương trình xảy ra như sau: 2Cu2+ (aq) + 4I- (aq) → 2CuI(s) + I2(aq)
I2(aq) + 2S2O32-(aq) ⟶ 2I-(aq) + S4O62-(aq)
Biết rằng các huy chương Đồng được làm bằng hợp kim chứa copper. Tính % khối lượng copper (Cu) trong chiếc huy chương trên. (Kết quả làm tròn đến hàng phần mười)
Đáp án đúng là: 97,6
I2(aq) + 2S2O32-(aq) ⟶ 2I-(aq) + S4O62-(aq)
nI2 = ½ nS2O32-
⟹ %Cu
Đáp án cần điền là: 97,6
Việc sản xuất tơ visco có đặc điểm thấm mồ hôi tốt, rất thoáng khí. Do đó, chúng được ứng dụng rất nhiều trong ngành công nghiệp dệt may, thời trang. Quy trình chế tạo tơ visco từ cellulose được mô tả khái quát bằng các bước như sau:
(1) Xay thật nhuyễn cellulose, thường là bông.
(2) Lọc bỏ tạp chất rồi dùng con lăn ép chặt nhằm loại bỏ triệt để các chất dư thừa.
(3) Cho cellulose xay nhuyễn vào trong dung dịch sodium hydroxide để loại bỏ các tạp chất.
(4) Tạo sợi visco bằng cách ép tạo sợi và định hình sợi trong dung dịch sulfuric acid một thời gian rồi rửa sạch.
(5) Khuấy cellulose ở trên trong dung dịch carbon disulfide được hoà tan cùng sodium hydroxide. Quá trình này kết thúc sẽ thu được thành phẩm chính là visco. Sau đó vẫn tiếp tục và ngâm chúng trong vài giờ tiếp theo.
Liệt kê các bước lần lượt theo thứ tự phù hợp với quy trình sản xuất tơ visco.
Đáp án đúng là: 13254
Quy trình sản xuất polymer bán tổng hợp.
Đáp án cần điền là: 13254
Trong máu người trưởng thành, khỏe mạnh vào lúc đói (8 giờ sau ăn) có lượng đường huyết trong khoảng 4,4 – 7,2 mmol/L (theo quyết định số 5481/QĐ-BYT ngày 30 tháng 12 năm 2020 của Bộ Y tế). Kết quả xét nghiệm đường huyết của anh X vào buổi sáng (chưa ăn) là 168 mg/dL (biết 1L= 10dL). Tính lượng đường huyết trong mẫu xét nghiệm của anh X theo đơn vị mmol/L? (Kết quả làm tròn đến hàng phần mười).
Đáp án đúng là: 9,3
Lượng đường huyết trong mẫu xét nghiệm của anh X theo đơn vị mmol/L = $\dfrac{V}{m}$(mmol/L)
Đáp án cần điền là: 9,3
Cho dãy các carbohydrate sau: glucose, saccharose, cellulose, tinh bột và fructose. Có bao nhiêu carbohyrate trong dãy trên phản ứng được với Cu(OH)2 trong môi trường kiềm ở nhiệt độ thường tạo thành dung dịch có màu xanh lam?
Đáp án đúng là: 3
Lí thuyết về tính chất hóa học của các hợp chất carbohydrate.
Đáp án cần điền là: 3
Epibatidine, một lọai dầu không màu được phân lập từ da của loài ếch mũi tên độc Equadorian Epipedobates ba màu. Đây là hợp chất có tác dưng giảm đau gấp vài lần morphine, nhung lại không gây nghiện. Cấu trúc hóa học của epibatidine mô tả như hình dưới:
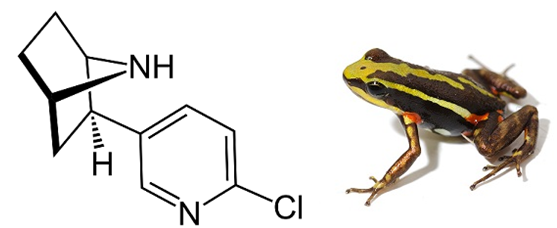
Có bao nhiêu nguyên tử hydrogen trong một phân tử epibatidine?
Đáp án đúng là: 13
Dựa vào công thức cấu tạo của epibatidine.
Đáp án cần điền là: 13
Nhiều enzyme tham gia có chọn lọc với các liên kết peptide nhất định. Chẳng hạn trypsin là một enzyme tiêu hóa xúc tác quá trình thủy phân liên kết peptide ở phía carboxyl của các amino acid arginine (Arg) và lysine (Lys). Thủy phân peptide sau: Ala−Phe−Lys−Val−Met−Tyr−Gly−Arg−Ser−Trp−Leu−His bằng enzyme trypsin thu được tối đa bao nhiêu peptide có mạch ngắn hơn?
Đáp án đúng là: 5
Lí thuyết về phản ứng thủy phân peptide.
Đáp án cần điền là: 5