
Trong khái niệm về liên kết kim loại: "Liên kết kim loại là liên kết hình thành do lực hút tĩnh điện giữa các electron hoá trị ...(1)... với ...(2)... kim loại ở các nút mạng".
Các từ cần điền vào vị trí (1), (2) lần lượt là
Đáp án đúng là: C
Dựa vào khái niệm về liên kết hoá học.
Đáp án cần chọn là: C
Khi có tia lửa điện trong các cơn mưa, trong không khí nitrogen sẽ tác dụng được với oxygen tạo khí X. Khí X sẽ chuyển hóa thành nitrate, cung cấp một lượng phân đạm cho cây trồng. Khí X là hóa chất nào sau đây?
Đáp án đúng là: A
Dựa vào lí thuyết về nitrogen.
Đáp án cần chọn là: A
Ester methyl methacrylate là nguyên liệu để tổng hợp poly(methyl methacrylate), polymer được sử dụng để chế tạo thuỷ tinh hữu cơ plexiglas. Công thức của methyl methacrylate là
Đáp án đúng là: D
Lí thuyết về danh pháp, ứng dụng của ester.
Đáp án cần chọn là: D
Trong quá trình sản xuất bia, enzyme amylase tham gia vào quá trình thủy phân tinh bột thành maltose. Nhận định nào sau đây đúng?
Đáp án đúng là: C
Lí thuyết về maltose và tinh bột.
Đáp án cần chọn là: C
Cho biết: $E_{Al^{3 +}/Al}^{o} = - 1,676V;E_{Zn^{2 +}/Zn}^{o} = - 0,763V;E_{Pb^{2 +}/Pb}^{o} = - 0,126V;E_{Cu^{2 +}/Cu}^{o} = + 0,340V$ . Trong các pin điện hoá sau pin nào có sức điện động chuẩn lớn nhất?
Đáp án đúng là: B
Sức điện động của pin điện: $E_{pin}^{o} = E_{X^{n +}/X}^{o} - E_{Y^{m +}/Y}^{o} > 0$
Sự chênh lệch thế điện cực chuẩn càng lớn, giá trị sức điện động của pin càng nhiều.
Đáp án cần chọn là: B
Phản ứng đơn giản là những phản ứng xảy ra một giai đoạn duy nhất. Cho phương trình hoá học của phản ứng đơn giản: CHCl3(g) + Cl2(g) ⟶ CCl4(g) + HCl(g). Khi nồng độ của CHCl3 giảm 4 lần, nồng độ Cl2 giữ nguyên thì tốc độ phản ứng sẽ
Đáp án đúng là: D
Biểu thức định luật tác dụng khối lượng. (Áp dụng cho phản ứng đơn giản)
Đáp án cần chọn là: D
Các gốc $\alpha$-glucose trong phân tử tinh bột tạo dạng mạch amylose không nhánh liên kết với nhau bởi liên kết
Đáp án đúng là: A
Cấu tạo của tinh bột.
Đáp án cần chọn là: A
Tỉ lệ phần trăm số nguyên tử các đồng vị tự nhiên của chlorine (Cl) được xác định theo phổ khối lượng sau:
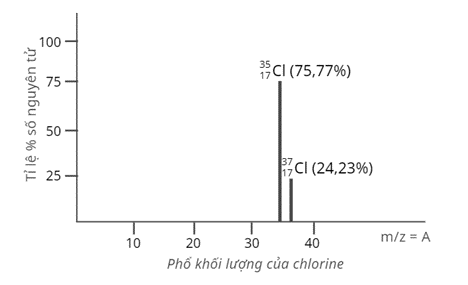
Nguyên tử khối trung bình của Cl là
Đáp án đúng là: B
\(\overline A = \dfrac{{{x_1}\% .{A_1} + {x_2}\% .{A_2}}}{{100\% }}\)
Đáp án cần chọn là: B
Đối với một hệ ở trạng thái cân bằng, nếu thêm chất xúc tác thì
Đáp án đúng là: C
Dựa vào ảnh hưởng của xúc tác tới tốc độ phản ứng và chuyển dịch cân bằng.
Đáp án cần chọn là: C
Điện phân NaCl nóng chảy, ở anode xảy ra quá trình
Đáp án đúng là: C
Cách quá trình xảy ra trong bình điện phân :
Anode : xảy ra quá trình oxi hóa
Cathode : xảy ra quá trình khử
Đáp án cần chọn là: C
Trên một số vật dụng làm từ chất dẻo polypropylene (PP) có ký hiệu 3 mũi tên tạo thành tam giác, kí hiệu này giúp người sử dụng và thu gom vật liệu polymer biết được thông tin gì?

Đáp án đúng là: D
Ý nghĩa kí hiệu chất dẻo.
Đáp án cần chọn là: D
Nước và rượu dễ dàng được tách ra khỏi hỗn hợp rượu và nước bằng cách chưng cất vì chúng có
Đáp án đúng là: C
Dựa vào lý thuyết về phương pháp chưng cất.
Đáp án cần chọn là: C
Glutamic acid có các dạng tồn tại và giá trị pH mà dạng tồn tại đó là chủ yếu (≈ 100 %) như sau:
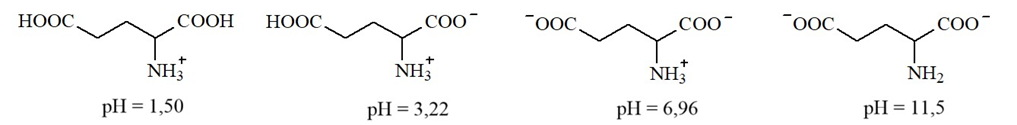
Phát biểu nào sau đây đúng khi nói về quá trình điện li của glutamic acid?
Đáp án đúng là: A
Lí thuyết về tính điện di của amino acid.
Đáp án cần chọn là: A
Một mẫu nước có chứa các muối tan: MgCl2 và Ca(HCO3)2. Mẫu nước này được gọi là
Đáp án đúng là: D
Phân loại nước cứng.
Đáp án cần chọn là: D
Formaldehyde không có ứng dụng nào dưới đây?
Đáp án đúng là: A
Một số ứng dụng formaldehyde.
Đáp án cần chọn là: A
Để lợp nhà, các tấm tôn (thép mỏng mạ zinc) được gắn với nhau bởi các đinh thép. Theo thời gian, các tấm tôn bị ăn mòn. Nhận định nào sau đây là đúng?
Đáp án đúng là: A
Lý thuyết về sự ăn mòn hóa học.
Đáp án cần chọn là: A
Cyanide (CN-) là một loại chất độc hại được tìm thấy trong nước thải của các công ty khai thác quặng kim loại. Cyanide có khả năng tạo phức mạnh với kim loại, các công ty khai thác mỏ đã kiếm được lợi nhuận khổng lồ từ việc sử dụng cyanide để chiết xuất Au từ quặng của nó. Theo tiêu chuẩn Việt Nam, hàm lượng cyanide trong nước thải của các nhà máy phải xử lí trong khoảng 0,05-0,2 mg/lít trước khi thải ra môi trường.
Hàm lượng ion cyanide có thể xác định bằng phương pháp chuẩn độ Liebig: dùng dung dịch AgNO3 0,01 M làm chất chuẩn.
Phương trình chuẩn độ: 2 CN- + Ag+ ⇋ Ag(CN)2-
Trả lời cho các câu 17, 18 dưới đây:
Trong quy trình xử lý nước thải chứa cyanide, việc sử dụng dung dịch AgNO3 để chuẩn độ dựa trên phản ứng tạo phức ion Ag(CN)2- thay vì tạo kết tủa AgCN có ý nghĩa gì trong việc kiểm soát ô nhiễm và đảm bảo an toàn môi trường?
Đáp án đúng là: A
Phân tích ý nghĩa của việc tạo phức ion Ag(CN)2- thay vì tạo kết tủa AgCN đối với kiểm soát ô nhiễm và đảm bảo an toàn môi trường.
Đáp án cần chọn là: A
Thực hiện xác định nồng độ của 100ml nước thải với dung dịch AgNO3 0,01 M. Chuẩn độ 3 lần thì cho kết quả như sau.
| Lần chuẩn độ | 1 | 2 | 3 |
| Thể tích chất chuẩn đã dùng (ml) | 1,9 | 2 | 1,95 |
Nồng độ cyanide trong mẫu nước là?
Đáp án đúng là: D
Tính thể tích trung bình của AgNO3, từ đó tính nồng độ CN- theo phản ứng chuẩn độ.
Đáp án cần chọn là: D
Nhóm các bạn học sinh tiến hành làm thí nghiệm theo các bước sau:
Bước 1: Cho vào cốc thủy tinh chịu nhiệt khoảng 5 gam dầu dừa và 10 mL dung dịch NaOH 40%.
Bước 2: Đun sôi nhẹ hỗn hợp, liên tục khuấy đều bằng đũa thủy tinh khoảng 10 phút. Thỉnh thoảng cho thêm vài giọt nước cất để tránh hỗn hợp bị cạn.
Bước 3: Kết thúc phản ứng rót vào cốc thủy tinh trên 50 mL dung dịch NaCl bão hòa, khuấy nhẹ. Để nguội hỗn hợp, tách lấy khối xà phòng màu trắng nổi lên ở trên đem trộn với chất tạo hương rồi ép thành bánh.
| Đúng | Sai | |
|---|---|---|
| a) Cấu tạo của phân tử xà phòng và chất giặt rửa phổ biến thường gồm 2 phần: Phần ưa nước và phần kị nước. | ||
| b) Sau bước 3 thấy có lớp chất rắn màu trắng nổi lên chứa muối sodium của acid béo. | ||
| c) Nếu thay dầu dừa bằng dầu mỡ bôi trơn máy (thành phần chính là hydrocarbon) thì hiện tượng cũng xảy ra tương tự. | ||
| d) Sau khi thành công với mẫu ban đầu, nhóm các bạn học sinh cải tiến để sản xuất quy mô lớn hơn. Các bạn sử dụng một loại chất béo chứa 88,4% triolein về khối lượng còn lại là tạp chất trơ. Thực hiện phản ứng xà phòng hóa trên bằng dung dịch NaOH thu được một loại xà phòng chứa 82,08% muối sodium oleate về khối lượng. Giả thiết hiệu suất của cả quá trình là 80%. Quy cách đóng gói mỗi bánh xà phòng có khối lượng tịnh là 100 gam. Để sản xuất được một đơn hàng 1000 bánh xà phòng thì khối lượng chất béo tối thiểu cần sử dụng là 99,45 kg (kết quả làm tròn đến hàng phần trăm). |
Đáp án đúng là: Đ; Đ; S; S
a) Đặc điểm cấu tạo xà phòng.
b) Tính chất vật lí của xà phòng.
c) Đặc điểm cấu tạo dầu dừa (chất béo) với dầu máy bôi trong (thành phần chính là hydrocarbon).
d) 1000 bánh xà phòng ⟹ $m_{C_{17}H_{33}COONa}$
${(C_{17}H_{33}COO)}_{3}C_{3}H_{5} + 3NaOH\overset{}{\rightarrow}3C_{17}H_{33}COONa + C_{3}H_{5}{(OH)}_{3}$
$n_{{(C_{17}H_{33}COO)}_{3}C_{3}H_{5}} = \dfrac{1}{3}.n_{C_{17}H_{33}COONa}$
⟹ mchất béo
Đáp án cần chọn là: Đ; Đ; S; S
Bột đá vôi có thể được dùng để xử lí khí thải chứa sulfur dioxide từ các nhà máy điện đốt than và dầu mỏ (khử sulfur trong khí thải). Phương trình của phản ứng là
CaCO3(s) + SO2(g) ⟶ CaSO3(s) + CO2(s) (1)
Calcium sulfide (CaSO3) thu được thường được chuyển hoá thành thạch cao theo phản ứng
2CaSO3 + O2 + 4H2O ⟶ 2CaSO4.2H2O (2)
| Đúng | Sai | |
|---|---|---|
| a) Trong phản ứng (1) sulfur bị khử nên SO2 là chất oxi hoá. |
||
| b) Phản ứng (2) làm tăng hiệu suất hấp thụ SO2 trong khí thải. |
||
| c) Phản ứng sử dụng CaCO3 ở dạng bột để phản ứng xảy ra thuận lợi hơn về năng lượng. |
||
| d) Nếu trong khí thải có 49,59 lít SO2 (đkc), hiệu suất phản ứng (1) và (2) đều đạt 80% thì khối lượng CaSO4.2H2O thu được là 275,2 kg. |
Đáp án đúng là: S; S; S; S
Dựa vào tính chất hoá học của các chất.
Đáp án cần chọn là: S; S; S; S
Hiện nay, mạ điện được sử dụng rộng rãi trong thực tế, mạ điện là quá trình phủ một lớp kim loại lên bề mặt kim loại khác bằng phương pháp điện phân. Giả sử người ta cần mạ Ag lên hai mặt của một tấm kim loại (mỏng, phẳng) hình tròn có bán kính 30 cm, độ dày lớp mạ là 0,01 mm. Nếu được cung cấp nguồn điện một chiều có cường độ dòng điện $\text{I} = 2,5~\text{A}$ thì thời gian cần dùng là t giờ . Biết rằng khối lượng riêng của Ag là $10,5~\text{g}/\text{cm}^{3};\pi = 3,14$; hằng số Faraday ($\text{F} = 96500\text{C}/\text{mol}$ ); hiệu suất điện phân là $100\%$.
| Đúng | Sai | |
|---|---|---|
| a) Cần dùng thanh Ag (tinh khiết) làm anode và tấm kim loại cần mạ làm cathode. | ||
| b) Trong quá trình điện phân lượng cation kim loại trong dung dịch không thay đổi. | ||
| c) Giá trị của t là 2,95 (chỉ làm tròn ở phép tính cuối cùng, kết quả làm tròn đến hàng phần trăm). | ||
| d) Dung dịch dùng trong quá trình điện phân ở trên là $\text{AgNO}_{3}$ hoặc $\text{Cu}\left( \text{NO}_{3} \right)_{2}$. |
Đáp án đúng là: Đ; Đ; S; S
a), b), d) Lí thuyết về mạ điện.
c) Áp dụng công thức ne = It/F
Đáp án cần chọn là: Đ; Đ; S; S
Poly(vinyl chloride) (PVC) là một chất dẻo có tính cách điện tốt, không thấm nước, bền với acid vì vậy nó được dùng để sản xuất vật liệu cách điện, ống dẫn nước,…Khi đun nóng, PVC mềm ra rồi nóng chảy và khi để nguội nó lại đóng rắn. Hiện nay, trong công nghiệp sản xuất PVC người ta đi từ nguyên liệu là khí ethylene và chlorine. Quy trình sản xuất thực hiện theo sơ đồ khép kín như sau:
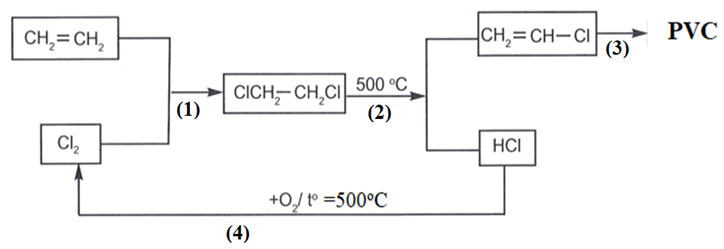
| Đúng | Sai | |
|---|---|---|
| a) Phản ứng (4) giúp giảm thải khí gây ô nhiễm môi trường và tăng hiệu quả của quá trình sản xuất. | ||
| b) Đốt cháy là một trong các phương pháp xử lí chất thải nhựa PVC mà không làm ô nhiễm môi trường. |
||
| c) PVC thuộc loại polymer nhiệt dẻo và vật liệu làm bằng PVC có thể tái chế. |
||
| d) Biết chỉ có 1,4% lượng chlorine bị thất thoát vì vậy để sản xuất 1 tấn PVC cần 576 kg chlorine (làm tròn số đến phần nguyên). |
Đáp án đúng là: Đ; S; Đ; Đ
Lí thuyết về polymer và liên hệ thực tiễn.
Đáp án cần chọn là: Đ; S; Đ; Đ
Nhỏ dung dịch mỗi chất: glycine, ethylamine, aniline, lysine, glutamic acid vào các mẩu giấu quỳ tím riêng rẽ. Có bao nhiêu dung dịch làm giấy quỳ tím chuyển thành màu xanh?
Đáp án đúng là:
Lí thuyết về tính chất hóa học của aminde và amino acid.
Làm quỳ tím chuyển mảu xanh ⟶ môi trường base.
Đáp án cần điền là: 2
Đun nóng 13,875 gam một dẫn xuất monochlorine no Y với dung dịch NaOH dư. Acid hóa dung dịch thu được sau phản ứng bằng dung dịch HNO3 thu được dung dịch A. Nhỏ từ từ vào dung dịch AgNO3 vào dung dịch A thấy tạo thành 21,525 gam kết tủa. Số nguyên tử hydrogen trong 1 phân tử Y là bao nhiêu
Đáp án đúng là:
Dựa vào tính chất hoá học của dẫn xuất halogen.
Đáp án cần điền là: 9
Quặng pyrite được sử dụng là nguyên liệu trong quá trình sản xuất iron (sắt) và sulfuric acid. Nung nóng pyrite với không khí xảy ra phản ứng: $FeS_{2} + O_{2}\overset{t^{0}}{\rightarrow}Fe_{2}O_{3} + SO_{2}$. Tổng hệ số (nguyên, tối giản nhất) của các chất trong phương trình phản ứng trên là bao nhiêu?
Đáp án đúng là:
Cân bằng phản ứng oxi hoá khử bằng phương pháp thăng bằng electron.
Đáp án cần điền là: 25
Cho công thức cấu tạo và danh pháp thay thế một số hydrocarbon không no sau:
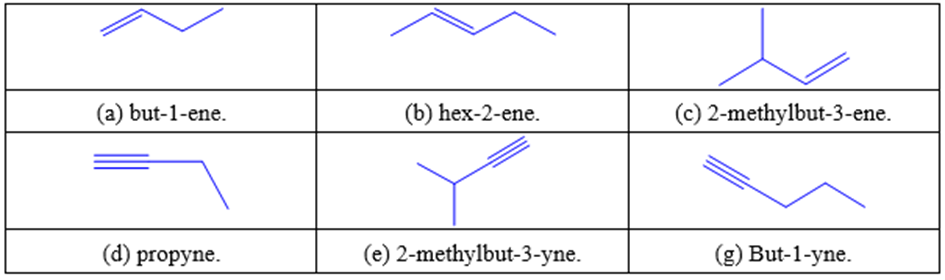
Số trường hợp có tên gọi không đúng với công thức cấu tạo là bao nhiêu?
Đáp án đúng là:

Lưu ý:
- Chọn mạch carbon dài nhất, có nhiều nhánh nhất và có chứa liên kết bội làm mạch chính.
- Đánh số sao cho nguyên tử carbon có liên kết bội (đôi hoặc ba) có chỉ số nhỏ nhất (đánh số mạch chính từ đầu gần liên kết bội).
- Dùng chữ số (1, 2, 3,... ) và gạch nối (-) để chỉ vị trí liên kết bội (nếu chỉ có một vị trí duy nhất của liên kết bội thì không cần).
- Nếu alkene hoặc alkyne có nhánh thì cần thêm vị trí nhánh và tên nhánh trước tên của alkene và alkyne tương ứng với mạch chính.
Đáp án cần điền là: 5
Biến thiên enthalpy chuẩn của quá trình H2O(s) ⟶ H2O(l) là 6,020 kJ.
Biết rằng để làm cho nhiệt độ của 1 mol nước lỏng thay đổi 1 °C cần một nhiệt lượng là 75,4 J. Giả sử mỗi viên nước đá tương ứng với 1 mol nước, số viên đá tối thiểu cần tan chảy để có thể làm lạnh 500 gam nước lỏng ở 20 °C xuống 0 °C là x viên. Tính giá trị của x (làm tròn đến hàng đơn vị).
Đáp án đúng là:
Năng lượng của phản ứng hoá học.
Đáp án cần điền là: 7
Bệnh Wilson là bệnh do cơ thể tích tụ quá mức ion Cu2+ có thể được điều trị bằng penicillamine (Pen), một hợp chất có nhóm –SH (thiol). Penicillamine tạo phức bền với ion Cu2+ theo phản ứng:
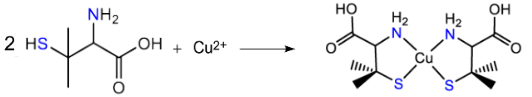
Cho các phát biểu sau:
(1) Việc tạo phức [Cu(Pen)2] giúp loại bỏ ion Cu2+ ra khỏi cơ thể dưới dạng không độc.
(2) Phức chất [Cu(Pen)2] tan trong nước, dễ đào thải qua nước tiểu.
(3) Penicillamine là phối tử một càng, chỉ có thể tạo liên kết với Cu2+qua nhóm –SH.
(4) Cơ chế điều trị bệnh Wilson dựa trên khả năng tạo phức bền với Cu2+ để làm giảm nồng độ Cu2+ tự do trong cơ thể.
(5) Ngoài nhóm –SH, penicillamine còn có thể tạo liên kết với ion kim loại qua nhóm –NH2, giúp tạo phức bền hơn.
(6) Penicillamine chỉ có thể tạo phức với ion Cu2+ trong môi trường base mạnh và ở nhiệt độ trên 100°C.
Hãy liệt kê các phát biểu đúng theo thứ tự tăng dần (1234, 245 ,…)
Đáp án đúng là:
Dựa vào phản ứng penicillamine tạo phức bền với ion Cu2+ và ứng dụng của phản ứng này.
Đáp án cần điền là: 1245


