Đề thi thử đại học môn Hóa đề số 37
Thời gian thi : 90 phút - Số câu hỏi : 60 câu - Số lượt thi : 156
Chú ý: Để xem lời giải chi tiết vui lòng chọn "Click vào đề thi"
Một số câu hỏi trong đề thi
Câu 1: Cho 27,4 gam Ba tan hết vào nước thu được dung dịch X. Cho dung dịch X tác dụng với 150ml dung dịch FeSO4 1M, lọc lấy kết tủa, rồi nung trong không khí đến khối lượng không đổi còn lại chất rắn có khối lượng là (Cho H = 1, O = 16, Fe = 56, S = 32, Ba = 137)
Câu 2: Để xà phòng hóa hoàn toàn 3,28 gam hỗn hợp hai este được tạo ra từ hai axit đơn chức, mạch hở và một ancol đơn chức, mạch hở cần dùng 500ml dung dịch NaOH 0,1M. Khối lượng muối thu được sau phản ứng xà phòng hóa là (Cho H = 1, C = 12, Na = 23, O = 16)
Câu 3: Cho 8,9 gam alanin tác dụng vừa đủ với dung dịch NaOH thu được dung dịch X. Đem dung dịch X tác dụng với dung dịch HCl (dư), thu được dung dịch Y. Cô cạn cẩn thận dung dịch Y (trong quá trình cô cạn không xảy ra phản ứng hóa học) thu được khối lượng chất rắn khan là (Cho H = 1, C = 12, Na = 23, O = 16, Cl = 35,5, N = 14)
Câu 4: Dãy gồm các chất đều có khả năng làm mất màu nước brom là
Câu 5: Sự mô tả nào sau đây không đúng hiện tượng hóa học?
Câu 6: Dung dịch CH3NH2 có khả năng phản ứng với tất cả các chất trong dãy nào sau đây?
Câu 7: Ankan có mạch cacbon không phân nhánh là ankan mà trong phân tử chỉ chứa các nguyên tử C.
Câu 8: Trong phòng thí nghiệm khi điều chế Cl2 từ MnO2 và dung dịch HCl đặc, đung nóng, để loại bỏ khí HCl lẫn trong Cl2 người ta thường rửa khí này bằng
Câu 9: Thủy phân hoàn toàn 1 mol pentapeptit X thì thu được 3 mol glixin, 1 mol analin và 1 mol valin. Khi thủy phân không hoàn toàn X thì trong hỗn hợp sản phẩm thấy có các đipeptit Ala - Gly, Gly - Ala và tripeptit Gly - Gly - Val. Phần trăm khối lượng của N trong X là (Cho H = 1, C = 12, N = 14, O = 16)
Câu 10: Thuỷ phân hoàn toàn 88,8 gam một triglixerit thu được 9,2 gam glixerol (glixerin) và hai loại axit béo. Hai loại axit béo đó là (Cho H=1, C=12, N=14, O=16)
Câu 11: Hòa tan hết m gam hỗn hợp Cr và Zn vào dung dịch HCl (dư, đun nóng) thu được 8,96 lít khí (đktc). Nếu cho m gam hỗn hợp đó vào dung dịch H2SO4 đặc, nguội (dư) đến phản ứng hoàn toàn thì thu được 2,24 lít khí SO2 (sản phẩm khử duy nhất, đktc). Phần trăm số mol của Cr và Zn trong m gam hỗn hợp ban đầu lần lượt là (Cho Cr = 52, Zn = 65)
Câu 12: Hòa tan hết 10,8 gam Ag vào dung dịch HNO3 đặc, đun nóng thu được khí X (sản phẩm khử duy nhất). Hấp thụ toàn bộ khí X vào 200ml dung dịch KOH 1M thu được dung dịch Y. Cô cạn dung dịch Y rồi nung đến khối lượng không đổi thì khối lượng chất còn lại là (Cho Ag = 108, N = 14, O = 16, K = 39)
Câu 13: Hợp chất mà bằng một phản ứng hóa học không thể tạo ra HNO3 là
Câu 14: Ion nào sau đây có số electron độc thân nhiều nhất? (Cho Fe (Z = 26), Cr (Z = 24), Cu (Z = 29), Al (Z = 13))
Câu 15: Để phản ứng hết a mol kim loại m cần 1,25a mol H2SO4 và sinh ra khí X (sản phẩm khử duy nhất). Hòa tan hết 19,2 gam kim loại M vào dung dịch H2SO4 tạo ra 4,48 lít khí X (sản phẩm khử duy nhất, đktc). Kim loại M là (Cho Al = 27, Fe = 56, Mg = 24, Cu = 64)
Câu 16: X và Y đều là dẫn xuất của benzen có công thức phân tử là C8H10O2. X tác dụng với dung dịch NaOH theo tỉ lệ mol nX : nNaOH = 1 : 1. Còn Y tác dụng với dung dịch NaOH theo tỉ lệ mol nY : nNaOH = 1 : 2. Công thức cấu tạo thu gọn của X và Y lần lượt là
Câu 17: Cho m gam hỗn hợp Cu và Fe2O3 vào dung dịch H2SO4 loãng (dư), khuấy đều cho các phản ứng xảy ra hoàn toàn thấy có 3,2 gam kim loại không tan và dung dịch X. Cho NH3 (tới dư) vào dung dịch X, lọc lấy kết tủa, nung trong không khí đến khối lượng không đổi còn lại 16 gam chất rắn. Giá trị của m là (Chi H = 1, O = 16, Fe = 56, Cu = 64)
Câu 18: Cho hỗn hợp chất rắn gồm CaC2, Al4C3 và Ca vào nước thu được hỗn hợp X gồm 3 khí, trong đó có hai khí cùng số mol. Lấy 8,96 lít hỗn hợp X (đktc) chia làm hai phần bằng nhau. Phần 1 cho vào dung dịch AgNO3 trong NH3 (dư), sau phản ứng hoàn toàn, thấy tách ra 24 gam kết tủa. Phần 2 cho đi qua Ni, đun nóng thu được hỗn hợp khí Y. Thể tích O2 vừa đủ (đktc) cần dùng để đốt cháy hoàn toàn Y là (Cho H = 1, C = 12, Ag = 108, O = 16)
Câu 19: Khẳng định không đúng là
Câu 20: Phản ứng hóa học giữa các chất nào sau đây không xảy ra?
Câu 21: Nguyên tố X có Z = 29. Vị trí của X trong bảng tuần hoàn là
Câu 22: Trộn 5,4 gam bột Al với 14 gam Fe2O3 rồi tiến hành phản ứng nhiệt nhôm (không có oxi, Fe2O3 bị khử về Fe). Sau khi kết thúc phản ứng, làm nguội hỗn hợp và hòa tan hỗn hợp này bằng lượng dung dịch NaOH (dư), cho đến phản ứng hoàn toàn thu dược 1,68 lít khí (đktc). Hiệu suất phản ứng nhiệt nhôm là (Cho H = 1, O = 16, Al = 27, Fe = 56, Na = 23)
Câu 23: Trong các polime: polistiren, amilozơ, amilopectin, poli (vinyl clorua), tơ capron, poli(metyl metacrylat) và teflon. Những polime có thành phần giống nhau là:
Câu 24: Để phân biệt SO2 và SO3 (hơi) bằng phản ứng trao đổi ta dùng thuốc thử là:
Câu 25: Điện phân 200ml dung dịch chứa đồng thời AgNO3 1M và Cu(NO3)2 2M trong thời gian 48 phút 15 giây, với cường độ dòng điện 10 ampe (điện cực trơ, hiệu suất điện phân là 100%). Sau điện phân để yên bình điện phân cho các phản ứng xảy ra hoàn toàn thu được V lít khí NO (sản phẩm khử duy nhất, đktc). Giá trị của V là (Cho Ag = 108, Cu = 64)
Câu 26: Hỗn hợp X chứa đồng thời hai muối natri của hai halogen liên tiếp trong bảng tuần hoàn. Lấy một lượng X cho tác dụng vừa đủ với 100ml dung dịch AgNO3 1M thì thu được 15 gam kết tủa. Công thức phân tử của hai muối trong X là (Cho F = 19, Cl = 35,5, Br = 80, I = 127, Na = 23)
Câu 27: Khi điện phân một dung dịch với điện cực trơ, không màng ngăn thì dung dịch sau điện phân có pH tăng so với dung dịch trước khi điện phân. Vậy dung dịch đem điện phân là
Câu 28: Hòa tan hết m gam hỗn hợp hai oxit của kim loại kiềm và kiềm thổ vào dung dịch HCl (dư). Cô cạn dung dịch thu được, rồi tiến hành điện phân nóng chảy hết chất rắn (với điện cực trơ) thì ở catot sinh ra 11 gam kim loại và ở anot có 2,24 lít khí thoát ra (đktc). Giá trị của m là (Cho Cl = 35,5, O = 16)
Câu 29: Cho các chất sau tác dụng với nhau trong dung dịch a) KI + FeCl3 → b) HI + FeO → c) KI + O3 + H2O → d) KI + H2O2 → e) Pb(NO3)2 + KI → f) Cl2 + KI → g) KI + K2Cr2O7 + H2SO4 loãng → Những phản ứng hóa học tạo ra sản phẩm I2 là
Câu 30: Một loại khí than chứa đồng thời N2, CO và H2. Đốt cháy 4,48 lít khí (đktc) hỗn hợp khí này bằng lương O2 vừa đủ rồi dẫn sản phẩm cháy vào nước vôi trong (dư) thấy tách ra 10 gam kết tủa, thu được dung dịch X và có 0,56 lít khí N2 (đktc) thoát ra. Khối lượng dung dịch X thay đổi so với khối lượng dung dịch nước vôi trong ban đầu (Cho H = 1, O = 16, C = 12, Ca = 40)
Câu 31: Cho luồng khí H2 (dư) đi qua ống chứa đồng thời 0,1 mol mỗi chất sau đây đốt nóng: MgO, Fe3O4, Al2O3 và CuO. Sau khi các phản ứng xảy ra hoàn toàn, dẫn toàn bộ khí và hơi thu được qua bình đựng 100 gam dung dịch H2SO4 98% (cho rằng H2 dư không phản ứng với H2SO4 đặc, hơi nước bị hấp thụ hết). Nồng độ % của dung dịch H2SO4 thu được là (Cho H = 1, O = 16, S = 32)
Câu 32: Số lượng hợp chất hữu cơ chứa C, H, O có khối lượng phân tử 74u, vừa có khả năng tác dụng với Na, vừa có khả năng tham gia phản ứng tráng bạc là (Cho H = 1, C = 12, O = 16)
Câu 33: Một hỗn hợp X gồm C2H6, C3H6, C4H6 có tỉ khối so với H2 là 18,6. Đốt cháy hoàn toàn 4,48 lít hỗn hợp X (đktc), sản phẩm cháy cho lần lượt qua bình I đựng dung dịch H2SO4 đặc, (dư), bình II đựng dung dịch KOH (dư) thì khối lượng bình I, II tăng lần lượt là (Cho H = 1, C = 12, O = 16)
Câu 34: Không thể điều chế axeton bằng phương pháp
Câu 35: Hợp chất X được tạo ra từ ancol đơn chức và amino axit chứa một chức axit và một chức amin. X có công thức phân tử trùng với công thức đơn giản nhất. Để đốt cháy hoàn toàn 0,89 gam X cần vừa đủ 1,2 gam O2 và tạo ra 1,32 gam CO2, 0,63 gam H2O. Khi cho 0,89 gam X tác dụng với 200ml dung dịch NaOH 1M rồi cô cạn thì khối lượng chất rắn khan thu được là (Cho H = 1, C = 12, N = 14, Na = 23, O = 16)
Câu 36: Cho phản ứng thuận nghịch sau ở trạng thái cân bằng: N2 (k) + 3H2 (k) <=> 2NH3 (k) ∆H < 0 Những yếu tố tác động lên hệ cân bằng đều làm cho cân bằng chuyển dịch theo chiều thuận là
Câu 37: Cho xiclopropan vào nước brom thu được chất hữu cơ X. Cho X vào dung dịch NaOH đun nóng (dư), tạo ra sản phẳm hữu cơ Y. Y tác dụng với CuO, đốt nóng thu được hợp chất đa chức Z. Khi đem n mol Z tham gia phản ứng tráng bạc thì số mol Ag tối đa thu được là
Câu 38: Hòa tan hết 4 gam oxit FexOy cần dùng 52,14ml dung dịch HCl 10% (d = 1,05 gam/ml). Để khử hóa hoàn toàn 4 gam oxit sắt này cần ít nhất thể tích khí CO (đktc) là (Cho H = 1, Cl = 35,5, O = 16, C = 12)
Câu 39: Dãy các phân tử và ion mà mỗi phân tử và ion đó vừa có tính oxi hóa, vừa có tính khử là
Câu 40: Cho sơ đồ phản ứng:
CH3OH 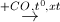 (X)
(X) 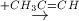 (Y)
(Y) 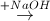 (Z) → propan-2-ol
Công thức cấu tạo thu gọn của X và Z lần lượt là
(Z) → propan-2-ol
Công thức cấu tạo thu gọn của X và Z lần lượt là
Câu 41: Hợp chất MX3 có tổng số hạt proton là 75. Công thức hóa học của MX3 là (Cho Fe(Z = 26), Cr(Z = 24), Cl(Z = 17), Al(Z = 13), Br(Z = 35))
Câu 42: Cho 0,3 mol hỗn hợp khí gồm hai anken có mạch cacbon không phân nhánh lội từ từ qua bình đựng nược brom (dư) sau phản ứng hoàn toàn thấy khối lượng của bình tăng 16,8 gam. Biết hai anken là chất khí ở điều kiện thường. Công thức cấu tạo thu gọn của hai anken là (Cho H = 1, C = 12)
Câu 43: Cho 10,8 gam bột Al tan hoàn toàn trong dung dịch HNO3 thấy thoát ra 3 khí N2, NO và N2O có tỉ lệ mol tương ứng là 1 : 2 : 1, Trong dung dịch thu được không có NH4NO3. Thể tích 3 khí trên (đktc) là (Cho H = 1, N = 14, Al = 27, O = 16)
Câu 44: Trong các dung dịch: Phenyl amoni clorua, natri axetat, natri phenolat, natri hiđrosunfat, natri clorua. Những dung dịch có pH < 7 là
Câu 45: Khi đốt cháy hoàn toàn hỗn hợp các ancol no mạch hở thì thu được tỉ lệ mol 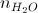 :
: 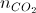 = T.T có khoảng giá trị
= T.T có khoảng giá trị
Câu 46: Thủy phân hoàn toàn 34,2 gam saccarozơ, thu lấy toàn bộ sản phẩm hữu cơ rồi đem tác dụng với Cu(OH)2 (dư) trong môi trường kiềm cho tới phản ứng hoàn toàn thu được khối lượng kết tủa Cu2O là (Cho H = 1, C = 12, Cu = 64, O = 16)
Câu 47: Hợp chất hữu cơ X có công thức phân tử C3H5Br3. Cho X tác dụng với dung dịch NaOH loãng (dư), đun nóng rồi cô cạn dung dịch thu được thì còn lại chất rắn trong đó có chứa sản phẩm hữu cơ của Na. X có tên gọi là
Câu 48: Trong các dung dịch riêng biệt chứa các chất tan: mantozơ, glucozơ, saccarozơ, glixerol (glixerin), axit fomic, anđehit fomic, axit axetic. Những dung dịch vừa hòa tan Cu(OH)2 vừa tham gia phản ứng tráng bạc là
Câu 49: Cho sơ đồ phản ứng:
Fe 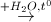 (X)
(X) 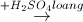 (Y)
(Y) 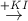 (Z)
(Z) 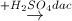 (Y)
X và Z lần lượt là
(Y)
X và Z lần lượt là
Câu 50: Hòa tan hoàn toàn m gam hỗn hợp 3 kim loại bằng dung dịch HNO3 thu được V lít hỗn hợp khí D (đktc) gồm NO và NO2. Tỉ khối của D so với H2 là 18,2. Giả thiết không có phản ứng tạo NH4NO3. Tổng khối lượng muối trong dung dịch thu được tính theo m và V là (Cho H = 1, N = 14, O = 16)
Câu 51: Phát biểu không đúng là
Câu 52: Cho thế điện cực chuẩn: Zn2+/Zn = -0,76V; Fe2+/Fe = -0,44V; Ni2+/Ni = -0,26V; Cu2+/Cu = +0,34V. Pin điện hóa có suất điện động chuẩn nhỏ nhất là pin tạo bởi hai điện cực
Câu 53: Trong các chất: NaCl, SO2, FeSO4, H2S, Na2SO4. Những chất có khả năng tác dụng với K2Cr2O7 (trong môi trường H2SO4 loãng dư) là
Câu 54: Hỗn hợp X gồm 2 axit hữu cơ đơn chức, đồng đẳng kế tiếp. Lấy m gam X đem tác dụng hết với 12 gam Na thì thu được 14,27 gam chất rắn và 0,336 lít H2 (đktc). Cũng m gam X tác dụng vừa đủ với 600ml nước brom 0,05M. Công thức phân tử của hai axit là (Cho H = 1, C = 12, O = 16, Br = 80, Na = 23)
Câu 55: Khi tách nước nội phân tử 3-metylpentan-2-ol thu được anken X có cặp đồng phân hình học. Cho X vào dung dịch KMnO4 loãng, nóng, có mặt H2SO4 loãng thu được các sản phẩm hữu cơ là
Câu 56: Biết trong dung dịch NH3 có Kb = 1,8.10-5. Dung dịch chứa đồng thời NH4Cl 0,1M và NH3 0,1M có pH là
Câu 57: Phương pháp thủy luyện dùng để tách Au thường được sử dụng các hóa chất nào?
Câu 58: Chất X có thành phần nguyên tố: C, H, O và tỷ khối hơi của X đối với H2 là 30. X có phản ứng với dung dịch NaOH, số công thức cấu tạo phù hợp của X là (Cho H = 1, C = 12, O = 16)
Câu 59: Một tấm kim loại bằng Au bị bám một lớp sắt trên bề mặt. Ta có thể rửa lớp sắt đó bằng cách dùng dung dịch nào trong số các dung dịch sau: (I) CuSO4 dư, (II) FeSO4 dư, (III) FeCl3 dư, (IV) ZnSO4 dư, (V) HNO3
Câu 60: Cho các axit sau, hãy sắp xếp các axit đó theo thứ tự tăng dần tính axit (độ mạnh): 1. CH2=CH-COOH; 2. CH3-CH2-COOH; 3. CH≡C-COOH
Bạn có đủ giỏi để vượt qua
| Xếp hạng | Thành viên | Đúng | Làm | Đạt | Phút |
| 1 |
|
50 | 50 | 100% | 2.73 |
| 2 |
|
40 | 50 | 80% | 90.2 |
| 3 |
|
30 | 50 | 60% | 81.93 |
| 4 |
|
29 | 50 | 58% | 54.65 |
| 5 |
|
18 | 21 | 86% | 26.45 |
| 6 |
|
9 | 15 | 60% | 7 |
| 7 |
|
0 | 0 | 0% | 0.32 |
| 8 |
|
21 | 59 | 36% | 36.6 |
| 9 |
|
32 | 60 | 53% | 15.9 |
| 10 |
|
1 | 3 | 33% | 0.72 |
| 11 |
|
16 | 49 | 33% | 49.47 |