Đề thi thử đại học môn hóa năm 2013 đề số 8
Thời gian thi : 60 phút - Số câu hỏi : 48 câu - Số lượt thi : 258
Chú ý: Để xem lời giải chi tiết vui lòng chọn "Click vào đề thi"
Một số câu hỏi trong đề thi
Câu 1: Hỗn hợp X gồm SO2 và O2 có tỉ khối so với H2 bằng 28. Lấy 4,48 lít khí hỗn hợp X (đtkc) cho đi qua bình đựng V2O5 nung nóng. Hỗn hợp thu được cho lội qua dung dịch Ba(OH)2 dư thấy 33,51 gam kết quả. Hiệu suất phản ứng oxi hóa SO2 thành SO3 là
Câu 2: Hỗn hợp X gồm hai chất đơn chức X1, X2 cấu tạo từ C, H, O mạch hở. Cho 12,2 gam X tác dụng vừa đủ với 150 gam dung dịch NaOH 4% đung nóng, thoát ra ancol Y. Cho Y qua bình đựng Na dư thì khối lượng bình này tăng lên 3,6 gam và có 0,08 gam khí thoát ra. Công thức của X1, X2 lần lượt là
Câu 3: Cho V lít hỗn hợp khí X gồm Cl2 và O2 (ở đktc) tác dụng vừa đủ với hỗn hợp Y (gồm 2,7 gam Al và 3,6 gam Mg). Kết thúc thí nghiệm thu được 22,1 gam sản phẩm. Giá trị của V là
Câu 4: Hòa tan hoàn toàn hỗn hợp gồm 0,02 mol FeS2 và 0,03 mol FeS vào lượng dư dung dịch H2SO4 đặc, nóng được dung dịch X và khí SO2 (sản phẩm khử duy nhất). Hấp thụ hết SO2 bằng một lượng vừa đủ dung dịch KMnO4 thu được dung dịch không màu, trong suốt có pH = 2, Thể tích của dung dịch Y là
Câu 5: X, Y là các chất hữu cơ đồng chức chứa C, H, O, Khi tác dụng với AngNO3/NH3 thì 1 mol mỗi chất đều tạo ra 4 mol Ag, còn khi đốt cháy X, Y thì được tỉ lệ như sau: - Đối với X: nO2: nCO2 : nH2O = 1 : 1 : 1 - Đối với Y: nO2: nCO2 : nH2O = 1,5 : 2 : 1 Công thức cấu tạo thu gọn của X, Y lần lượt là
Câu 6: Thực hiện các thí nghiệm sau: (1) Đốt dây sắt trong khí Clo. (2) Đốt nóng hỗn hợp Fe và S (trong điều kiện có oxi) (3) Cho FeO vào dung dịch HNO3 (loãng, dư) (4) Cho Fe vào dung dịch Fe2(SO4)3 (5) Cho Fe vào dung dịch H2SO4 ( loãng dư) Có bao nhiêu thí nghiệm tạo ra muối sắt(II)?
Câu 7: Cho m gam hỗn hợp gồm FeO, Fe2O3 và Fe3O4 vào dung dịch HCl dư chia dung dịch thu được làm hai phần bằng nhau - Phần 1: cô cạn được m1 gam muối khan - Phần 2 : sục khí Cl2 dư vào rồi cô cạn được m2 gam muối khan Biết m2 – m1 = 0,71 gam và trong hỗn hợp đầu tỉ lệ mol FeO : Fe2O3 =1 : 1 Giá trị của m là
Câu 8: Hợp chất hữu cơ X có công thức phân tử C4H6O2. Cho X tác dụng với dung dịch NaOH, cô cạn được chất rắn Y và hỗn hợp hơi Z, từ Z chưng cất thu được E, E tham gia phản ứng tráng bạc cho sản phẩm F, F tác dụng với NaOH lại thu được Y. Công thức cấu tạo của X là
Câu 9: Cho các chất: C6H5OH (1); CH3-C6H4-OH (2) ; C6H5-CH2OH (3); CH3-C6H4-CH2OH (4). Cặp chất là đồng đẳng của nhau là
Câu 10: Đốt cháy hoàn toàn a mol axit hữu cơ X thu được 2a mol CO2. Mặt khác để trung hòa a mol X cần dung vừa đủ 2a mol NaOH. Kết luận nào dưới đây không đúng?
Câu 11: Cho các dung dịch sau: HCl, Ca(NO3)2, FeCl3, AgNO3, NH3, (HCl + NaNO3), (NaHSO4 + NaNO3); (NaHCO3 + NaNO3) . Số dung dịch có thể hòa tan Cu kim loại là
Câu 12: Nhận định nào về các nguyên tố kim loại sau đây đúng?
Câu 13: Để nhận biết hai bình khí CO2 và SO2, cách nào sau đây không đúng?
Câu 14: Tiến hành các thí nghiệm sau (1).Sục khí H2S vào dung dịch FeSO4. (2). Sục khí H2S vào dung dịch CuSO4. (3). Sục khí CO2 dư vào dung dịch Na2SiO3. (4). Sục khí CO2 dư vào dung dịch Ca(OH)2. (5).Nhỏ từ từ dung dịch NH3 đến dư vào dung dịch Al2(SO4)3. (6). Nhỏ từ từ dung dịch Ba(OH)2 đến dư vào dung dịch Al2(SO4)3. Sau khi các phản ứng xảy ra hoàn toàn, số thí nghiệm thu được kết tủa là
Câu 15: Tính chất nào sau đây không đúng với H3N+- CH(COOH)-COO-?
Câu 16: Hai đồng phân X và Y có cùng công thức phân tử C3H6O2. Tính chất của X và Y thể hiện trong bảng sau: Dung dịch NaOH Na AgNO3/NH3 X Có phản ứng Có phản ứng Không phản ứng Y Có phản ứng Không phản ứng Có phản ứng Công thức cấu tạo của X và Y lần lượt là
Câu 17: Cho một chất X tác dụng với dung dịch H2SO4 đặc nóng sinh ra khí SO2 (sản phẩm khử duy nhất). Nếu tỉ lệ mol H2SO4 đem dùng : số mol SO2= 4:1 thì X có thể là chất nào trong các chất sau?
Câu 18: Cho P2O5 tác dụng với dung dịch NaOH được dung dịch gồm hai chất tan. Hai chất đó có thể là
Câu 19: Khí nào sau đây không bị oxi hóa bởi nước Gia-ven.
Câu 20: Chia 1 lít dung dịch Br2 0,5M thành hai phần bằng nhau. Sục vào phần một 4,48 lít khí HCl được dung dịch X có pH = x. Sục phần hai vào 2,24 lít khí SO2 được dung dịch Y có pH = y (giả sử thể tích dung dịch không thay đổi, các khí đo ở đktc). Mối quan hệ giữa x và y là
Câu 21: Đun 57,5 gam etanol với H2SO4 đặc ở 1700C. Dẫn sản phẩm khí và hơi lần lượt đi qua các bình riêng rẽ: dung dịch NaOH, CuCO4 khan, dung dịch Br2/CCl4 dư. Sau khi thí nghiệm thấy khối lượng bình cuối cùng tăng thêm 2,1 gam. Hiệu suất của quá trình đehiđrat hoá etanol là
Câu 22: Nung hỗn hợp bột gồm 15,2 gam Cr2O3 và m gam Al ở nhiệt độ cao. Sau khi phản ứng xảy ra hoàn toàn thu được 23,3 gam hỗn hợp chất rắn X. Cho toàn bộ X phản ứng với HCl(dư) thoát ra V lít khí H2 (đktc). Giá trị của V là
Câu 23: Cho các chất sau: HO-C6H4CH2OH; H2NCH2COOCH3; H2NCH2-CH(NH2)COOH; CH3COONH4 ; HO-C6H4-CH2-NH2. Số chất có tính lưỡng tính là
Câu 24: Dẫn V lít (đktc) hỗn hợp X gồm axetilen và H2 qua ống sứ đựng bột Ni nung nóng, thu được hỗn hợp khí Y. Dẫn Y vào lượng dư dung dịch AgNO3/NH3 được 12 gam kết tủa. Khi ra khỏi dung dịch phản ứng vừa đủ với dung dịch chứa 16 gam Br2 và còn lại khí Z. Đốt cháy hoàn toàn Z thu được 0,1 mol CO2 và 0,25 mol nước. Giá trị của V là
Câu 25: Có bao nhiêu hợp chất chứa vòng benzen có công thức phân tử C7H6O2 vừa tác dụng với dung dịch NaOH, vừa tham gia phản ứng tráng bạc?
Câu 26: Xà phòng hóa hoàn toàn m gam chất béo X bằng 200 gam dung dịch NaOH 8%. Sau phản ứng được 9,2 gam glixerol và 94,6 gam chất rắn khan. Công thức cấu tạo của X là
Câu 27: Khi nói về peptit và protein, phát biểu nào sau đây sai?
Câu 28: Nhận định nào sau đây đúng?
Câu 29: Keo ure fomanđehit được tổng hợp theo sơ đồ: H2NCONH2 + HCHO ![\xrightarrow[t^{0}]{H^{+}}](http://images.tuyensinh247.com/picture/learning/exam/2013/1118/4201_457520_1.gif) H2NCONH-CH2OH →-(-NH-CONH-CH2-)-n Biết hiệu suất của quá trình trên là 80%. Khối lượng dung dịch HCHO 90% cần lấy để tổng hợp được 180 gam keo dán là
H2NCONH-CH2OH →-(-NH-CONH-CH2-)-n Biết hiệu suất của quá trình trên là 80%. Khối lượng dung dịch HCHO 90% cần lấy để tổng hợp được 180 gam keo dán là
Câu 30: Cho 5,1 gam hỗn hợp X gồm Fe và Mg vào 250ml dung dịch CuSO4 sau khi các phản ứng xảy ra hoàn toàn, lọc thu được 6,9 gam chất rắn Y và dung dịch Z chứa hai muối. Cho dung dịch NaOH dư vào Z lọc kết tủa nung trong không khí đến khối lượng không đổi được 4,5 gam chất rắn E. Nồng độ mol dung dịch CuSO4 là
Câu 31: Cho cân bằng hóa học sau: Cr2O32- + H2O 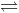 2CrO42- + 2H+
(da cam) (vàng)
Trong các trường hợp sau : (1) thêm OH- vào hệ ; (2) pha loãng ; (3) thêm BaCl2 ; (4) thêm Na2CO3 ; (5) thêm NH4Cl ; (6) thêm NaCl. Số trường hợp khi tác động vào hệ làm cho dung dịch chuyển sang màu vàng là
2CrO42- + 2H+
(da cam) (vàng)
Trong các trường hợp sau : (1) thêm OH- vào hệ ; (2) pha loãng ; (3) thêm BaCl2 ; (4) thêm Na2CO3 ; (5) thêm NH4Cl ; (6) thêm NaCl. Số trường hợp khi tác động vào hệ làm cho dung dịch chuyển sang màu vàng là
Câu 32: Có 4 ống nghiệm được đánh số thứ tự 1, 2, 3, 4. Mỗi ống nghiệm chứa một trong các dung dịch AgNO3, ZnCl2, HI, Na2CO3. Biết rằng: -Dung dịch trong ống nghiệm 2 và 3 tác dụng được với nhau sinh ra chất khí. -Dung dịch trong ống nghiệm 2 và 4 không phản ứng được với nhau. -Dung dịch trong ống nghiệm 2 và 4 không phản ứng được với nhau. Dung dịch trong các ống nghiệm 1, 2, 3, 4 lần lượt là:
Câu 33: Hỗn hợp X gồm Fe và Cu với tỉ lệ phần trăm khối lượng là 4:6 . Hòa tan m gam X bằng dung dịch HNO3 thu được 0,448 lít khí NO( sản phẩm khử duy nhất, đktc) dung dịch Y và có 0,65m gam kim loại không tan. Khối lượng muối tạo thành trong dung dịch Y là
Câu 34: Có 6 gói bột màu đen: FeS, CuS, Ag2O, MnO2, CuO, PbS. Nếu chỉ dùng dung dịch HCl thì có thể nhận biết được bao nhiêu gói bột ?
Câu 35: Hòa tan hoàn toàn 12,9 gam hỗn hợp X gồm Cu, Zn vào dung dịch H2SO4 đặc nóng được 0,14 mol SO2; 0,64 gam S và dung dịch muối sunfat. Thành phần % khối lượng Cu trong hỗn hợp ban đầu là
Câu 36: Hòa tan chất X vào nước thu được dung dịch trong suốt, rồi thêm tiếp dung dịch chất Y thì thu được chất Z (làm vẩn đục dung dịch ). Các chất X, Y, Z lần lượt là:
Câu 37: Cho các dung dịch sau đây tác dụng với nhau từng đôi một : NaHSO4, NaHCO3, BaCl2, NaOH, NH4HCO3. Số phản ứng xảy ra là
Câu 38: Chất X có thể tác dụng với Al, Fe, H2SO3, Ca(OH)2, H2S, FeCl2, KI. X là chất nào trong các chất sau?
Câu 39: Cặp chất nào sau đây khi phản ứng kết thúc tạo ra phenol?
Câu 40: X, Y là các đồng phân có cùng công thức phân tử C5H10. X làm mất màu dung dịch Br2 ở điều kiện thường tạo sản phẩm là 1,3-đibrom-2-metylbutan. Y phản ứng với Br2 khi chiếu sáng tạo ra một dẫn xuất monobrom duy nhất. X, Y lần lượt là
Câu 41: Cho các hiđrocacbon: eten, axetilen, benzen, toluen, stiren, xiclopropan, naphtalein, isopentan. Số chất làm mất màu dung dịch Br2 là
Câu 42: Cho phương trình sau: C6H5CH=CH2 + KMnO4 + H2SO4 →C6H5COOH + CO2+ MnSO4 + K2SO4 + H2O Tổng hệ số tối giản của các chất tham gia phản ứng khi cân bằng là
Câu 43: Cho các chất riêng biệt sau: FeSO4, AgNO3, Na2SO3, H2S, NaI, NaCl, Fe3O4, Fe2O3 tác dụng với dung dịch H2SO4 đặc nóng. Số trường hợp xảy ra phản ứng oxi hóa khử là
Câu 44: Trong các chất sau: H2O2; O3; HNO3; KMnO4. Chất chỉ thể hiện tính oxi hóa không thể hiện tính khử là
Câu 45: Cho 50 gam dung dịch axit đơn chức X có nồng độ 7,4% tác dụng với dung dịch NaOH dư, cô cạn dung dịch được chất rắn Y. Nung Y với CaO đến phản ứng hoàn toàn được 11,2 lít khí Z. Công thức của X là
Câu 46: Trộn dung dịch chứa Ba2+; OH- 0,06 mol và Na+ 0,02 mol với dung dịch chứa HCO3- 0,04 mol ; CO32- 0,03 mol và Na+.Khối lượng kết tủa thu được sau khi trộn là
Câu 47: Trộn dung dịch chứa Ba2+; OH- 0,06 mol và Na+ 0,02 mol với dung dịch chứa HCO3- 0,04 mol ; CO32- 0,03 mol và Na+.Khối lượng kết tủa thu được sau khi trộn là
Câu 48: Cho các chất sau: CH3OH, C2H5OH, CH3CHO,C2H2, C2H4, C4H10, CH3COONa, CH3CN. Số chất tạo được CH3COOH chỉ bằng 1 phản ứng là
Bạn có đủ giỏi để vượt qua
| Xếp hạng | Thành viên | Đúng | Làm | Đạt | Phút |
| 1 |
|
38 | 50 | 76% | 52.82 |
| 2 |
|
33 | 49 | 67% | 4.72 |
| 3 |
|
21 | 28 | 75% | 17.25 |
| 4 |
|
17 | 31 | 55% | 36.68 |
| 5 |
|
21 | 50 | 42% | 58.35 |
| 6 |
|
11 | 24 | 46% | 1.13 |
| 7 |
|
19 | 49 | 39% | 51.25 |
| 8 |
|
1 | 1 | 100% | 2.53 |
| 9 |
|
2 | 5 | 40% | 11.87 |
| 10 |
|
4 | 11 | 36% | 2.65 |
| 11 |
|
16 | 49 | 33% | 17.52 |
| 12 |
|
0 | 0 | 0% | 0.03 |
| 13 |
|
0 | 0 | 0% | 9.47 |
| 14 |
|
5 | 13 | 38% | 14.8 |
| 15 |
|
0 | 1 | 0% | 0.65 |