Đề thi thử ĐH môn Hóa đề số 45
Thời gian thi : 90 phút - Số câu hỏi : 60 câu - Số lượt thi : 197
Chú ý: Để xem lời giải chi tiết vui lòng chọn "Click vào đề thi"
Một số câu hỏi trong đề thi
Câu 1: Cho 6g kẽm hạt vào một cốc đựng dung dịch H2SO4 4M ở nhiệt thường. Tác động nào sau đây không làm tăng tốc độ phán ứng?
Câu 2: Để thu được CO2 tinh khiết từ phàn ứng CaCC>3 với dung dịch HC1, người ta cho sản phẩm khí đi qua lần lượt các bình đựng các dung dịch nào sau dây?
Câu 3: Đốt cháy hoàn toàn 0,1 mol cste X rồi dẫn sản phẩm cháy vào dung dịch Ca(OH)2 dư thu được 20g kết tủa (cho H =1, C=12, O =16, Ca = 40). Công thức cẩu tạo của X là
Câu 4: Cho các chất: Dung dịch H2SO4 0,1M. KMnO4 rắn. Dung dịch NaOH 0.1M Có thể điều chế khí oxi từ chất nào trong các chất trên?
Câu 5: Cho 4,2 gam anđehit X mạch hở phản ứng hết với Ag2O trong dung dịch NH3 dư. Toàn bộ lượng bạc thu được hoà tan hết vào dung dịch HNO3 đặc, nóng, n được 3,792 lít NO2 ở 27°c và 740 mm Hg. Biết ti khối hơi của X so với nitơ nhỏ 4 (cho H=1, C = 12, N=14. O = 16, Ag = 108). Công thức cấu tạo của X là
Câu 6: Ankađien sau đây có bao nhiêu đồng phân hình học?
Câu 7: Cặp chất nào sau đây có khả năng phản ứng với nhau trong dung dịch?
Câu 8: Cho phản ứng: FeCH + KmnO4 + H2SO4 —> Fe2(SO4)3 + Cl2 + MnSO4 + K2SO4 + H2SO4 Hệ số tối giản của các chất tham gia phản ứng trong phương trình trên lần lượt là
Câu 9: Axit nào sau đây mạnh nhất?
Câu 10: Chia dung dịch H2SO4 thành 3 phần bằng nhau: - Trung hoà phần một vừa đủ bởi 200ml dung dịch NaOH 1M. - Trộn phần hai với phần ba rồi cho tiếp vào một lượng dung dịch NaOI 1 như đà dùng ở phần một, cô cạn thu dược m gam muối (cho H = 1,O = 16, Na=23, S= 32). Giá trị m là
Câu 11: Phát biểu nào sau đây đúng?
Câu 12: Để diệt chuột trong một nhà kho, người la đốt lưu huỳnh rồi đóng kín cửa nhà kho lại. Chuột hít phải khói sẽ bị sưng yết hầu, co giật, tê liệt cơ quan hô hấp dần đến bị ngạt mà chết. Chất gì đã làm chuột chết?
Câu 13: Để tách phenol ra khỏi hỗn hợp lỏng gồm phenol, benzen và anilin cỏ thể làm theo cách nào sau đây?
Câu 14: Để rửa sạch chai lọ đựng phenol, có thể làm theo cách nào sau đây?
Câu 15: Phản ứng sau đạt trạng thái cân bằng trong bình kín:
2NaHCO3 (r) 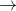 Na2CO3 (r) + CO2 (k) + H2O (k)
Nếu tăng thể tích của bình chứa, giữ nguyên nhiệt độ thì số mol Na2CO3 thay đổi như thế nào?
Na2CO3 (r) + CO2 (k) + H2O (k)
Nếu tăng thể tích của bình chứa, giữ nguyên nhiệt độ thì số mol Na2CO3 thay đổi như thế nào?
Câu 16: Hợp chất hữu cơ X (chứa C, H, O) không no. Hiđro hoá hoàn toàn X thu được hợp chất hữu cơ Y. Đun Y trong H2SO4 đặc ở 170°c nhận dược hợp chất z. Trùng hợp z thu được poli iso-butilen. Công thức cấu tạo của X là
Câu 17: Ancol mạch nhánh X có công thức phân tử là C5H12O. Oxi hoá X trong ống đựng CuO đun nóng thu được xeton. Trong các công thức cấu tạo sau, công thức nào thoả mãn điều kiện của X:
Câu 18: Cho các phân tử chất hữu cơ: H3C-CH3(X); H2C – CH2(Y); HC=CH(Z). Nhận xét nào sau đây là đúng?
Câu 19: Khí nào sau đây không thể đốt cháy trong không khí được?
Câu 20: Có thể phân biệt cặp chất nào sau đây bằng nước Br2?
Câu 21: Cho dư hỗn hợp Na, Mg vào 73,6g dung dịch H2SO4 26,63% thì thể tích khí H2 thoát ra (ờ đktc) là
Câu 22: Este X có công thức đơn giản nhất là C2H4O2. Đun sôi 4,4 gam X với 200 gam dung dịch NaOH 3% đến khi phản ứng hoàn toàn. Cô cạn dung dịch sau phản ứng thu được 8,1 gam chất rắn khan. Công thức của X là
Câu 23: Đường nào sau đây không thuộc loại cacbohiđrat?
Câu 24: Hiđrocacbon X ở thể lỏng ở diều kiện thường có phần trăm khối lượng H2 xấp xỉ 7,7%. X có thể lảm mất màu dung dịch brom. Chất nào sau đây là công thức phân từ của chất X?
Câu 25: Phát biểu nào sau đây không đúng?
Câu 26: Khi điện phân dung dịch AgNO3, pH dung dịch thu dược
Câu 27: Đốt cháy hoàn toàn m gam hỗn hợp 2 ankin cho ra 13,2 gam CO2 và 3,6 gam H2O. Tính khối lượng brom tối đa có thể cộng vào m gam hồn hợp trên (cho H= 1,C = 12, O =16, Br= 80).
Câu 28: Khẳng định nào sau đây đúng?
Câu 29: Hiđrocacbon có công thức cấu tạo (CH3)3C-C  CH có tên quốc tế là
CH có tên quốc tế là
Câu 30: Đốt cháy hoàn toàn hỗn hợp 2 chất hữu cơ X, Y cùng dãy đồng đẳng (chứa C, H, O) thu được 3,5 lít CO2 (điều kiện tiêu chuẩn) và 4,5 sam H2O (cho H = 1, C = 12, O=16). X, Y có khả năng tác dụng được với dãy chấl nào ừong các dãy chất sau:
Câu 31: Cho các phản ứng:
C2H2 + H2O 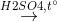 CH3CHO
C2H4+H2
CH3CHO
C2H4+H2 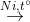 C2H6
CH4 + 2O2
C2H6
CH4 + 2O2 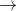 CO2 + 2H2O
3C2H4 + 2KMnO4 + 4H2O
CO2 + 2H2O
3C2H4 + 2KMnO4 + 4H2O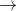 3C2H4(OH)2 + 2MnO2 + 2KOH
Sổ phản ứng oxi hóa - khử là
3C2H4(OH)2 + 2MnO2 + 2KOH
Sổ phản ứng oxi hóa - khử là
Câu 32: Cặp dung dịch nào có khả năng hòa tan Cu(OH)2 ?
Câu 33: Số nguyên tố hóa học có cấu hình electron ngoài cùng 4s2 là
Câu 34: Hấp thụ hoàn toàn 3,36 lít CO2 (điều kiện tiêu chuẩn) vào 500 ml nước vôi trong nồng độ 0,2 M. Dung dịch thu được sau khi lọc bò kết tủa có khối lượng so với dung dịch nước vôi trong ban đầu thay đổi như thế nào? (cho H=1, C=12, O = 16, Ca=40).
Câu 35: Cho hồn hợp gồm FeS và Fe tác dụng với dung dịch HC1 dư, thu được 22.4 lít khí (đktc). Dần hỗn hợp khí này đi qua dung dịch Cu(NO3)2 và Fe(NO3)2 thu được 38,4 gam kết tủa. Khối lượng Fe trong hỗn hợp rắn ban đầu là
Câu 36: Cho 5.76 gam axit hữu cơ đơn chức X tác dụng hết với CaCO3 thu được 7.28gam muối hữu cơ Y (cho H =1, C=12. O =16, Ca = 40). X là
Câu 37: Có các dung dịch: HCl, HNO3, NaOH, AgNO3, NaNO3. Chỉ dùng thêm chất nào sau đây đế phân biệt các dung dịch trên?
Câu 38: Xét các phàn úng sau trong dung dịch nước:
CH3COOH + CaCO3 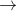 CH3COOH + NaCl
CH3COOH + NaCl 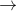 C17H35COONa + H2SO4
C17H35COONa + H2SO4 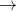 C17H35COONa + Ca(HCO3)2
C17H35COONa + Ca(HCO3)2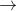 Có bao nhiêu phản ứng không xảy ra?
Có bao nhiêu phản ứng không xảy ra?
Câu 39: Có các cặp dung dịch: a) Glucozơ và glixerol b) GIucozơ và anđehit axctic. c) Saccaroza và mantoza d) Mantoza và fructozơ. Chỉ dùng Cu(OH)2 có thể phân biệt được bao nhiêu cặp chất trên
Câu 40: Bằng một phản ứng trực tiếp từ các chất nào sau đây có thể điều chê được khi NH3?
Câu 41: Có bao nhiêu loại liên kết hidro trong hồn hợp lòng ancol etylic và phenol?
Câu 42: Alcohol nào sau đây khi bị oxi hóa bời dung dịch KMnO4 loãng (trong môi trường H2SO4 loãng, lạnh) sinh ra aldehyde?
Câu 43: Cho vài giọt phenolphtalein vào dung dịch NaOH thấy dung dịch chuyển sang màu hồng, nhò từ từ dung dịch HCl vào cho đến dư thì thấy
Câu 44: Các ion có cùng cấu hình electron: F-, Na+.O2- bán kính giảm dần theo dãy nào sau đây?
Câu 45: Cho 3g hỗn hợp gồm Na và kim loại kiềm M lác dụng hết với nước. Để trung hoà dung dịch thu được cần 800ml dung dịch HCl 0.25M (cho Li = 7, Al= 23, K = 39, Rb = 85,5) Kim loại M là
Câu 46: Cho các cặp chất: 1. NaCl và NaBr 2. NaCl và Nai 3. NaF và NaCl có thể dùng dung dịch AgNO3 để phân biệt cặp hoá chất nào ?
Câu 47: Dung dịch NaHCO3 có lẫn tạp chất là Na2CO3. Bằng cách nào đế loại bỏ lạp chất, thu được NaHCO3 tinh khiết?
Câu 48: Cho hợp chất ion MX3 tổng số các hạt cơ bán là 124, trong MX3 hạt mang điện nhiều hơn hại không mang điện là 36 và MM - MX = 8. Tổng số hạt cơ bản trong X- ít hơn trong M3+ là 8. Vậy M. X là
Câu 49: Cho 0.1 mol chất X (C2H8O3N2)tác dụng với dung dịch chứa 0,2 mol NaOH đun nóng thu được chất khí nặng hơn không khí, làm xanh giấy quỳ tím ẩm và dung dịch Y. Cô cạn dung dịch Y thu được m gam chất rắn khan. Giá trị m là (Cho: H=1, C= 12,N= 14 , O = 16, Na = 23)
Câu 50: Khẳng định nào sau đây là không chính xác?
Câu 51: Khí SO2 do các nhà máy thải ra là nguyên nhân chính gây ô nhiễm môi trường. Tổ chức Y tế thế giới (WHO) quy định nếu lượng SO2 vượt quá 3.10-5 mol/m3 không khí coi như ô nhiễm. Người ta lấy 50ml không khí ở một thành phố vá phân tích thu được 0,012mg SO2. Kết luận nào sau đây là đúng?
Câu 52: ứng dụng nào sau đây không được áp dụng?
Câu 53: Cho 0,1 mol khí co vào bình kín dung tích 1 lít đã có sẵn hơi nước đẻ thực hiện phản ứng sau: CO (khí) + H2O(hơi) 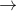 CO2 (khỉ) + H2 (khỉ)
Ờ t°c, hằng số cân bằng của phản ứng: KC = 1. Nếu có 90% CO chuyển hóa thành CO2, thì nồng độ H2O ban đầu là
CO2 (khỉ) + H2 (khỉ)
Ờ t°c, hằng số cân bằng của phản ứng: KC = 1. Nếu có 90% CO chuyển hóa thành CO2, thì nồng độ H2O ban đầu là
Câu 54: Au không bị hoà tan trong trường hợp nào sau đây?
Câu 55: Tại 25°c phản ứng: 2N2O5 (k) ⟶ 4NO2(k) + CO2(k) có hằng số tốc đô k = 1,8.10-5 ; biểu thức tính tốc độ phàn ứng V = k. CN2O5 . Phản ứng trên xảy ra trong bình kín thể tích 20,0 lít không đổi. Ban dầu lượng N2O5 cho vừa đầy bình. Ờ thời điếm khảo sát, áp suất riêng phần N2O5 là 0,070 atm. Các khí đều là lí tưởng. Tốc độ tiêu thụ N2O5 (mol.l-1.s-1) là:
Câu 56: Hình dạng của phân tử CH4, BF3, H2O, BeH2 tương ứng lần lượt là
Câu 57: Trộn 3 dung dịch H2SO4 0,1M; HNO3 0,2M; HCl 0.3M với những thể tích bằng nhau thu được dung dịch A. Lấy 300 ml dung dịch A cho phản ứng với V lit dung dịch B gồm NaOH 0.2M và KOH 0,29M thu được dung dịch có pH=2. Giá trị V là
Câu 58: Nung nóng hoàn toàn 28,9 gam hồn hợp KNO3 và Cu(NO3)2. Hồn hợp khí sinh ra được dẫn vào nước lấy dư thì còn 1,12 lít khí (đktc) không bị hấp thụ (coi oxi không tan trong nước), % khối lượng KNO3 trong hỗn hợp ban đầu là
Câu 59: Ion nào sau đây có 32 electron?
Câu 60: Để nhận biết sản phẩm khi đốt cháy photpho trong bình oxi. có thể dùng cách nào sau đây?
Bạn có đủ giỏi để vượt qua
| Xếp hạng | Thành viên | Đúng | Làm | Đạt | Phút |
| 1 |
|
26 | 50 | 52% | 36.82 |
| 2 |
|
20 | 41 | 49% | 48.32 |
| 3 |
|
0 | 1 | 0% | 1.47 |
| 4 |
|
26 | 60 | 43% | 10.68 |
| 5 |
|
0 | 0 | 0% | 0.6 |
| 6 |
|
1 | 3 | 33% | 7.62 |
| 7 |
|
13 | 50 | 26% | 40.42 |