Đề thi thử đại học môn Hóa - Đề số 6
Thời gian thi : 90 phút - Số câu hỏi : 59 câu - Số lượt thi : 241
Chú ý: Để xem lời giải chi tiết vui lòng chọn "Click vào đề thi"
Một số câu hỏi trong đề thi
Câu 1: Hấp thụ hoàn toàn 6,72 lít CO2 (đktc) vào 750 ml dung dịch chứa đồng thời NaOH 0,1M và Ca(OH)2 0,2M, kết thúc phản ứng thu được m gam kết tủa. Giá trị của m là (Cho Ca = 40, O = 16, H=1, Na = 23,C = 12)
Câu 2: Cho sơ đồ phản ứng:
CH3COOH 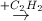 (X)
(X) 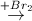 (X1)
(X1) 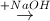 (X2)
(X2)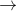 C2H4(OH)2.
Các chất X và X2 lần lượt là
C2H4(OH)2.
Các chất X và X2 lần lượt là
Câu 3: Xét cân bằng sau trong một bình kín: CaCO3 (r) <=> CaO (r) + CO2 (k), ΔH = 178 kJ Ở 820°C hằng số cân bằng Kc = 4,28.10-3. Khi phản ứng đang ờ trạng thái cân bằng, để hằng số cân bằng Kc thay đổi thì ta cần biến đổi một trong những điều kiện nào sau đây?
Câu 4: Thủy phần hoàn toàn 419 gam protein X thu được 234 gam valin. Nếu phân tử khối của X là 4190u thì số mắt xích valin trong phân tử X là (Cho C = 12, O= 16, H = 1, N= 14)
Câu 5: Một loại nước cứng chứa đồng thời Ca(HCO3)2, CaCl2, MgSO4. Để làm giảm tính cứng của loại nước cứng này ta cần dùng thêm hóa chất là
Câu 6: Nhóm các vật liệu được điều chế từ polime tạo ra do phản ứng trùng hợp là
Câu 7: Cho các nguyên tử và ion: V (Z = 23), Cr2+ (Z = 24), Ni2+ (Z = 28), Fe3+ (Z = 26), Mn2+ (Z = 25). sổ lượng nguyên tử và ion có cùng cấu hinh electron là
Câu 8: Hòa tan hết 20,6 gam Cr(OH)3 trong 500 ml dung dịch HC1 2M đun nóng, thu được dung dịch X. Khối lượng Zn phản ứng vừa hết các chất trong dung dịch X là (Cho Cr = 52, Zn = 65, O= 16, H=1)
Câu 9: Hỗn hợp X gồm hai hiđrocacbon mạch hở X1 và X2 có cùng số nguyên tử cacbon. Tỉ khối của X so với H2 là 21. Công thức phân từ của X1 và X2 lần lượt là (Cho C= 12, O= 16, H= 1)
Câu 10: Hòa tan hỗn hợp chửa đồng thời 0,15 mol mỗi kim loạiFe và Cu trorg 675 ml dung dịch AgN03 1M, khối lượng chất rắn thu được khi kết thúc phản ứng là (Cho Fe = 56, Cu = 64,O = 16, Ag = 108, H=1,N= 14)
Câu 11: Đốt cháy hoàn toàn m gam hỗn hợp X gồm hai anđehit X1, X2: (Mx1 <MX2 ) cùng dãy đồng đắng liên tiếp rồi cho toàn bộ sản phẩm cháy vào bình đựng dung dịch Ba(OH)2 (dư) thấy có 49,25 gam kết tủa xuất hiện và khối lượng dung dịch này giảm 33,75 gam so với ban đầu. Mặt khác, nêu cho m gam X tác dụng với lượng dư dung dịch AgNO3 trong NH3 thì thu được 43,2 gam kêt tủa bạc. Phần trăm khối iượng của X1 trong hồn hợp X là (Cho C = 12, O = 16. H = 1, Ba = 137, Ag = 108)
Câu 12: Hợp chất không phải là chất lưỡng tính là
Câu 13: X là hỗn hợp của SO2 và O2, cỏ tỉ khối so với H2 là 22,4. Nung nóng X một thời gian trong bình kín có chất xúc tác thích hợp, thu được hỗn hợp khí có tỉ khối so với H2 là 26,67. Hiệu suất của phản ứng tổng hợp SO3 là (Cho S = 32, O = 16,H=1)
Câu 14: Một dung dịch chứa 0,02 mol Fe(NO3)3 và 0,3 mol HCl. Dung dịch này có khả năng hòa tan tối đa số gam Cu là (Cho Cu = 64)
Câu 15: Khẳng định không đủng là
Câu 16: Cation M3+ có cấu hình electron ngoài cùng là 2p6. Khi cho dung dịch MCl3 vào các ống nghiệm đựng lượng dư các dung dịch: Na2CO3, NaOH, NH3, Na2SO4. Số ống nghiệm sau phản ứng có kết tủa hiđroxit là
Câu 17: Dãy các kim loại đều có thể điều chế bằng phương pháp thủy luyện là
Câu 18: Hợp chất khi tác dụng với nước không tạo ancol etylic là
Câu 19: Khẳng định nào sau đây là sai?
Câu 20: Hợp chẩt hữu cơ X chứa chức ancol và anđehit. Đốt cháy X thu được số mol CO2 bằng số mol H2O. Nếu cho m gam X phản ứng với Na thu được V lít khí H2, còn nếu cho m gam X phản ứng hết với H2 thì cần V lít H2 (các thể tích khi đo ở cùng điều kiện nhiệt độ và áp suất). Công thức phân tử của X có dạng:
Câu 21: Đốt cháy hoàn toàn m gam hỗn họp gồm hai este X1, X2 là đồng phân của nhau cần dùng 19,6 gam O2, thu được 11,76 lít CO2 (đktc) và 9,45 gam H2O khác, nếu cho m gam hỗn hợp trên tác dụng hết với 200 ml dung dịch NaOH 1M cô cạn dung dịch thu được sau phản ứng thì còn lại 13,95 gam chất rẳn khan. Biết axit của X2 có số nguyên tử cacbon lớn hơn gốc axit của X1. Ti lệ mol của X1 và X2 trong hỗn hợp trên lần lượt là (Cho C= 12, O= 16, H = 1, Na= 23)
Câu 22: Phản ứng không dùng để điều chế chất khí trong phòng thí nghiệm là
Câu 23: Cho 18,1 gam axit 2-amino-ß-(p-hidroxi phenyl)propanoic (tyrosin) tác dụng với 150ml dung dịch HCl 1M thu được dung dịch X. Cho dung dịch X tác dụng với 400ml dung dịch NaOH 1M, từ dung dịch sau phản ứng thu được m gam chất rắn khan. Giá trị của m là (Cho Cl = 35,5, O= 16, H = 1,N=14,Na = 23, O = 12)
Câu 24: Dãy gồm các phân tử có cùng bản chất liên kết là:
Câu 25: Cho sơ đồ phản ứng:
CrO3 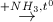 (X)
(X) 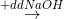 (X1)
(X1) 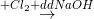 (X2)
(X2) 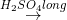 (X3)
Các chất X1, X2 lần lượt là
(X3)
Các chất X1, X2 lần lượt là
Câu 26: Hỗn hợp chứa đồng thời X mol mỗi chất Fe3O4, Cu, Al, NaCl có thể tan hoàn toàn trong lượng dư dung dịch nào sau đây?
Câu 27: Dung dịch X chứa HCl có pH = 2. Cho 0,2 lít dung dịch AgNO3 1M vào 0,5 lít dung dịch X thu được khối lượng kết tủa là (Cho Cl = 35,5, Ag = 108)
Câu 28: Tiến hành phản ứng nhiệt nhôm vói Fe3O4 trong điều kiện không có không khí, cho biết phản ứng xảy ra hoàn toàn và Fe3O4 chỉ bị khử thành Fe. Chia hỗn hợp thu được sau phản ứng thành hai phần bằng nhau. Cho phần 1 tác dụng hết với dung dịch NaOH (dư) thu được 2,52 lít H2 (đktc). Hoà tan hết phần 2 bằng dung dịchHNO3 đặc, nóng (dư) thấy có 11,76 lít khí bay ra (đktc). Khối lượng Fe sinh ra sau phản ứng nhiệt nhôm là (Cho Fe = 56,O = 16,H =1,Al = 23, Na = 23)
Câu 29: Cho các phản ứng sau:
(1) Ca(OH)2 + Cl2 → CaOCl2 + H20
(2) C2H5Cl + NaOH → C2H5OH + NaCl
(3) 2KMn04 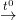 K2MnO4 + MnO2 + O2↑
(4) C2H2 + H2O
K2MnO4 + MnO2 + O2↑
(4) C2H2 + H2O 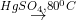 CH3CHO
Các phản ứng thuộc loại phản ứng tự oxi hóa - khử là
CH3CHO
Các phản ứng thuộc loại phản ứng tự oxi hóa - khử là
Câu 30: Cho 7,8 gam Zn tan hết trong dung dịch HNO3 thu được V lít khí duy nhất là N2O (đktc). Lấy dung dịch còn lại làm bay hơi từ từ thu được 23,8 gam chất rắn khan. Giá trị của V là (Cho N = 14, O= 16, H= 1, Zn = 65)
Câu 31: Thực hiện phản ứng xà phòng hóa giữa 0,1 mol một este đơn chức X với 200ml dung dịch NaOH 1M thu được 8,8 gam ancol và dung dịch chứa 12,2 gam chất tan. Este X có tên gợi là {Cho H = 1, C= 12, O = 16)
Câu 32: Biết rằng 5,688 gam poli(butađien-stiren) phản ứng vừa hết 3,462 gam brom trong CCl4. Tì lệ số mắt xích butađien, stiren trong polime này lần lượt là {Cho C = 12, H = 1, Br= 80)
Câu 33: Dung dịch X chứa đồng thời các ion: Mg2+, Ba2+, Ca2+, 0,1 mol Cl- và 0,2 mol NO3-. Thêm từ từ dung dịch Na2SO3 0,5 M vào dung dịch X đến khi lượng kết tủa lớn nhất thi thể tích dung dịch Na2SO3 đã cho vào là
Câu 34: Có thể pha chế một dung dịch chứa đồng thời các ion
Câu 35: Đốt cháy hoàn toàn một amin no, đơn chức X thì sinh ra 17,6 gam CO2 và 9,9 gam H2O. Số lượng amin đồng phân cấu tạo ứng với công thức phân tử của X là (Cho C=12, O = 16, H=1,N= 14)
Câu 36: Nhỏ từ từ cho đến hết 400ml dung dịch HCl1M vào 200ml dung dịch chứa đồng thời Na2CO31M và NaHCO31M, kết thúc phản ứng thu được V lít CO2(đktc).Giá trị của V là (Cho C = 12, O = 16, H= 1, Na = 23, Cl= 35,5)
Câu 37: Nung 34,6 gam hỗn hợp gồm Ca(HCO3)2, NaHCO3, KHCO3, thu được 3,6 gam H2O và m gam hỗn hợp các muối cacbonat. Giá trị của m là (Cho Ca = 40, C = 12,H=1,Na = 23, K = 39,O = 16)
Câu 38: Có 6 chất lỏng: axit fomic, axit acrylic, axit axetic, xiclohexen, benzen và anilin. Thuốc thử để phân biệt các chất lỏng này là
Câu 39: SO2 bị khử bởi
Câu 40: Chia 31,2 gam hỗn hợp X gồm Cr, Zn, Ni và Al thành hai phần bằng nhau. Hòa tan hết phần 1 trong lượng dư dung dịch HCl loãng nóng thu được 7,28 lít H2 (đktc). Cho phần 2 tác dụng với khí Cl2(dư) đốt nóng, thu được 42,225 gam muối clorua. Phần trăm khối lượng của Cr trong hỗn hợp X là {Cho Cr= 52, Al = 27,Ni = 58, Zn = 65, Cl = 35,5, H = 1)
Câu 41: Cho dãy aminoaxit: glyxin, alanin, valin. số tripeptit chứa cả 3 amino axit trong dãy là
Câu 42: Cho hỗn hợp khí CO và H2 đi qua hỗn hợp bột gồm các oxit: Al2O3, CuO, Fe2O3, Ag2O đốt nóng, sau một thời gian thu được chất rắn khan có khối lượng giảm 4,8 gam so với ban đầu. Hòa tan toàn bộ lượng chất rắn này bằng dung dịch HNO3 loãng (dư) sinh ra V lít NO (sản phẩm khử duy nhất, đktc). Giá trị của V là (Cho Al = 27, Zn = 65, Cu = 64, Ag = 108, Fe = 56, H= 1, O = 16, N= 14)
Câu 43: Đun nóng m gam ancol đơn chức trong bình đựng CuO (dư), đốt nóng. Sau khi ancol phản ứng hết thu được 0,896 lít hỗn hợp hơi (ở 127°C và 1,4645at) có tỉ khối hơi so với H2 là 15,5. Giá trị của m là (Cho C = 12, H = 1, O 16)
Câu 44: Điện phân với điện cực trơ (hiệu suất 100%) dung dịch chứa đồng thời 0,04 mol FeNO3 và 0,02 mol HNO3 cường độ 1A. Sau 48 phút 15 giây thì ngừng điện phân. Để yên bình điện phân để các phản ứng xảy ra hoàn toàn được 200 ml dung dịch có pH là (Cho Cu = 64, Fe = 56, O = 16, H=1).
Câu 45: Có các dung dịch không màu: NaCl. K2CO3, Na2SO4, HCl, Ba(NO3)2 dựng trong các lọ riêng biệt. Không dùng thêm hóa chất bên ngoài có thể phân biệt được tối đa bao nhiêu dung dịch trong số các dung dịch trên?
Câu 46: Đốt cháy hoàn toàn hỗn hợp X gồm 3 axit cacboxylic X1, X2, X3 liên tiếp nhau trong cùng dãy đồng đẳng cần dùng 19,6 lít O2(đktc) thu được 33 gam CO2 và 13,5 gam H2O. Khẳng định nào sau đây là không hoàn toàn đúng? (Cho C = 12, O = 16, H = 1)
Câu 47: Tổng số liên kết đơn trong phân tử ankađien có công thức chung CnH2n-2 là
Câu 48: Có các chất khí: NO2, Cl2, CO2, SO2, SO3, HCl. Những chất khí khi tác dụng với dung dịch NaOH xảy ra phản ứng oxi hóa — khử là
Câu 49: Cho phenol tác dụng với anhiđrit axetic thu được m gam phenyl axetat, để trung hòa axit axetic lạo ra sau phản ứng cần 2 lít dung dịch NaOH 1M. Giá trị của m là (Cho H=1, C=12, O=16)
Câu 50: Trong nước thải của một nhà máy có chứa các ion: Cu2+, Zn2+', Fe3+, Pb2+, Hg2+. Có thể dùng chất nào sau đây để xử lí sơ bộ nước thải trên?
Câu 51: Trong cơ chế của phản ứng nitro hóa vòng benzen (xúc tác là: H2SO4 độc) thì phân tử hay ion nào sau đây tấn công trực tiếp vào vòng benzen?
Câu 52: Cho dãy các chất: benzen, benzandehit, axeton, glucoza, mantoza. saccarozơ, fructozơ, axit oleic, số chất trong dãy làm mất màu nước brom là
Câu 53: Cho biết suất điện động của pin 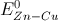 = 1,10V và
= 1,10V và 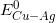 = 0,46V
Suất điện động chuẩn của pin điện hoá được ghép bới 2 cặp oxi hóa - khứ chuẩn Ag+/Ag; Zn2+/Zn là:
= 0,46V
Suất điện động chuẩn của pin điện hoá được ghép bới 2 cặp oxi hóa - khứ chuẩn Ag+/Ag; Zn2+/Zn là:
Câu 54: Một pin điện hóa gồm điện cực là sợi dây bạc nhúng vào dung dịch AgNO3 và điện cực kia là một sợi dây platin nhúng vào dung dịch chứa đồng thời Fe(NO3)3 và Fe(NO3)2. Phản ứng xảy ra ở điện cực dương của pin điện hóa (ở điều kiện chuẩn) là (Cho 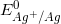 = + 0,8 V;
= + 0,8 V; 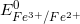 = + 0,77 V)
= + 0,77 V)
Câu 55: Đun nóng axit axeticvới rượu iso-amylic có H2SO4 đặc xúc tác thu được dầu chuối. Biết hiệu suất phản ứng đạt 68%. Lượng dầu chuối thu được từ 132,35 gam axit axetic đun nóng với 200 gam rượu iso-amylic là
Câu 56: Cho 100ml dung dịch hỗn hợp CuSO41M và Al2(SO4)3 IM tác dụng với dung dịch NH3 dư, lọc lấy kết tủa đem nung đến khối lượng không đổi thu được chất rắn có khối lượng là
Câu 57: Cho biết thế diện hoá chuẩn của các cặp oxi hoá khử Mg2+/Mg; Zn2+/Zn; Cu2+ /Cu; Ag+/Ag lần lượt là: - 2,37V; - 0,76V; 0,34V; 0,8V. E°pin= 2.71V là suất điện động chuẩn của pin điện hoá nào trong số các pin sau;
Câu 58: Để pha chế 1 lít dung dịch hỗn hợp Na2SO4 0,03M; K2SO4 0,02M; KCl 0,06M người ta đã lấy lượng các muổi như sau:
Câu 59: Cho 13,7 gam kim loại Ba vào 200ml dung dịch FeSO41M, sau khi các phản ứng xảy ra hoàn toàn, thu được kết tủa có khối lượng là (cho Fe = 56, Ba= 137, S = 32, O = 16, H= 1)
Bạn có đủ giỏi để vượt qua
| Xếp hạng | Thành viên | Đúng | Làm | Đạt | Phút |
| 1 |
|
41 | 46 | 89% | 83.73 |
| 2 |
|
29 | 50 | 58% | 67.2 |
| 3 |
|
23 | 47 | 49% | 6.42 |
| 4 |
|
21 | 41 | 51% | 66.32 |
| 5 |
|
13 | 46 | 28% | 52.2 |
| 6 |
|
0 | 0 | 0% | 0.15 |
| 7 |
|
0 | 1 | 0% | 1.25 |