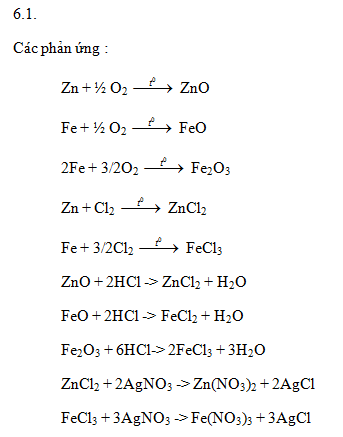(2,25 điểm): 6.1. Đốt cháy hoàn toàn hỗn hợp gồm 5,2g Zn và 4,48g Fe với lượng vừa đủ hỗn
(2,25 điểm):
6.1. Đốt cháy hoàn toàn hỗn hợp gồm 5,2g Zn và 4,48g Fe với lượng vừa đủ hỗn hợp khí X gồm Cl2 và O2, sau phản ứng chỉ thu được hỗn hợp Y gồm các oxit và muối clorua. Hòa tan Y bằng một lượng vừa đủ 120 ml dung dịch HCl 2M, thu được dung dịch Z. Cho AgNO3 dư vào dung dịch Z thu được 56,69g kết tủa.
Viết các phương trình hóa học xảy ra và tính phần trăm theo thể tích khí O2 trong X.
6.2. Trong các hang động như động Hương Tích (Chùa Hương) , động Thiên Cung, hang Đầu Gỗ (Vịnh Hạ Long), động Phong Nha, Hang Sơn Đoòng (Quảng Bình) và các hang động ở nhiều địa phương khác có nhiều thạch nhũ hình dáng khác nhau, trông lạ mắt và rất đẹp. Thạch nhũ được hình thành qua quá trình biến đổi liên tục và lâu dài.
Bằng kiến thức hóa học của mình, em hãy giải thích ngắn gọn sự hình thành thạch nhũ trong các hang động trên.
b. Khi dẫn từ từ đến dư khí CO2 vào một cốc đựng dung dịch Ca(OH)2 , kết quả thí nghệm được biểu diễn trên đồ thị sau :
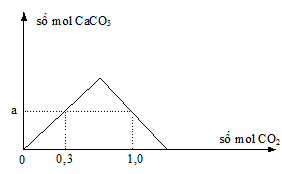
Dựa vào đồ thị , khi lượng CO2 đã dẫn vào dung dịch là 0,85 mol thì lượng kết tủa xuất hiện tương ứng là bao nhiêu gam?
Quảng cáo
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com