Hòa tan m gam hỗn hợp gồm Na, Ba, Na2O và BaO vào lượng dư H2O, thu được dung dịch X (có chứa 0,4
Hòa tan m gam hỗn hợp gồm Na, Ba, Na2O và BaO vào lượng dư H2O, thu được dung dịch X (có chứa 0,4 mol NaOH và 4,48 lít H2 (đktc). Dẫn từ từ khí CO2 vào X, kết quả thí nghiệm được ghi ở bảng sau:
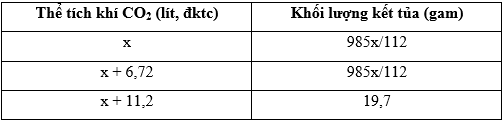
Giá trị gần nhất của m là
Đáp án đúng là: C
Quảng cáo
Đặt a = x/22,4 (nCO2)
TN1: nCO2 = a (mol); nBaCO3 = \(\dfrac{{985x}}{{112.197}} = \dfrac{x}{{22,4}} = a\)(mol)
TN2: nCO2 = a + 0,3 (mol) ; nBaCO3 = \(\dfrac{{985x}}{{112.197}} = \dfrac{x}{{22,4}} = a\)(mol)
TN3: nCO2 = a + 0,5 (mol); nBaCO3 = 19,7/197 = 0,1 mol
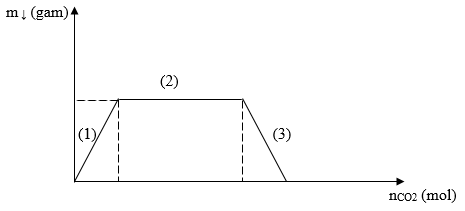
*Dùng đồ thị bài toán CO2 + dung dịch hỗn hợp Ba(OH)2/NaOH để đánh giá:
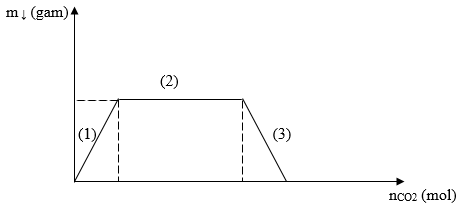
Chia đồ thị thành 3 giai đoạn:
Giai đoạn 1: CO2 + Ba(OH)2 → BaCO3 ↓ + H2O
Giai đoạn 2: CO2 + NaOH → NaHCO3
Giai đoạn 3: CO2 + BaCO3 ↓+ H2O → Ba(HCO3)2
Ở TN1 và TN2 với 2 giá trị nCO2 đều cho cùng một lượng kết tủa; và nBaCO3 = nCO2 (1)
⟹ Cả hai giá trị nCO2 = a (mol) và nCO2 = a + 0,3 (mol) đều nằm ở gđ 2
Khi đó nBaCO3 = a (mol) sẽ là kết tủa cực đại
⟹ nBa(OH)2 = nBaCO3
- Xét TN3:
BTNT Ba: nBa2+ = nBa(OH)2 – nBaCO3
BTNT C: nHCO3- = nCO2 – nBaCO3
Dung dịch X chứa các ion: \(\left\{ \begin{array}{l}B{a^{2 + }}\\N{a^ + }\\HCO_3^ - \end{array} \right.\)
BTĐT trong dung dịch X ⟹ Giá trị của a.
- Quy đổi hỗn hợp ban đầu thành: Na; Ba; O
Các quá trình nhường nhận electron khi hòa tan hỗn hợp vào nước:
Na – 1e → Na+ O0 + 2e → O-2
Ba – 2e → Ba+2 2H+ + 2e → H2
Bảo toàn electron ⟹ 2nO + 2nH2 = nNa + 2nBa ⟹ nO ⟹ m = mNa + mBa + mO
Đáp án cần chọn là: C
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com