Các loại hợp chất vô cơ
X là dung dịch AlCl3, Y là dung dịch NaOH 2M. Thêm 150ml dung dịch Y vào cốc chứa 100ml dung dịch X, khuấy đều thì trong cốc tạo ra 7,8 gam kết tủa. Lại thêm tiếp vào cốc 100ml dung dịch Y, khuấy đều thì lượng kết tủa có trong cốc là 10,92 gam. Các phản ứng đều xảy ra hoàn toàn. Hãy xác định nồng độ mol của dung dịch X?
Đáp án đúng là: C
Quảng cáo
Đáp án cần chọn là: C
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com . Học online tại nhà cũng giáo viên giỏi từ trường TOP đầu cả nước. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. Phụ huynh và học sinh tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com



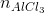 = 0,1.x = 0,1x mol
= 0,1.x = 0,1x mol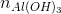 =
= 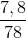 = 0,1 mol
= 0,1 mol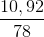 = 0,14 mol
= 0,14 mol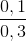 . 0,2 = 0,0667 mol > 0,04 mol
. 0,2 = 0,0667 mol > 0,04 mol







