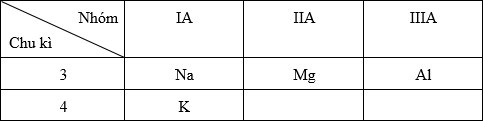
Cho các nguyên tố 11Na, 19K, 13Al, 12Mg. Chiều tăng dần tính kim loại của chúng
Cho các nguyên tố 11Na, 19K, 13Al, 12Mg. Chiều tăng dần tính kim loại của chúng là
Đáp án đúng là: B
Quảng cáo
- Từ Z → Cấu hình e → Vị trí trong BTH.
- Từ vị trí so sánh được tính kim loại của các nguyên tố:
+ Trong cùng một chu kì, theo chiều tăng của điện tích hạt nhân thì tính kim loại giảm dần.
+ Trong cùng một nhóm A, theo chiều tăng của điện tích hạt nhân thì tính kim loại tăng dần.
Đáp án cần chọn là: B
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com