Một hệ gồm nAO (n =2; 3; …) của cùng một nguyên tử, có thể tổ hợp với nhau để tạo ra hệ
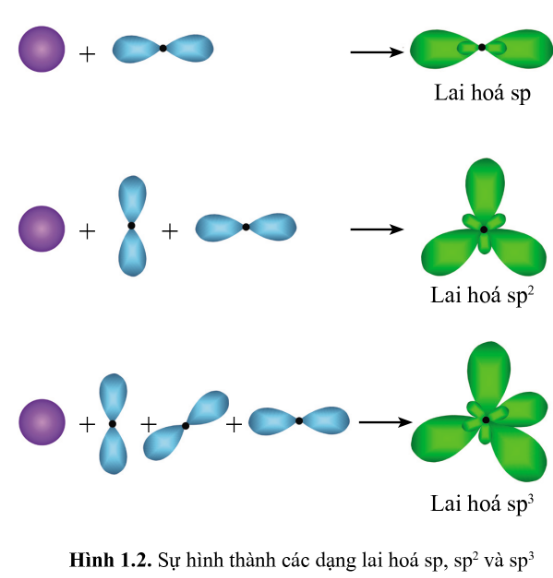
Một hệ gồm nAO (n =2; 3; …) của cùng một nguyên tử, có thể tổ hợp với nhau để tạo ra hệ n orbital mới (gọi là orbital lai hoá) có hình dạng như nhau, nhưng có định hướng không gian phù hợp với sự hình thành liên kết và dạng hình học phân tử tương ứng. Lai hoá là sụ tổ hợp các orbital của cùng nguyên tư để tạo ra các orbital mó́i có cùng dạng hình học và năng luợng nhưng có định huớng khác nhau trong không gian. Sự lai hoá thường chỉ xét với nguyên tử trung tâm.
Trả lời cho các câu 1, 2, 3, 4 dưới đây:
Lai hoá là sự tổ hợp các orbital thuộc các nguyên tử khác nhau để tạo thành các orbital lai có năng lượng và định hướng giống nhau.
Đáp án đúng là: B
Khái niệm lai hóa.
Đáp án cần chọn là: B
Tại sao các orbital cần lai hóa trước khi xen phủ tạo liên kết?
Đáp án đúng là: D
Hiểu bản chất của lai hoá: tạo điều kiện hình thành liên kết hoá học thuận lợi.
Đáp án cần chọn là: D
Cho biết các phát biểu sau về oribital lại hóa đúng hay sai?
| Đúng | Sai | |
|---|---|---|
| a) Lai hoá chỉ xảy ra giữa các orbital thuộc nguyên tử trung tâm. | ||
| b) Sau khi lai hoá, các orbital mới có năng lượng giống hệt nhau. | ||
| c) Các orbital lai hoá có định hướng không gian khác nhau nhưng hình dạng hoàn toàn khác nhau. | ||
| d) Số orbital lai hoá tạo thành luôn bằng số orbital tham gia lai hoá ban đầu. |
Đáp án đúng là: Đ; Đ; S; Đ
Ý nghĩa lai hóa orbital.
Đáp án cần chọn là: Đ; Đ; S; Đ
Một nguyên tử thực hiện lai hoá giữa 1 orbital s và 2 orbital p để tạo thành 3 orbital lai hoá có cùng hình dạng và định hướng phù hợp trong không gian. Quá trình lai hoá này được gọi là lai hoá_______
Đáp án đúng là: sp2
Tính số AO tham gia (1s + 2p = 3 AO), từ đó xác định tên loại lai hoá tương ứng.
Đáp án cần điền là: sp2
Quảng cáo
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











