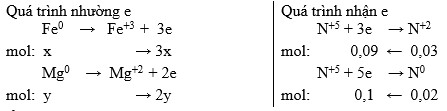Hoà tan 2,64 gam hỗn hợp Fe và Mg bằng dung dịch HNO3 loãng, dư, thu được sản phẩm khử là
Hoà tan 2,64 gam hỗn hợp Fe và Mg bằng dung dịch HNO3 loãng, dư, thu được sản phẩm khử là 0,896 lít (đktc) hỗn hợp khí gồm NO và N2, có tỷ khối so với H2 bằng 14,75. Thành phần % theo khối lượng của sắt trong hỗn hợp ban đầu là
Đáp án đúng là: C
Quảng cáo
- Xác định sự thay đổi số oxi hóa của một số nguyên tố: Fe0 → Fe+3; Mg0 → Mg+2; N+5 → N+2 + N0.
- Giải hệ phương trình tìm số mol mỗi khí.
- Viết quá trình trao đổi electron, áp dụng phương pháp bảo toàn electron, giải hệ phương trình tìm số mol mỗi kim loại.
- Chú ý: trong một phân tử N2 có hai nguyên tử N0.
Đáp án cần chọn là: C
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com