Axit hữu cơ, este và tác nhân phản ứng
Axit hữu cơ, este và tác nhân phản ứng
Trả lời cho các câu 1, 2 dưới đây:
Axit X (chỉ chứa C, H, O trong phân tử) là một hợp chất hữu cơ sinh học. Khi vận động mạnh trong một thời gian dài và cơ thể không được cung cấp đủ oxi, glucozơ trong cơ thể sẽ bị chuyển hóa thành axit X. Axit X sinh ra trong quá trình vận động là nguyên nhân chính tạo ra cảm giác mỏi ở cơ bắp. Axit X cũng có mặt trong sữa chua và dưa muối.
a) Bằng phương pháp phổ khối lượng MS, người ta xác định được phân tử khối của X là 90. Bằng các phương pháp phổ hiện đại khác như phổ hồng ngoại IR và phổ cộng hưởng từ hạt nhân NMR, người ta xác định được phân tử của X chứa nhóm chức -OH và –COOH cùng liên kết với một nguyên tử cacbon. Xác định công thức phân tử và công thức cấu tạo của axit X.
b) Nêu một biện pháp đơn giản giúp vận động viên giảm cảm giác mỏi cơ do axit X bị tích tụ nhiều
trong quá trình tập luyện thể thao.
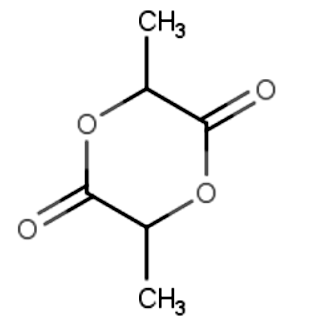
c) Để axit X trong bình phản ứng, cho thêm vài giọt axit sunfuricđặc (làm xúc tác), rồi đun nóng. Sau một thời gian, thu được hỗn hợp các chất, trong đó có hợp chất hữu cơ Y. Trong phân tử Y, nguyên tố oxi chiếm 44,44% về khối lượng và phân tử khối của Y khoảnh từ 75 đến 150 . Xác định công thức phân tử, công thức cấu tạo của Y. Viết phương trình hóa học của phản ứng tạo ra chất Y.
Dựa vào lý thuyết về axit.
Chất Z là một tác nhân hóa học được dùng nhiều trong tổng hợp hữu cơ.
a) Bằng phương pháp phân tích nguyên tố người ta xác định được thành phần phần trăm về khối lượng của N và H trong Z lần lượt là 87,5% và 12,5%. Do điều kiện thí nghiệm không đầy đủ nên người ta chỉ xác định được phân tử khối của Z năm trong khoảng 30 đến 40. Việt công thức cấu tạo của chất Z.
b) Biết chất Z có tính khử, viết phương trình hóa học xảy ra khi cho Z phản ứng với Cl2.
c) Ngoài việc thu được chất Y khi nhỏ axit sunfuric vào axit X (trong Câu 5.1, ý c ở trên), người ta còn thu được chất hữu cơ T. Quá trình hình thành và chuyển hóa T (có sử dụng tác nhân Z) thành chất hữu cơ Q như sau:
$X\xrightarrow[{ - {H_2}O}]{{{H_2}S{O_4},{t^0}}}T\xrightarrow[{ - {H_2}O}]{{C{H_3}OH/{H_2}S{O_4}}}P\xrightarrow[{ - C{H_3}OH}]{Z}Q$%
Dự đoán công thức cấu tạo của chất T, P và Q biết trong phân tử của Q, N chiếm 32,56% về khối lượng.
Dựa vào tính chất hóa học của các chất.
Quảng cáo
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com . Học online tại nhà cũng giáo viên giỏi từ trường TOP đầu cả nước. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. Phụ huynh và học sinh tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com