Trả lời cho các câu 1, 2, 3, 4 dưới đây:
Cho cấu tạo lớp vỏ electron của nguyên tử thuộc các nguyên tố kí hiệu X1, X2, X3, X4, X5 như sau:
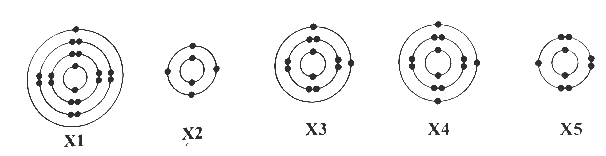
Trong số các nguyên tố trên, hãy cho biết:
a) Nguyên tố nào thuộc nhóm II của bảng tuần hoàn các nguyên tố hóa học?
b) Nguyên tố nào có 13 proton ở hạt nhân nguyên tử?
c) Nguyên tố nào phản ứng với kim loại kiềm theo tỉ lệ mol 1:1?
d) Nguyên tố nào ở chu kỳ 4, nhóm I.
Dựa vào lý thuyết cấu tạo nguyên tử.
Viết các phương trình phản ứng xảy ra trong các thí nghiệm sau:
a) Cho dung dịch Na2CO3 vào dung dịch AlCl3, thu được kết tủa màu rắng và có khí thoát ra.
b) Hòa tan hoàn toàn MgO trong dung dịch NH4Cl đặc thấy thoát ra khí mùi khai.
Dựa vào tính chất hóa học của các chất.
Trình bày phương pháp hóa học để làm sạch:
a) Khí CO2 có lẫn SO2.
b) Khí H2S có lẫn tập chất HCl.
Dựa vào tính chất hóa học của các chất.
Tinh thể muối ngậm nước FeSO4.xH2O được điều chế bằng cách cho lượng dư muối sắt (II) cacbonat phản ứng với dung dịch axit sunfuric loãng theo qui trình sau: Thêm từng lượng nhỏ sắt (II) cacbonat đến dư vào dung dịch axit sunfuric loãng. Sau đó, lọc hỗn hợp phản ứng để thu lấy dung dịch. Đun nóng dung dịch đến khi thu được dung dịch bão hoà rồi để nguội. Lọc thu lấy tinh thể chất rắn và thẩm khô bằng giấy lọc.
a) Tại sao phải dùng lượng dư sắt (II) cacbonat?
b) Hãy chỉ ra dấu hiệu cho thấy lượng sắt (II) cacbonat đã dư.
c) Hãy cho biết hoá chất nào có thể thay thế sắt (II) cacbonat trong quy trình trên.
d) Biết Fe chiếm 20,14 % khối lượng của FeSO4. xH2O. Hãy xác định x.
Dựa vào tính chất hóa học của các chất.
Quảng cáo
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com . Học online tại nhà cũng giáo viên giỏi từ trường TOP đầu cả nước. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. Phụ huynh và học sinh tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











