Câu 5 (TH): 2 điểm 1. Chất rắn A có sẵn trong tự nhiên dưới dạng nhiều khoáng khác nhau. Nung
Câu 5 (TH): 2 điểm
1. Chất rắn A có sẵn trong tự nhiên dưới dạng nhiều khoáng khác nhau. Nung nóng A ở 1100 0C là phương pháp để sản xuất lượng lớn chất B. Cho B phản ứng với nước sẽ được chất C và tỏa nhiều nhiệt. Trong phòng thí nghiệm, dung dịch nước của C được dùng để phát hiện khí D. Khí D được sử dụng trong rất nhiều loại nước giải khát.
a. Viết các phản ứng thể hiện những biến đổi hóa học trên.
b. Khí D có duy trì sự cháy không? Cho ví dụ cụ thể.
c. Thay vì sử dụng đá để bảo quản thực phẩm, người ta sử dụng chất D ở thể rắn – “Nước đá khô” để bảo quản thực phẩm. Cho biết lợi ích của việc làm này.
2. Khí D trong câu 5.1 ở trên có nhiều ứng dụng trong công nghiệp, một trong số đó là điều chế muối E (không bền) theo phương pháp Solvay : cho một lượng bằng nhau về số mol của NH3 và khí D sục qua dung dịch natri clorua (nước biển) ở nhiệt độ thấp. Sản phẩm tạo thành ngoài muối E còn có muối amoni clorua NH4Cl. Do ít tan ở nhiệt độ thấp nên muối E sẽ kết tủa.
a. Viết phương trình phản ứng điều chế muối E theo phương pháp Solvay.
b. Một dung dịch muối E được trộn với dung dịch HCl có cùng khối lượng. Khối lượng của hỗn hợp sau phản ứng giảm 10% so với tổng khối lượng dung dịch ban đầu. Tính nồng độ phần trăm sản phẩm tạo thành trong dung dịch cuối.
3. Nhiên liệu luôn là vấn đề có tính thời sự trên toàn cầu.Các nhiên liệu hóa thạch như than đá, dầu mỏ đóng vai trò không thể thiếu trong cuộc sống hằng ngày. Tuy nhiên do có nhiều hạn chế nên hiện nay các nhà khoa học đang tập trung nghiên cứu dùng hidro làm nhiên liệu. Mặc dù việc điều chế và bảo quản hidro gặp nhiều khó khăn nhưng đây vẫn là hướng phát triển mạnh ở thời điểm hiện tại.
a. Cho biết những hạn chế của việc sử dụng nhiên liệu hóa thạch.
b. Tại sao dùng khí hidro làm nhiên liệu lại được đưa vào nghiên cứu.
c. Viết 2 phương trình hóa học điều chế khí hidro trong phòng thí nghiệm.
Quảng cáo
1.Dựa vào đặc điểm đặc trung của khí CO2 và điều chế Na2CO3 bằng phương pháp Solvay.
2.
b) Giả sử dung dịch muối NaHCO3 và HCl cùng khối lượng là 50g
mdung dịch giảm = mCO2 = 10%.(50 + 50) = 10g => nCO2 = ? mol
Phản ứng : NaHCO3 + 2HCl NaCl + CO2 + H2O
Mol ? ¬ ?
=> C%NaCl
3. Lý thuyết về Hóa học và các vấn đề môi trường. Hidrocacbon.
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com



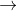 C và tỏa nhiều nhiệt => B là CaO
C và tỏa nhiều nhiệt => B là CaO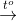 CaO + CO2
CaO + CO2







