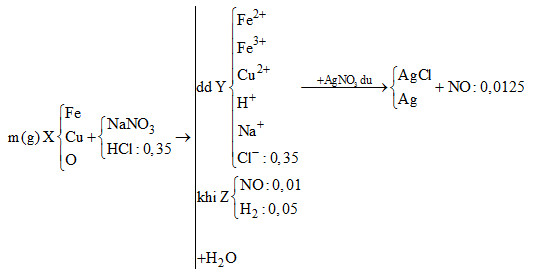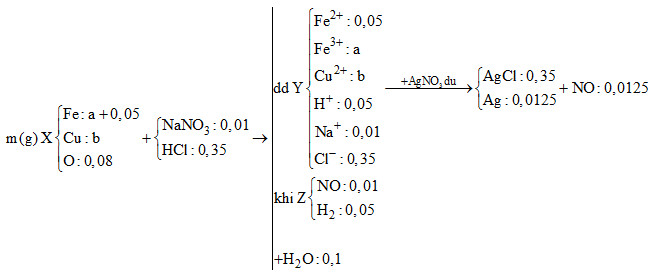Hòa tan hoàn toàn m gam hỗn hợp X gồm Fe, Cu và oxit sắt bằng hỗn hợp dung dịch chứa NaNO3 và
Hòa tan hoàn toàn m gam hỗn hợp X gồm Fe, Cu và oxit sắt bằng hỗn hợp dung dịch chứa NaNO3 và 0,35 mol HCl, thu được dung dịch Y và 1,344 lít hỗn hợp khí Z có tỉ khối so với hiđro là 20/6. Cho dung dịch AgNO3 dư vào dung dịch Y trên thì thu thêm được 0,28 lít NO ở đktc và 51,575 gam kết tủa. Nếu lấy 61 gam hỗn hợp X thì có thể điều chế tối đa 53 gam kim loại. Phát biểu nào sau đây đúng? (Biết NO là sản phẩm khử duy nhất của N+5 trong toàn bộ bài toán).
Đáp án đúng là: C
Quảng cáo
Do khi thêm dung dịch AgNO3 dư vào Y thu được khí NO nên trong Y có chứa Fe2+ và H+, không chứa NO3-
Áp dụng các định luật bảo toàn khối lượng, bảo toàn nguyên tố, bảo toàn e để tính được số mol của các ion.
Đáp án cần chọn là: C
>> 2K8 Chú ý! Lộ Trình Sun 2026 - 3IN1 - 1 lộ trình ôn 3 kì thi (Luyện thi 26+ TN THPT, 90+ ĐGNL HN, 900+ ĐGNL HCM, 70+ ĐGTD - Click xem ngay) tại Tuyensinh247.com.Đầy đủ theo 3 đầu sách, Thầy Cô giáo giỏi, luyện thi theo 3 giai đoạn: Nền tảng lớp 12, Luyện thi chuyên sâu, Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com