Dẫn xuất của hidrocacbon, polime
Đốt cháy hoàn toàn a gam rượu CnH2n + 1OH bằng CuO thu được 39.6 gam CO2 và 21,6 gam nước và b gam Cu. Tính các giá trị a, b và xác định công thức phân tử của rượu.
Đáp án đúng là: C
Quảng cáo
Đáp án cần chọn là: C
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com . Học online tại nhà cũng giáo viên giỏi từ trường TOP đầu cả nước. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. Phụ huynh và học sinh tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com



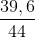 = 0,9 mol
= 0,9 mol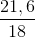 = 1,2 mol
= 1,2 mol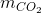 +
+ 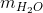 + mCu
+ mCu 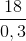 = 60
= 60







