Nguyên tố clo có số hiệu nguyên tử là 17. a) Viết cấu hình e của nguyên tử clo và xác định
Nguyên tố clo có số hiệu nguyên tử là 17.
a) Viết cấu hình e của nguyên tử clo và xác định vị trí của clo trong bảng tuần hoàn (giải thích).
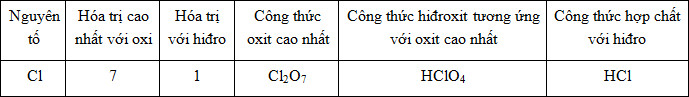
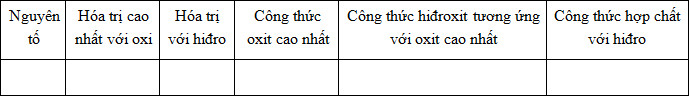
b) Điền thông tin vào bảng sau:
c) Viết công thức electron, công thức cấu tạo phân tử hợp chất của clo với hiđro.
d) Viết phương trình hoá học của phản ứng tạo thành liên kết ion khi Cl2 tác dụng với kim loại K (nhóm IA).
Quảng cáo
a) Viết cấu hình e của nguyên tử clo và xác định vị trí của clo trong bảng tuần hoàn:
Số thứ tự ô = Số hiệu nguyên tử
Số thứ tự chu kì = Số lớp electron
Số thứ tự nhóm = Số electron hóa trị
b) Nguyên tố R thuộc nhóm nA thì:
+ Hóa trị cao nhất với oxi của R là n
+ Hóa trị trong hợp chất khí với H là 8-n
Từ đó viết được công thức oxit cao nhất, công thức hiđroxit và công thức hợp chất khí với hiđro.
c) Dựa vào số electron ở lớp ngoài cùng của clo để viết công thức electron, công thức cấu tạo phân tử hợp chất của clo với hiđro.
d) Viết phương trình hoá học của phản ứng tạo thành liên kết ion khi Cl2 tác dụng với kim loại K (nhóm IA).
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com