Sự điện phân là quá trình oxi hóa - khử xảy ra trên bề mặt các điện cực khi có dòng điện
Sự điện phân là quá trình oxi hóa - khử xảy ra trên bề mặt các điện cực khi có dòng điện một chiều đi qua chất điện li nóng chảy hoặc dung dịch chất điện li nhằm thúc đẩy một phản ứng hóa học mà nếu không có dòng điện, phản ứng sẽ không tự xảy ra. Trong thiết bị điện phân:
+ Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa. Anot được nối với cực dương của nguồn điện một chiều.
+ Catot của thiết bị là nơi xảy ra bán phản ứng khử. Catot được nối với cực âm của nguồn điện một chiều.
Cho dãy điện hóa sau:

Thí nghiệm 1: Một sinh viên thực hiện quá trình điện phân dung dịch chứa đồng thời CuSO4 và NaCl có cùng nồng độ mol bằng hệ điện phân sử dụng các điện cực than chì.
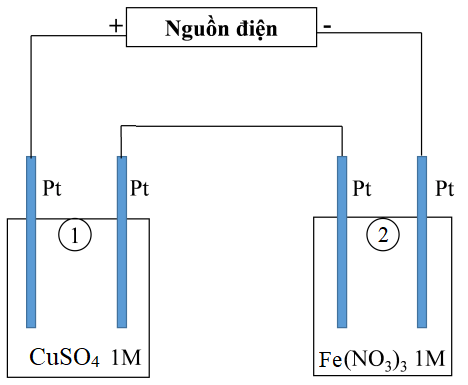
Thí nghiệm 2: Sinh viên đó tiếp tục thực hiện điện phân theo sơ đồ như hình bên.
- Bình (1) chứa 200 ml dung dịch CuSO4 1M.
- Bình (2) chứa 300 ml dung dịch Fe(NO3)3 1M.
Sau một thời gian, sinh viên quan sát thấy có 5,6 gam kim loại sắt bám lên điệc cực của bình (2). Biết trong hệ điện phân nối tiếp, số điện tử truyền dẫn trong các bình là như nhau. Nguyên tử khối của Cu và Fe lần lượt là 64 và 56 đvC.
Trả lời cho các câu 1, 2, 3 dưới đây:
Trong thí nghiệm 1, bán phản ứng nào xảy ra ở catot?
Đáp án đúng là: D
Catot của thiết bị là nơi xảy ra bán phản ứng khử.
Đáp án cần chọn là: D
Trong thí nghiệm 1, dung dịch sau điện phân có pH như thế nào?
Đáp án đúng là: B
- Anot của thiết bị là nơi xảy ra bán phản ứng oxi hóa; catot của thiết bị là nơi xảy ra bán phản ứng khử.
- Dựa vào số mol ban đầu của mỗi muối ⟹ Các phản ứng điện phân.
- Từ sản phẩm của quá trình điện phân suy ra giá trị pH của dung dịch điện phân.
Đáp án cần chọn là: B
Trong thí nghiệm 2, số gam kim loại Cu bám lên điện cực trong bình (1) là
Đáp án đúng là: C
*Bình (2): Các phản ứng điện phân tại catot bình (2):
Fe3+ + 1e → Fe2+
Fe2+ + 2e → Fe
Từ số mol của Fe3+ và Fe tính được số mol e trao đổi ở bình (2).
Do 2 bình điện phân mắc nối tiếp nên mol electron trao đổi như nhau nên ⟹ ne (bình 1) = ne (bình 2)
*Bình (1):
So sánh ne (bình 1) với \(2.{n_{C{u^{2 + }}}}\) ⟹ CuSO4 đã bị điện phân hết, H2O đang bị điện phân
Từ đó tính được lượng Cu bám vào catot bình (1).
Đáp án cần chọn là: C
Quảng cáo
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











