Điện phân 400 ml dung dịch X gồm KCl, HCl và CuCl2 0,02M (điện cực trơ, màng ngăn xốp) với
Điện phân 400 ml dung dịch X gồm KCl, HCl và CuCl2 0,02M (điện cực trơ, màng ngăn xốp) với cường độ dòng điện bằng I = 1,93A. Biết thể tích dung dịch không thay đổi trong quá trình điện phân, bỏ qua sự thủy phân của ion Cu2+. Cho đồ thị biểu diễn mối quan hệ giữa thời gian điện phân và pH của dung dịch như hình vẽ:
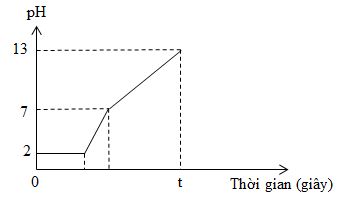
Phát biểu nào sau đây sai?
Đáp án đúng là: D
Quảng cáo
*Đoạn 1: pH không thay đổi trong khoảng thời gian catot khử Cu2+ và anot oxi hóa ion Cl-.
Catot: Cu2+ + 2e → Cu
→ ne đoạn 1 = 2.nCu2+
*Đoạn 2: pH tăng nhanh chóng do H+ bị khử cho tới khi hết tại catot:
Catot: 2H+ + 2e → H2
→ ne đoạn 2 = nH+
*Đoạn 3: pH tiếp tục tăng, dung dịch chuyển sang môi trường kiềm do H2O bị khử tại catot tạo OH-.
Catot: 2H2O + 2e → 2OH- + H2
→ ne đoạn 3 = nOH-
Vậy số mol electron trao đổi trong cả 3 giai đoạn bằng: ne trao đổi = ne đoạn 1 + ne đoạn 2 + ne đoạn 3.
Đáp án cần chọn là: D
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











