Hỗn hợp X gồm KCl, CuO, Na2CO3. Cho 30,05 gam X tác dụng vừa đủ với dung dịch chứa HCl và H2SO4,
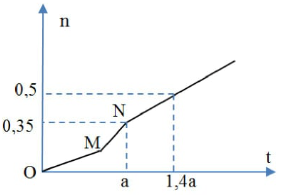
Hỗn hợp X gồm KCl, CuO, Na2CO3. Cho 30,05 gam X tác dụng vừa đủ với dung dịch chứa HCl và H2SO4, sau phản ứng thu được 2,24 lít CO2 và dung dịch Y chỉ chứa muối trung hòa. Tiến hành điện phân Y với các điện cực trơ, màng ngăn xốp, dòng điện không đổi. Tổng số mol khí thu được trên cả hai điện cực (n mol) phụ thuộc vào thời gian điện phân (t giây) được mô tả như đồ thị bên. Giả sử hiệu suất điện phân là 100%, bỏ qua sự bay hơi của nước. Khối lượng chất tan trong dung dịch Y là
Đáp án đúng là: D
Quảng cáo
X: {KCl, CuO, Na2CO3} + {HCl, H2SO4} ⟶ CO2 (0,1) + Y {K+ ; Na+ ; Cu2+; Cl-; SO42-}
30,05 gam
nNa2CO3 = nCO2 ⟹ nNa+ = 2nNa2CO3
+) Tại M: Cu2+ bị điện phân hết:
Catot (-): Cu2+ + 2e ⟶ Cu
Anot (+): 2Cl- ⟶ Cl2 + 2e
+) Tại N: Cl- bị điện phân hết
Catot (-):
Cu2+ + 2e ⟶ Cu
2H2O + 2e ⟶ H2 + 2OH-
Anot (+): 2Cl- ⟶ Cl2 + 2e
⟹ 2nCu2+ + 2nH2 = 2nCl2 (*)
⟹ ne = 2nCl2 = (I/F).a (1)
Mà: nCl2 + nH2 = 0,35 (2)
+) Từ điểm N đến điểm cuối số mol khí tăng là do H2O điện phân
2H2O ⟶ 2H2 + O2
2a ⟵ a
⟹ nO2 + nH2 = 0,5 - 0,35 = 0,15 ⟹ a
⟹ ne = 4nO2 = (I/F).(1,4a - a) (3)
Từ (1) và (3) ⟹ nCl2
Thay vào (2) ⟹ nH2
Thay vào (*) ⟹ nCu2+ = nCuO
BTKL: mKCl = mX - mNa2CO3 - mCuO ⟹ nKCl = nK+
BTĐT trong Y: nK+ + nNa+ + 2nCu2+ = nCl- + 2nSO42- ⟹ nSO42-
⟹ mY
Đáp án cần chọn là: D
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











