Cho phản ứng sau:Cho các khẳng định sau:a) \({\Delta _f}H_{298}^o\left( {S{O_2},\;g} \right)\) = – 296,8
Cho phản ứng sau:
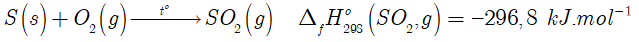
Cho các khẳng định sau:
a) \({\Delta _f}H_{298}^o\left( {S{O_2},\;g} \right)\) = – 296,8 kJ/mol là lượng nhiệt tỏa ra khi tạo ra 1 mol SO2 (g) từ đơn chất S (s) và O2 (g), đây là các đơn chất bền nhất ở điều kiện chuẩn.
b) Ở điều kiện chuẩn \({\Delta _f}H_{298}^o\left( {{O_2},\;g} \right) \ne \) 0.
c) Ở điều kiện chuẩn \({\Delta _f}H_{298}^o\left( {S,\;s} \right)\)= 0.
d) Hợp chất SO2(g) kém bền hơn về mặt năng lượng so với các đơn chất bền S (s) và O2 (g).
Số khẳng định đúng là
Đáp án đúng là: C
Quảng cáo
Dựa vào lý thuyết về năng lượng hoá học.
Đáp án cần chọn là: C
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com



















