Trong một thí nghiệm, ở điều kiện chuẩn, nhiệt độ 25oC, cho một miếng Zn có khối lượng m
Trong một thí nghiệm, ở điều kiện chuẩn, nhiệt độ 25oC, cho một miếng Zn có khối lượng m gam vào lượng dư dung dịch H2SO4 loãng. Thể tích khí hydrogen thoát ra theo thời gian được cho trong bảng sau:
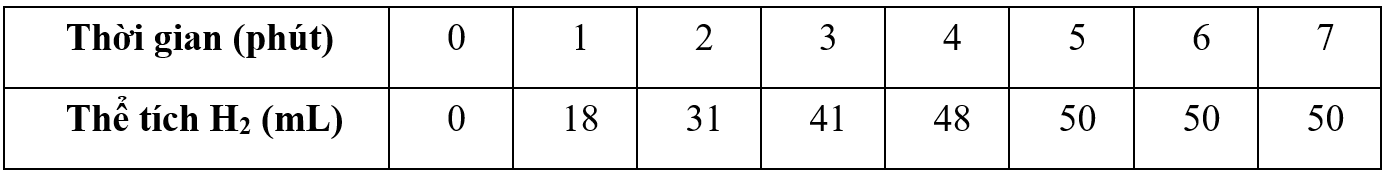
a. Hãy cho biết: Tổng thể tích khí hydrogen tạo ra trong thí nghiệm là bao nhiêu? Giá trị của m bằng bao nhiêu? Biết thể tích của 1 mol chất khí ở điều kiện chuẩn, nhiệt độ 25oC là 24,79 lít.
b. Nếu lặp lại thí nghiệm trên ở 35oC (các điều kiện khác không đổi) thì khoảng thời gian bao lâu phản ứng kết thúc? Cho biết hệ số nhiệt độ Van’t Hoff của phản ứng trên là γ = 2,4.
Quảng cáo
Tốc độ trung bình phản ứng: \(\bar v = \dfrac{{\Delta C}}{{\Delta t}}\)
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com



















