Cho nhiệt tạo thành chuẩn của một số chất trong bảng
Cho nhiệt tạo thành chuẩn của một số chất trong bảng sau:
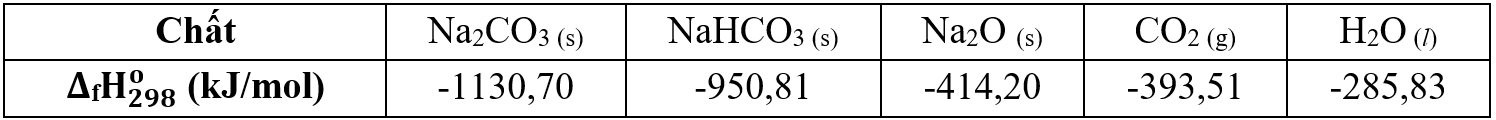
Trả lời cho các câu 1, 2, 3 dưới đây:
Cho phản ứng hóa học sau:
$2NaHC{O_3}(s)\xrightarrow{{}}N{a_2}C{O_3}(s) + C{O_2}(g) + {H_2}O(l)$
Biến thiên enthalpy chuẩn của phản ứng trên có giá trị là bao nhiêu kJ? (làm tròn kết quả tới chữ số hàng phần mười)
Đáp án đúng là:
\({\Delta _r}H_{298}^o = \sum {{\Delta _f}H_{298}^o(sp)} - \sum {{\Delta _f}H_{298}^o(cd)} \)
Đáp án cần điền là: 91,6
Cho phản ứng hóa học sau:
$N{a_2}C{O_3}(s)\xrightarrow{{}}N{a_2}O(s) + C{O_2}(g)$
Biến thiên enthalpy chuẩn của phản ứng trên có giá trị là bao nhiêu kJ? (làm tròn kết quả tới chữ số hàng đơn vị)
Đáp án đúng là:
\({\Delta _r}H_{298}^o = \sum {{\Delta _f}H_{298}^o(sp)} - \sum {{\Delta _f}H_{298}^o(cd)} \)
Đáp án cần điền là: 323
Cho các nhận định sau:
(a) Quá trình hình thành muối NaHCO3 từ các đơn chất thuận lợi về mặt năng lượng hơn so với quá trình hình thành muối Na2CO3 từ các đơn chất.
(b) Phản ứng phân hủy Na2CO3(s) ⟶ Na2O(s) + CO2(g) không diễn ra ở điều kiện thường.
(c) Ở trạng thái rắn, Na2CO3 bền với nhiệt hơn NaHCO3.
(d) Để phân hủy hoàn toàn 16,8 gam NaHCO3 ở trạng thái rắn, tạo thành Na2CO3(s), CO2(g) và H2O(l) cần cung cấp năng lượng là 18,316 kJ.
(e) Phản ứng tạo thành Na2CO3(s) từ Na2O(s) và khí CO2(s) thuận lợi về mặt năng lượng.
Có bao nhiêu phát biểu đúng trong các phát biểu trên?
Đáp án đúng là:
\({\Delta _r}H_{298}^o\) < 0 ⟶ Phản ứng tỏa nhiệt, có thể tự diễn biến
\({\Delta _r}H_{298}^o\) > 0 ⟶ Phản ứng thu nhiệt, không tự diễn biến
Đáp án cần điền là: 3
Quảng cáo
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











