Ammonia được tổng hợp từ phản ứng giữa khí nitrogen và khí hydrogen. Đây
Ammonia được tổng hợp từ phản ứng giữa khí nitrogen và khí hydrogen. Đây là phản ứng thuận nghịch và tỏa nhiệt. Theo nguyên lý chuyển dịch cân bằng Le Chaterlie, muốn cho cân bằng chuyển dịch về phía tạo thành ammonia, cần phải hạ nhiệt độ và tăng áp suất. Tuy nhiên, nếu nhiệt độ thấp quá thì phản ứng xảy ra rất chậm và nếu áp suất cao quá thì đòi hỏi thiết bị cồng kềnh và phức tạp. Trên thực tế, người ta thường thực hiện phản ứng ở nhiệt độ khoảng 450 – 500 °C, áp suất khoảng 200 – 300 atm và dùng chất xúc tác là sắt kim loại được hoạt hóa bằng hỗn hợp Al2O3 và K2O để làm cho cân bằng nhanh chóng được thiết lập. Ở các điều kiện như trên, hiệu suất chuyển hóa thành NH3 cũng chỉ đạt tới 20 – 25%.
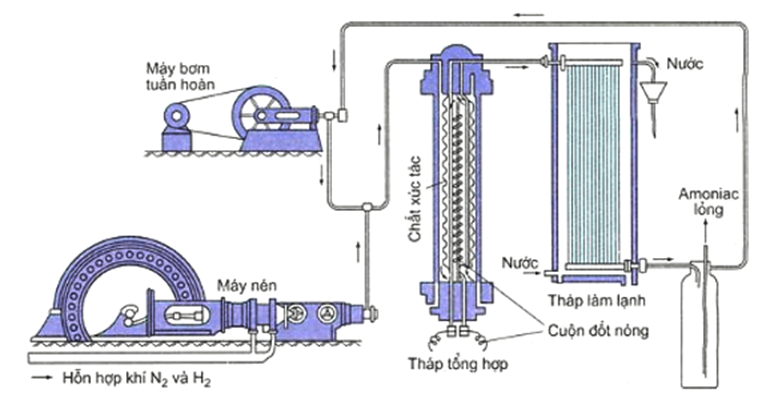
Hình 3.7. Sơ đồ thiết bị tổng hợp amoniac trong công nghiệp.
Hỗn hợp khí N2 và H2 (tỷ lệ mol 1 : 3) được nén ở áp suất cao và đưa vào tháp tổng hợp (hình 3.7). Trong tháp này, ammonia được tạo thành ở các điều kiện nhiệt độ, áp suất và chất xúc tác thích hợp đã nêu ở trên. Hỗn hợp khí đi ra từ tháp tổng hợp (gồm có N2, H2 và NH3) được dẫn đến tháp làm lạnh. Ở đây, khí amoniac hóa lỏng và được tách riêng ra, còn hỗn hợp khí N2 và H2 chưa phản ứng được đưa trở lại tháp tổng hợp, việc đưa trở lại này làm tăng hiệu suất chung của quá trình tổng hợp NH3 trong công nghiệp đạt đến gần 100%.
Trả lời cho các câu 1, 2, 3, 4, 5 dưới đây:
Hãy cho biết các phát biểu sau là đúng hay sai?
| Đúng | Sai | |
|---|---|---|
| a) Phản ứng tổng hợp NH3 tỏa nhiệt nên không cần cung cấp nhiệt cho phản ứng. | ||
| b) Nhiệt độ của tháp tổng hợp càng cao thì hiệu suất phản ứng càng lớn. | ||
| c) Chất xúc tác làm tăng hiệu suất của phản ứng tổng hợp NH3 từ N2 và H2. | ||
| d) Khi qua tháp làm lạnh chỉ NH3 hóa lỏng, điều này chứng tỏ NH3 có nhiệt độ hóa lỏng cao hơn N2 và H2. |
Đáp án đúng là: S; S; S; Đ
Đọc kĩ đoạn văn.
Đáp án cần chọn là: S; S; S; Đ
Trước khi đi vào tháp tổng hợp, hỗn hợp khí gồm N2 và H2 được lấy theo tỉ lệ mol H2 : N2 = a. Giá trị của a là____
Đáp án đúng là: 3
Đọc kĩ đoạn dữ liệu.
Đáp án cần điền là: 3
Hiệu suất của quá trình tổng hợp NH3 trong công nghiệp thường đạt gần 100%, và lớn hơn nhiều hiệu suất của phản ứng. Yếu tố nào sau đây quyết định đến hiệu suất tổng hợp NH3 trong công nghiệp cao như vậy?
Đáp án đúng là: B
Theo ngữ liệu “Hỗn hợp khi đi ra từ tháp tổng hợp (gồm có N2, H2 và NH3) được dẫn đến tháp làm lạnh. Ở đây, khi amoniac hóa lỏng và được tách riêng ra, còn hỗn hợp khí N2 và H2 chưa phản ứng được đưa trở lại tháp tổng hợp, việc đưa trở lại này làm tăng hiệu suất chung của quá trình tổng hợp NH3 trong công nghiệp đạt đến gần 100%”.
Đáp án cần chọn là: B
Theo những đặc điểm tổng hợp ammonia được mô tả ở trên, nếu tiến hành phản ứng tổng hợp ammonia ở áp suất cao sẽ dẫn đến những thay đổi nào sau đây? (hãy chọn những câu trả lời đúng).
| Đúng | Sai | |
|---|---|---|
| a) Làm tăng tốc độ phản ứng. | ||
| b) Phản ứng sẽ hướng đến sự tạo thành sản phẩm khác. | ||
| c) Giảm khả năng xúc tác của chất xúc tác. | ||
| d) Tăng hiệu suất tổng hợp NH3. |
Đáp án đúng là: Đ; S; S; Đ
Theo ngữ liệu “Ammonia được tổng hợp từ phản ứng giữa khi nitrogen và khí hdrogen. Đây là phản ứng thuận nghịch và tỏa nhiệt. Theo nguyên lý chuyển dịch cân bằng Le Chaterlie, muốn cho cân bằng chuyên dịch về phía tạo thành ammonia, cần phải hạ nhiệt độ và tăng áp suất’’
Đáp án cần chọn là: Đ; S; S; Đ
Hiệu suất phản ứng tổng hợp ammonia là 25%. Thành phần % theo thể tích của khí NH3 sau khi đi qua tháp tổng hợp là
Đáp án đúng là: B
Nếu khí dẫn vào tháp có nN2 = 1 (mol) thì nH2 = 3 (mol)
⟹ Số mol N2 phản ứng = ?
⟹ Số mol khí đi ra khỏi tháp
Đáp án cần chọn là: B
Quảng cáo
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











