Nước tự nhiên được sử dụng làm nguồn nước uống có nhiều loại khoáng
Nước tự nhiên được sử dụng làm nguồn nước uống có nhiều loại khoáng chất hòa tan như magnesium (\(M{g^{2 + }}\)), sodium (Na+) và calcium (\(C{a^{2 + }}\)). Nồng độ của các loại khoáng chất này cần được xử lý và kiểm soát một cách nghiêm ngặt để không ảnh hưởng tới sức khỏe của người sử dụng.
Mẫu nước uống cần được kiểm tra bằng phương pháp chuẩn độ EDTA \(M{g^{2 + }}\)(EDTA là ethylenediaminetetraacetic acid – một acid có khả năng liên kết với ion kim loại tạo thành phức chất hòa tan trong nước ngay cả ở pH trung tính) để xác định nồng độ của ion . Thí nghiệm được tiến hành như sau:
Bước 1. Thêm 10 ml mẫu nước cần xác định nồng độ ion \(C{a^{2 + }}\) và \(M{g^{2 + }}\) vào bình erlen, thêm chỉ thị X.
Bước 2. Thêm chính xác 50 ml EDTA (tồn tại dưới dạng \({Y^{4 - }}\)) có nồng độ 20 ppm (phần triệu) vào buret.
Bước 3: Tiến hành chuẩn độ cho tới khi nhìn thấy sự đổi màu bền của dung dịch trong bình erlen.
Biết: Chất chỉ thị X có khả năng hình thành phức chất với ion \(M{g^{2 + }}\) tạo thành dung dịch có màu tím, còn khi tồn tại trạng thái tự do thì có màu xanh lam. EDTA hình thành phức chất với ion \(M{g^{2 + }}\) với tỉ lệ phản ứng là 1 : 1.
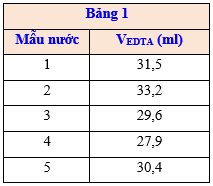
Tiến hành chuẩn độ với 5 mẫu nước, thể tích của dung dịch EDTA đã tham gia chuẩn độ được ghi trong bảng 1 như sau:
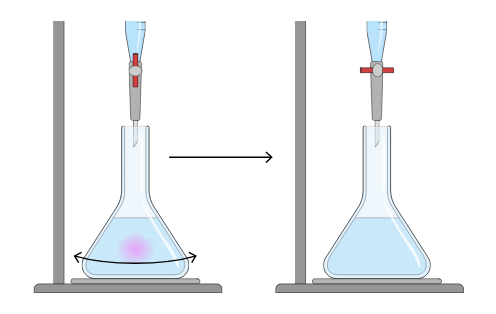
Hình 1.
Trả lời cho các câu 1, 2, 3 dưới đây:
Nhận định nào dưới đây là đúng về hiện tượng xảy ra trong bình erlen tại điểm kết thúc chuẩn độ?
Đáp án đúng là: B
Dựa vào đoạn thông tin mô tả sự biến đổi màu sắc của chất chỉ thị X: Chất chỉ thị X có khả năng hình thành phức chất với ion \(M{g^{2 + }}\) tạo thành dung dịch có màu tím, còn khi tồn tại trạng thái tự do thì có màu xanh lam.
Đáp án cần chọn là: B
Ion \(M{g^{2 + }}\) trong nước cao gây ra hiện tượng nước cứng, gây ảnh hưởng nhiều đến đời sống. Bảng 2 cho biết thông số để phân loại nước cứng dựa vào nồng độ ion \(M{g^{2 + }}\) như sau:
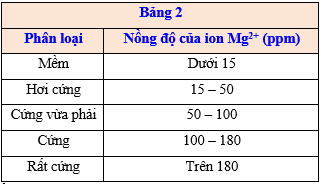
Mẫu nước số 5 trong thí nghiệm chuẩn độ là
Đáp án đúng là: C
Tính nồng độ ion \(M{g^{2 + }}\) tham gia phản ứng rồi phân loại nước cứng.
Đáp án cần chọn là: C
Một mẫu nước máy từ một nơi khác được cũng thực hiện quy trình chuẩn độ ion \(M{g^{2 + }}\) và nhận thấy mẫu nước trên đã được xử lý đến mức không còn ion \(M{g^{2 + }}\). Nhận định nào dưới đây đúng về mẫu nước trên?
Đáp án đúng là: B
Dựa vào đoạn thông tin nói về sự đổi màu của phức chất.
Đáp án cần chọn là: B
Quảng cáo
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











