Cho mô hình tinh thể kim loại sodium (Na) và mô hình tinh thể muối sodium
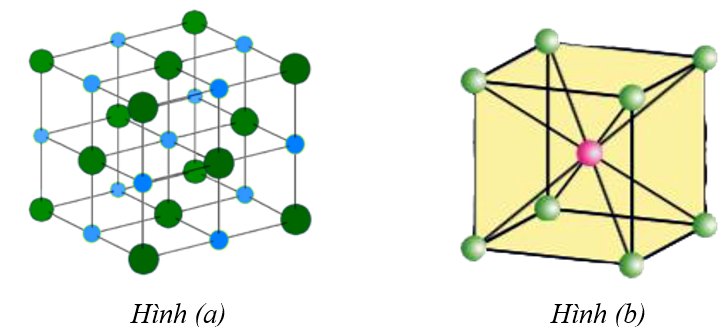
Cho mô hình tinh thể kim loại sodium (Na) và mô hình tinh thể muối sodium chloride (NaCl) như hình vẽ dưới đây. Biết rằng NaCl nóng chảy ở 801oC và Na nóng chảy ở 98oC.
| Đúng | Sai | |
|---|---|---|
| a) Mô hình tinh thể muối ăn (mô hình a) được tạo thành từ hai mạng tinh thể lập phương tâm mặt lồng vào nhau. | ||
| b) Nguyên tử trung tâm ở mô hình (b) chỉ có thể là ion Na+. | ||
| c) Năng lượng liên kết ion trong tinh thể NaCl lớn hơn năng lượng liên kết kim loại trong tinh thể Na. | ||
| d) Liên kết kim loại trong tinh thể Na và liên kết ion trong tinh thể NaCl đều được hình thành bởi lực hút tĩnh điện giữa cation kim loại và electron hóa trị tự do. |
Đáp án đúng là: Đ; S; Đ; S
Quảng cáo
a), b) Đặc điểm cấu tạo mạng tinh thể lập phương tâm mặt
c) Năng lượng liên kết ion với liên kết kim loại.
d) Đặc điểm mạng tinh thể ion mà mạng tinh thể kim loại.
Đáp án cần chọn là: Đ; S; Đ; S
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











