Chu trình nhiệt hóa học Na–O–H là một quá trình sản xuất hydro (H₂) từ nước (H₂O) mà
Chu trình nhiệt hóa học Na–O–H là một quá trình sản xuất hydro (H₂) từ nước (H₂O) mà không sử dụng nhiên liệu hóa thạch, thay vào đó dùng nhiệt năng (từ năng lượng tái tạo hoặc lò phản ứng hạt nhân).
Quá trình này gồm 3 phản ứng hóa học lặp lại tuần hoàn, trong đó nước là nguồn cung cấp hydro. Điểm đặc biệt là các hóa chất (Na, NaOH, Na₂O, Na₂O₂) được tái sử dụng liên tục, tạo thành một chu trình khép kín.
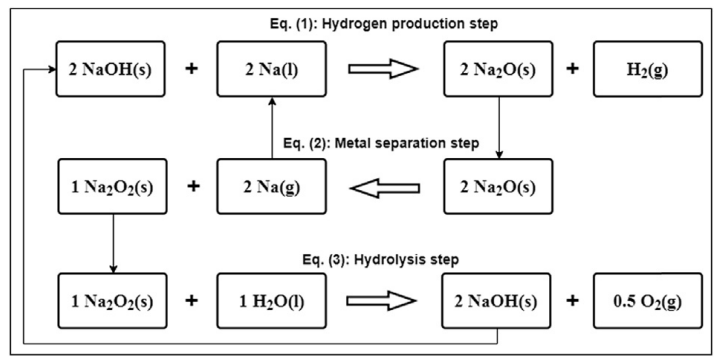
Ảnh 1. Sơ đồ các bước trong chu trình Na – O – H
Để xác định điều kiện tối ưu cho từng phản ứng trong chu trình, nhóm tác giả sử dụng năng lượng tự do Gibbs để phân tích các điều kiện vận hành khác, có thể tốt hơn cho chu trình Na – O – H.
$\Delta G_{i} = \Delta H_{i} - T_{i}\Delta S_{i}$ (4)
Trong đó:
i: điều kiện áp suất, nhiệt độ
∆Hi, ∆Si: biến thiên enthalpy và entropy của phản ứng
∆Gi: biến thiên năng lượng tự do Gibbs của phản ứng.
Có 3 giá trị có thể có của ∆G:
∆G < 0: Phản ứng tự xảy ra, không cần cung cấp năng lượng từ bên ngoài.
∆G = 0: Hệ ở trạng thái cân bằng
∆G > 0: Phản ứng không tự xảy ra, cần cung cấp năng lượng từ bên ngoài.
Giai đoạn 1: Tạo hydrogen:
$2NaOH(s) + 2Na(l)\overset{}{\rightarrow}2Na_{2}O(s) + H_{2}(g)$ (1)
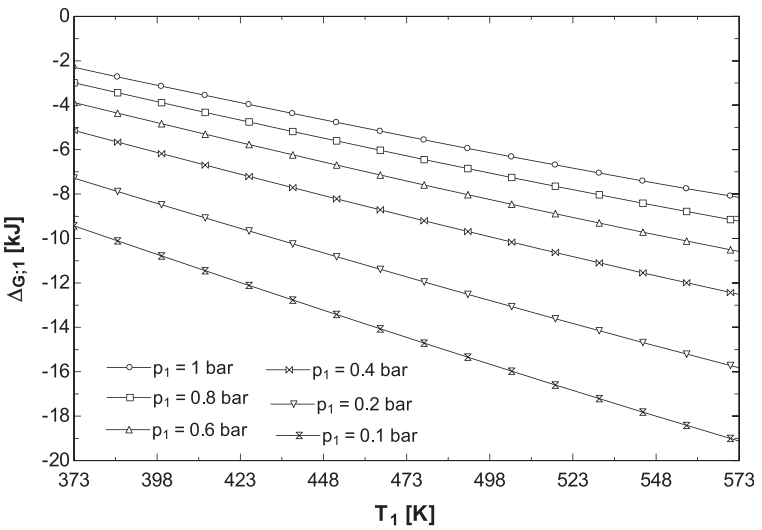
Phản ứng có thể diễn ra trong khoảng nhiệt độ từ 100oC, áp suất thường (1 bar)
Giai đoạn 2: Tách kim loại
$2Na_{2}O(s)\overset{}{\rightarrow}Na_{2}O(s) + 2Na(g)$ (2)
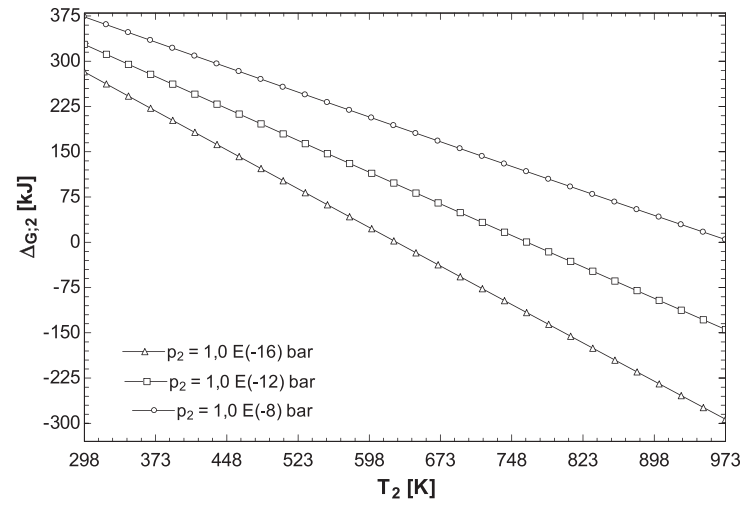
Phản ứng có thể diễn ra trong khoảng nhiệt độ 500oC với áp suất cực thấp.
Giai đoạn 3: Thuỷ phân nước
$Na_{2}O(s) + H_{2}O(l)\overset{}{\rightarrow}2NaOH + 1/2O_{2}(g)$
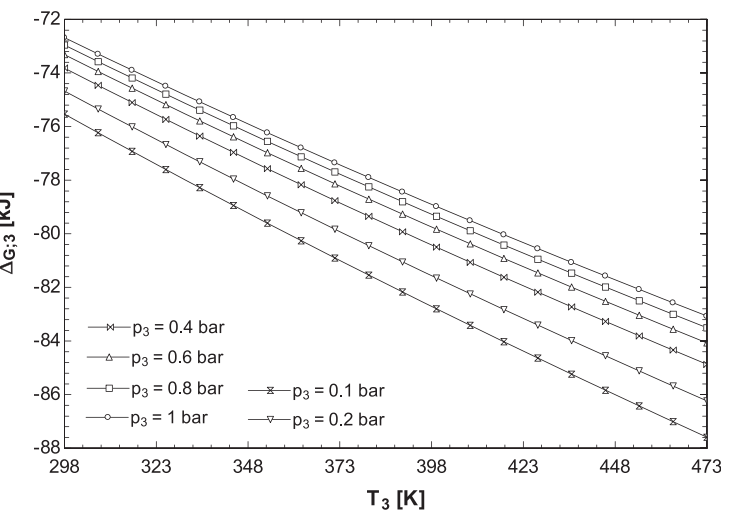
Phản ứng thuỷ phân được diễn ra ở điều kiện thường.
Nguồn: Joao G.O. Marques, Antonella L. Costa, Claubia Pereira, “Gibbs free energy (∆G) analysis for the NaeOeH (sodium-oxygen-hydrogen) thermochemical water splitting cycle”, https://doi.org/10.1016/j.ijhydene.2019.04.064
Trả lời cho các câu 1, 2, 3, 4, 5, 6, 7 dưới đây:
Phản ứng nào dưới đây là bước tạo hydrogen trong chu trình nhiệt hoá học Na – O – H?
Đáp án đúng là: A
Dựa vào thông tin bài đọc, xác định phản ứng tạo hydrogen tức hydrogen đóng vai trò sản phẩm.
Đáp án cần chọn là: A
Cho biết nhận định nào dưới đây đúng khi nói về bước thuỷ phân trong chu trình Na – O – H?
Đáp án đúng là: A; C
Dựa vào thông tin bài đọc, xác định sản phẩm, điều kiện phản ứng.
Đáp án cần chọn là: A; C
Phản ứng tách kim loại trong chu trình Na – O – H gặp trở ngại gì lớn nhất trong thực tế?
Đáp án đúng là: C
Điều kiện phản ứng.
Đáp án cần chọn là: C
Năng lượng tự do Gibbs âm cho thấy phản ứng tự xảy ra ở mọi điều kiện.
Đáp án đúng là: B
Ý nghĩa giá trị biến thiên năng lượng tự do Gibbs.
Đáp án cần chọn là: B
Cho biết các phát biểu sau về ∆G trong chu trình Na – O – H đúng hay sai?
| Đúng | Sai | |
|---|---|---|
| a) Nếu ∆G dương thì phản ứng xảy ra cần cung cấp năng lượng từ bên ngoài. | ||
| b) Tăng nhiệt độ luôn làm tăng ∆G. | ||
| c) ∆G của phản ứng thuỷ phân âm ở mọi điều kiện. | ||
| d) Phản ứng tách kim loại cần điều kiện chân không để ∆G. | ||
| e) ∆G phụ thuộc vào nhiệt độ và áp suất. |
Đáp án đúng là: Đ; S; Đ; Đ; Đ
Dựa vào thông tin bài đọc, xác định ý nghĩa ∆G trong từng gia đoạn phản ứng.
Đáp án cần chọn là: Đ; S; Đ; Đ; Đ
Trong điều kiện chuẩn (25oC, 1 atm), phản ứng thuỷ phân trong cho trình Na – O – H có biến thiên enthalpy và entropy lần lượt là -52,77 kJ và -66,82 J/K. Năng lượng tự do Gibbs của phản ứng tại điều kiện này là_______ (kJ) (Biết 25oC bằng 298K)
Đáp án đúng là: -32,87
Sử dụng công thức: $\Delta G_{i} = \Delta H_{i} - T.\Delta S_{i}$
Đáp án cần điền là: -32,87
Trong các chất sau đây, chất nào là nguyên liệu đầu vào thực sự (cần cung cấp từ bên ngoài) cho chu trình nhiệt hóa học Na–O–H nhằm sản xuất hydro? Chọn nhiều phương án
Đáp án đúng là: B; D
Dựa vào thông tin bài đọc, xác định sản phẩm, chất phản ứng và điều kiện phản ứng xa
Đáp án cần chọn là: B; D
Quảng cáo
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











