Động học hóa học là một nhánh của hóa học vật lý chuyên nghiên cứu tốc độ của các
Động học hóa học là một nhánh của hóa học vật lý chuyên nghiên cứu tốc độ của các phản ứng hóa học, tức là sự thay đổi nồng độ của chất phản ứng và sản phẩm theo thời gian. Hiểu động học hóa học giúp chúng ta biết được cách thức và tốc độ mà các phản ứng diễn ra, từ đó khám phá được cơ chế mà các phản ứng xảy ra. Nghiên cứu bậc của phản ứng cũng là một trong những nội dung quan trọng của động hoá học.
Cho phản ứng tổng quát: Aa + Bb ⟶ cC + dD
Tốc độ phản ứng trên được biểu diễn: $v = k.C_{A}{}^{n}.C_{B}{}^{m}$
Trong đó: v: Tốc độ phản ứng.
k: Hằng số tốc độ (phụ thuộc vào nhiệt độ, nếu xác định đúng bậc của phản ứng, k không đổi trong nhiệt độ nhất định).
Lúc này: n được gọi là bậc riêng phần đối với chất A, m được gọi là bậc riêng phần đối với chất b; n + m = bậc động học của phản ứng.
Từ phương trình động học của tốc độ, người ta tính toán và dự doán được cơ chế, thành phần các chất trong hệ tại thời điểm bất kỳ cũng như dự đoán được khả năng phản ứng của hệ tại nhiệt độ khác nhau.
Ví dụ với phản ứng bậc 1: $v = k.C_{X}{}^{1}$; tại thời điểm t bất kỳ: $k \times t = \ln\dfrac{C_{o}}{C_{t}} = \ln\dfrac{P_{o}}{P_{t}}$
Trong đó, C0; Ct là nồng độ chất tại thời điểm ban đầu và thời điểm t.
P0; Pt là áp suất chất tại thời điểm ban đầu và thời điểm t (Đối với chất khí).
Phương trình: $k \times t = \ln\dfrac{C_{o}}{C_{t}} = \ln\dfrac{P_{o}}{P_{t}}$ được gọi là phương trình động học của phản ứng.
Tại nhiệt độ T2 khác nhiệt độ T1 ban đầu, ta có: $\text{ln}\dfrac{\text{k}_{\text{2}}}{\text{k}_{\text{1}}}\text{=~-}\dfrac{\text{E}_{\text{a}}}{\text{R}}\left( {\dfrac{\text{1}}{\text{T}_{\text{2}}}\text{-}\dfrac{\text{1}}{\text{T}_{\text{1}}}} \right)$
Trong đó, $\text{k}_{\text{1}}\text{,k}_{\text{2}}$là hằng số tốc độ của phản ứng tại $\text{T}_{\text{1}}\text{,T}_{\text{2}}$;
$\text{E}_{\text{a}}$là năng lượng hoạt hoá của phản ứng
R: Hằng số ( = 8,314 J/K).
$\text{T}_{\text{1}}\text{,T}_{\text{2}}$: nhiệt độ (T = toC +273) K
Bằng cách tính được gần đúng năng lượng hoạt hoá, người ta dự đoán được khả năng xảy ra và có các biện pháp giúp phản ứng dễ xảy ra hơn.
Sunfuryl chloride ($\text{SO}_{\text{2}}\text{Cl}_{\text{2}}$) được sử dụng rộng rãi trong công nghiệp. Sunfuryl chloride là một chất lỏng không màu, có mùi cay, sôi ở 70oC. Khi nhiệt độ trên 70oC nó sẽ phân hủy tạo thành $\text{SO}_{\text{2}}$và $\text{Cl}_{\text{2}}$ theo phản ứng: $\text{SO}_{\text{2}}\text{Cl}_{\text{2}}{}_{(\text{k})}\ \overset{}{\rightarrow}\text{~SO}_{\text{2}}{}_{(\text{k})}\text{~+~Cl}_{\text{2}}{}_{(\text{k})}$
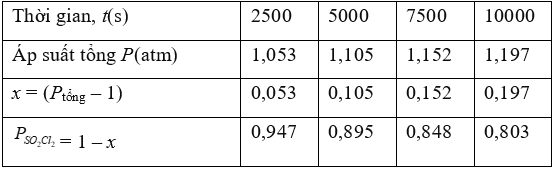
Khi nghiên cứu động học của phản ứng trên, cho thấy: Trong một bình kín thể tích không đổi chứa $\text{SO}_{\text{2}}\text{Cl}_{\text{2}}{}_{(k)}$được giữ ở nhiệt độ 375K. Quá trình phân hủy $\text{SO}_{\text{2}}\text{Cl}_{\text{2}}{}_{(k)}$được theo dõi bằng sự thay đổi áp suất trong bình. Kết quả thu được như sau:
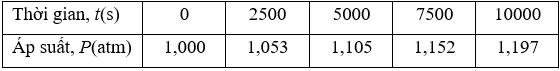
Trả lời cho các câu 1, 2, 3 dưới đây:
Phát biểu nào sau đây là sai?
Đáp án đúng là: B
Dựa vào lý thuyết được đưa ra trong bài đọc về ý nghĩa của động học hoá học, phương trình động học và thí nghiệm nghiên cứu, tìm ra nhận định đúng, nhận định sai.
Đáp án cần chọn là: B
Giá trị hằng số tốc độ của phản ứng ở 375K là bao nhiêu, giả sử phản ứng trên là phản ứng bậc 1?
Đáp án đúng là: C
Từ các dữ kiện về áp suất tổng, tính áp suất của $\text{SO}_{\text{2}}\text{Cl}_{\text{2}}$ở các thời điểm, từ đó tính k tại các thời điểm, giá trị của k là giá trị trung bình cộng của các k tính tại các thời gian khác nhau đó.
Đáp án cần chọn là: C
Nếu phản ứng trên được tiến hành ở 385K, áp suất của bình sau 1 giờ là 1,55 atm. Năng lượng hoạt hóa của phản ứng phân hủy trên là
Đáp án đúng là: A
Tính giá trị k2 tại 385K.
Áp dụng công thức: $\text{ln}\dfrac{\text{k}_{\text{2}}}{\text{k}_{\text{1}}}\text{=-}\dfrac{\text{E}_{\text{a}}}{\text{R}}\left( {\dfrac{\text{1}}{\text{T}_{\text{2}}}\text{-}\dfrac{\text{1}}{\text{T}_{\text{1}}}} \right)$
Tính được năng lượng hoạt hoá.
Đáp án cần chọn là: A
Quảng cáo
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com