1.1. (1,0 điểm) Nêu hiện tượng xảy ra trong các thí nghiệm sau và viết phương trình hoá học
1.1. (1,0 điểm)
Nêu hiện tượng xảy ra trong các thí nghiệm sau và viết phương trình hoá học minh hoạ:
a) Nhúng sợi dây đồng vào dung dịch iron(III) sulfate.
b) Cho mẩu nhỏ sodium vào dung dịch copper(II) chloride.
c) Sục từ từ khí SO2 đến dư vào dung dịch nước brommine.
d) Nhỏ từ từ dung dịch HCl đến dư vào dung dịch KAlO2.
1.2. (1,0 điểm)
Có 4 lọ X, Y, Z, T mất nhãn chứa các dung dịch không màu: BaCl2, HCl, Na2CO3 và KHSO4. Tiến hành 2 thí nghiệm như sau:
Thí nghiệm 1: Cho một lượng dung dịch Y vào dung dịch X hay một lượng dung dịch Y vào dung dịch Z thì đều thấy có bọt khí thoát ra.
Thí nghiệm 2: Cho một lượng dung dịch T vào dung dịch X hay một lượng dung dịch T vào dung dịch Y thì đều có kết tủa trắng tạo ra.
Hãy cho biết các chất trong các lọ X, Y, Z, T và viết các phương trình phản ứng xảy ra trong các thí nghiệm trên.
Quảng cáo
1.1 Tính chất hoá học của kim loại.
1.2 Dấu hiệu một số phản ứng, tính chất hoá học một số muối.
Cách giải:
1.1.
a) Sợi dây đồng bị ăn mòn, màu vàng nâu của dung dịch nhạt dần và chuyển dần sang màu xanh
Cu + Fe2(SO4)3 ⟶ CuSO4 + 2FeSO4
b) Mẩu Na tan ra, đồng thời xuất hiện bọt khí không màu và kết tủa màu xanh lam.
Ban đầu: 2Na + 2H2O ⟶ 2NaOH + H2
Sau đó: 2NaOH + CuSO4 ⟶ Na2SO4 + Cu(OH)2
c) Dung dịch nước brom bị nhạt màu dần đến mất màu
SO2 + Br2 + H2O ⟶ H2SO4 + 2HBr
d) Ban đầu xuất hiện kết tủa keo trắng, kết tủa tăng dần đến cực đại sau đó tan dần tạo dung dịch trong suốt, không màu.
Ban đầu: HCl + KAlO2 + H2O → Al(OH)3 + KCl
Sau đó: Al(OH)3 + 3HCl → AlCl3 + 3H2O
1.2.
- Thứ phản ứng của bốn hoá chất với nhau:
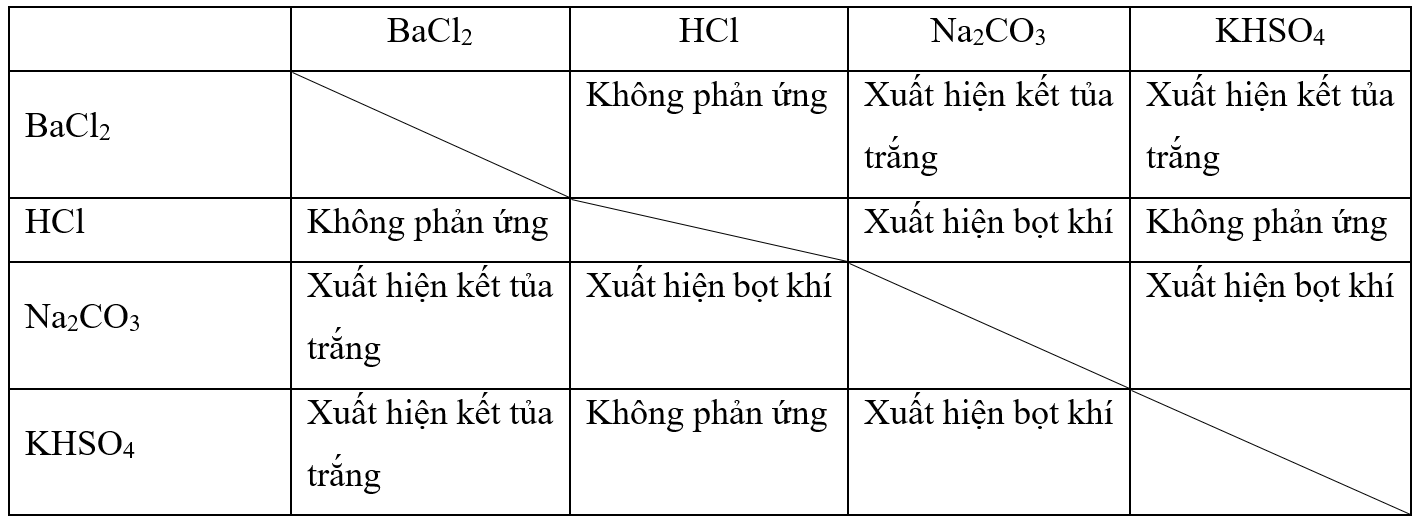
- Ta có:
Thí nghiệm 1: Y là Na2CO3; X hoặc Z là HCl hoặc KHSO4
Thí nghiệm 2: T là BaCl2; X hoặc Y là Na2CO3 hoặc KHSO4
- Vậy, X là KHSO4, Y là Na2CO3, Z là HCl, T là BaCl2
- Phương trình hoá học
(1) Na2CO3 + 2KHSO4 ⟶ Na2SO4 + K2SO4 + H2O + CO2
(2) Na2CO3 + 2HCl ⟶ 2NaCl + H2O + CO2
(3) BaCl2 + KHSO4 ⟶ BaSO4 + KCl + HCl
(4) BaCl2 + Na2CO3 ⟶ BaCO3 + 2NaCl
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











