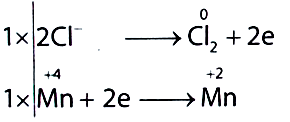Tiến hành điều chế một lượng nhỏ khí chlorine trong phòng thí nghiệm bằng
Tiến hành điều chế một lượng nhỏ khí chlorine trong phòng thí nghiệm bằng cách cho magnanese dioxide tác dụng với hydrochloric acid đặc, dư:
$\text{MnO}_{2} + \text{HCl}\overset{\text{t}^{0}}{\rightarrow}\text{MnCl}_{2} + \text{Cl}_{2} + \text{H}_{2}\text{O}$
a) Lập phương trình hoá học của phản ứng bằng phương pháp thăng bằng electron.
b) Cho KMnO4 rắn tác dụng với acid HCl đặc, dư ở nhiệt độ thường theo sơ đồ:
$\left. \text{KMnO}_{4} + \text{HCl}\rightarrow\text{KCl} + \text{MnCl}_{2} + \text{Cl}_{2} + \text{H}_{2}\text{O} \right.$
So sánh số mol Cl2 thoát ra ở (1) và (2) khi dùng MnO2 và KMnO4 với cùng khối lượng.
Quảng cáo
Cân bằng PTHH bằng phương pháp thăng bằng electron.
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com