Cho một lượng dư đá vôi vào 100 mL dung dịch HCl. Theo dõi thể tích
Cho một lượng dư đá vôi vào 100 mL dung dịch HCl. Theo dõi thể tích khí thoát ra theo thời gian, thu được kết quả trong bảng sau (thể tích khí đo ở 0oC, 1 atm)
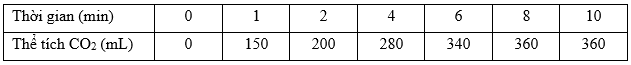
a) Tính tốc độ trung bình của phản ứng trong các khoảng thời gian:
- Trong 1 phút đầu tiên.
- Từ đầu đến phút thứ 8:
b) Phản ứng kết thúc sau mấy phút?
c) Tính nồng độ dung dịch HCl đã dùng.
Quảng cáo
a) Tốc độ trung bình: $\text{v}_{\text{tb}} = \dfrac{\Delta\text{v}}{\Delta\text{t}}$
b) Quan sát số liệu ở bảng.
c) nHCl = 2 nCO2 => CHCl
>> Học trực tuyến Lớp 10 cùng thầy cô giáo giỏi tại Tuyensinh247.com, (Xem ngay) Cam kết giúp học sinh học tốt, bứt phá điểm 9,10 chỉ sau 3 tháng, làm quen kiến thức, định hướng luyện thi TN THPT, ĐGNL, ĐGTD ngay từ lớp 10
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











