Ammonia có nhiều ứng dụng quan trọng như sản xuất phân đạm, nitric acid, làm dung
Ammonia có nhiều ứng dụng quan trọng như sản xuất phân đạm, nitric acid, làm dung môi. Hiện nay người ta sản xuất ammonia bằng cách chuyển hoá có xúc tác một hỗn hợp gồm không khí, hơi nước và khí methane (thành phần chính của khí thiên nhiên) theo quy trình Haber.
Phản ứng điều chế H2: $C{{H}_{4}}(g)+2{{H}_{2}}O(g)\xrightarrow{xt,{{t}^{o}}}C{{O}_{2}}(g)+4{{H}_{2}}(g)$ (1)
Phản ứng loại O2 để thu N2: $C{{H}_{4}}(g)+2{{O}_{2}}(g)\xrightarrow{{{t}^{o}}}C{{O}_{2}}(g)+2{{H}_{2}}O(g)$ (2)
Phản ứng tổng hợp NH3: $N_{2}(g) + 3H_{2}(g)\overset{xt,t^{o},p}{\rightleftharpoons}2NH_{3}$$\bigtriangleup_{r}H_{298}^{0} = - 92(kJ).$
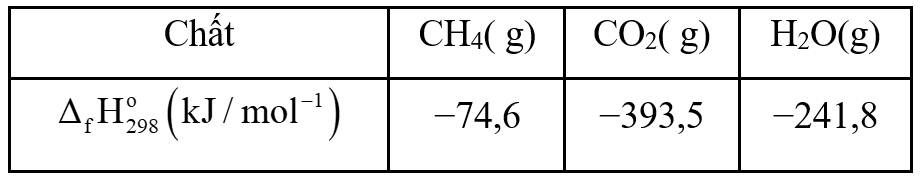
Phản ứng (1) là phản ứng thu nhiệt mạnh. Lượng nhiệt này được cung cấp từ quá trình đốt cháy hoàn toàn khí methane theo phương trình hóa học (2). Xét các phản ứng ở điều kiện chuẩn và hiệu suất chuyển hóa của methane là 100%. Biết 80% lượng nhiệt tỏa ra từ phản ứng (2) được cung cấp cho phản ứng (1) và các giá trị nhiệt tạo thành ($\bigtriangleup_{f}H_{298}^{0}$) của các chất ở điều kiện chuẩn được cho ở bảng sau:
Để sản xuất được 0,36 tấn khí hydrogen trong giai đoạn trên cần dùng m tấn khí methane. Giá trị của m là? (Không làm tròn kết quả các phép tính trung gian, chỉ làm tròn kết quả cuối cùng đến hàng phần mười).
Đáp án đúng là:
Quảng cáo
Tính nhiệt phản ứng (1) bằng nhiệt tạo thành ⟹ Xác định nhiệt thu để tạo H2:
$\bigtriangleup_{r}H_{298}^{0} = {\sum{\bigtriangleup H_{f}^{0}}}(sp) - {\sum{\bigtriangleup H_{f}^{0}(cd)}}$$= \lbrack 4 \bigtriangleup H_{f}^{0}(H_{2}) + \bigtriangleup H_{f}^{0}(CO_{2})\rbrack - \lbrack \bigtriangleup H_{f}^{0}(CH_{4}) + 2. \bigtriangleup H_{f}^{0}(H_{2}O)\rbrack.$
Tính nhiệt phản ứng (2)⟹ Xác định nhiệt tỏa khi đốt CH4:
$\bigtriangleup_{r}H_{298}^{0} = {\sum{\bigtriangleup H_{f}^{0}}}(sp) - {\sum{\bigtriangleup H_{f}^{0}(cd)}}$$= \lbrack 2 \bigtriangleup H_{f}^{0}(H_{2}O) + \bigtriangleup H_{f}^{0}(CO_{2})\rbrack - \lbrack \bigtriangleup H_{f}^{0}(CH_{4}) + 2. \bigtriangleup H_{f}^{0}(O_{2})\rbrack.$
Lấy 80% nhiệt tỏa (2) dùng để bù cho nhiệt thu (1) ⟹ suy ra lượng CH4 bị đốt.
Từ phương trình (1): CH4 → 4H2 ⟹ tính lượng CH4 tạo ra 0,36 tấn H₂.
Đáp án cần điền là: 0,9
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











