Câu 1(TH). (2 điểm) 1.1. Viết phương trình hóa học hoàn thành sơ đồ chuyển hóa sau, ghi rõ
Câu 1(TH). (2 điểm)
1.1. Viết phương trình hóa học hoàn thành sơ đồ chuyển hóa sau, ghi rõ điều kiện (nếu có).
\(\begin{gathered}
A\xrightarrow{{(1)}}B\xrightarrow{{(2)}}C\xrightarrow{{(3)}}D\xrightarrow{{(4)}}E\xrightarrow{{(5)}}F \hfill \\
\,\,\,\,\,\,\,\,\,\,\,\,\,\,{\,^{(6)}} \uparrow \hfill \\
\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,\,G \hfill \\
\end{gathered} \)
Cho biết B là glucozơ, F là metan và A, C, D, E, G là các hợp chất hữu cơ khác nhau.
1.2. Nguyên tố A có số hiệu nguyên tử là 11. Hãy cho biết:
a) Vị trí của A trong bảng tuần hoàn.
b) Tính chất hóa học cơ bản của A và so sánh với các nguyên tố lân cận.
1.3. Cho hỗn hợp gồm các chất rắn BaO, CuO và SiO2. Trình bày phương pháp hóa học tách riêng từng chất ra khỏi hỗn hợp với điều kiện không làm thay đổi khối lượng các chất.
Quảng cáo
1.1 Nắm vững tính chất hóa học của các chất hữu cơ cơ bản và viết PTHH thích hợp
1.2 Dựa vào p, e để xác định được vị trí của nguyên tố trong bảng hệ thống tuần hoàn, từ đó so sánh tính chất hóa học đặc trưng với các nguyên tố lân cận có cùng chu kỳ hoặc cùng nhóm.
1.3 Nhận biết các lọ mất nhã dựa vào các dung dịch HCl, NaOH và Na2CO3. Viết PTHH thích hợp để giải thích.
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com



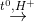 C6H12O6 (Glucozo) + C6H12O6 (Fructozo)
C6H12O6 (Glucozo) + C6H12O6 (Fructozo)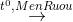 2CO2 + 2C2H5OH
2CO2 + 2C2H5OH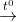 CH3COOH + H2O
CH3COOH + H2O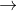 CH3COONa + H2O
CH3COONa + H2O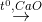 CH4 + Na2CO3
CH4 + Na2CO3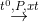 C6H12O6
C6H12O6







