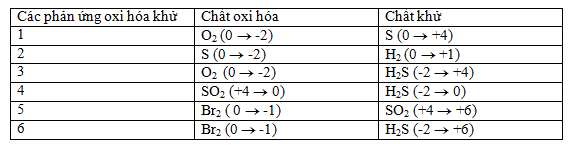Câu 1(VD) : 2 điểm 1. Phân loại thành đơn chất, hợp chất hoặc hỗn hợp cho các chất dưới
Câu 1(VD) : 2 điểm
1. Phân loại thành đơn chất, hợp chất hoặc hỗn hợp cho các chất dưới đây : xenlulozo, hồ tinh bột, kim cương, đất đèn
2. Nguyên tử của nguyên tố A có điện tích hạt nhân là 16+, 3 lớp electron, lớp electron ngoài cùng có 6 electron.
a. Giả thiết “bán kính nguyên tử” là khoảng cách từ hạt nhân tới electron ngoài cùng. Thông số này phụ thuộc vào electron và hạt nhân : Nếu lực hút càng mạnh, bán kính càng nhỏ và ngược lại. Nếu cung cấp năng lượng để 1 electron bứt ra khỏi lớp vỏ ngoài cùng, A chuyển thành A+ ; và ngược lại, cung cấp năng lượng để ép 1 electron vào lớp vỏ ngoài cùng , A chuyển thành A-. Dựa vào điện tích của hạt nhân nguyên tử, hãy sắp xếp theo thứ tự tăng dần bán kính của A, A+, A- và giải thích.
b. Xác định A, viết phương trình hóa học (ghi rõ điều kiện nếu có) để thực hiện các phản ứng chuyển hóa sau :
A + A1 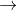 X (1) ; A + B
X (1) ; A + B 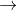 Y (2)
Y (2)
Y + A1 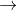 X + E (3) ; X + Y
X + E (3) ; X + Y 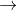 A + E (4)
A + E (4)
X + D + E 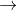 U + V (5) ; Y + D + E
U + V (5) ; Y + D + E 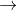 U + V (6)
U + V (6)
Biết mỗi chữ cái là một chất khác nhau.
c. Giả thiết “Số oxi hóa “ là điện tích của nguyên tử trong phân tử nến cho rằng phân tử tạo nên từ các ion đơn nguyên tử. Trong các đơn chất, nguyên tử có số oxi hóa bằng 0. Với đa số các hợp chất, nguyên tử hidro có số oxi hóa +1 ; oxi thường có số oxi hóa -2. Tổng đại số của các số oxi hóa của các nguyên tử trong phân tử bằng 0. Có thể định nghĩa phản ứng oxi hóa – khử là phản ứng có sự thay đổi số oxi hóa, chất oxi hóa là chất có số oxi hóa giảm, chất khử là chất có số oxi hóa tăng trong phản ứng oxi hóa – khử. Dựa vào các định nghĩa trên, hãy cho biết các phản ứng nào trong phần 2b là phản ứng oxi hóa khử? Xác định chất oxi hóa và chất khử trong mỗi phản ứng oxi hóa – khử tùy chọn ở trên
Quảng cáo
1.
ghi nhớ: đơn chất là chất được tạo nên từ 1 nguyên tố hóa học
hợp chất: là chất được tạo nên từ 2 nguyên tố hóa học trở nên
hỗn hợp: gồm nhiều chất trộn lẫn lại với nhau
=> từ đó phân loại được các chất.
2.
a) Lấy bán kính của A làm chuẩn
So sánh bán kính của A và A+
So sánh bán kính của A và A-
Từ đó sắp xếp được thứ tự bán kính của A, A+, A-
b) Dựa vào số điện tích của A là 16+ để tìm ra nguyên tố A. Từ đó vận dụng kiến thức về tính chất hóa học của A để viết các phương trình hóa học
c) Dựa vào lý thuyết về phản ứng oxi hóa rút ra được:
+ phản ứng oxi hóa – khử là phản ứng có sự thay đổi số oxi hóa của các chất trước và sau phản ứng.
+ chất oxi hóa là chất có số oxi hóa giảm sau phản ứng
+ chất khử là chất có số oxi hóa tăng sau phản ứng
=> Từ đó xác định được các phản ứng oxi hóa khử, chất khử; chất oxi hóa.
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com



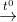 SO2
SO2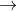 3S + 2H2O
3S + 2H2O