Câu 2(VDC) : 2 điểm 1. Sắt đứng đầu bảng trong các kim loại thương phẩm. Các quặng thông
Câu 2(VDC) : 2 điểm
1. Sắt đứng đầu bảng trong các kim loại thương phẩm. Các quặng thông thường của sắt như manhetit (Fe3O4), limonit (Fe2O3) cũng như sắt vụn đều được dùng để sản xuất sắt. Than cốc được sử dụng như một chất khử rẻ tiền.
a. Hãy viết các phản ứng xảy ra trong lò cao trong quá trình sản xuất sắt
b. Hãy giả sử hiệu suất trong lò cao là 92% theo khối lượng, tính xem với 1,6 tấn quặng chứa 18% manhetit (Fe3O4), 58% limonit (Fe2O3) ta sẽ thu được bao nhiêu kg thép chứa 2% cacbon ?
2. Thuyền trưởng Jack Sparrow trong loạt phim “Cướp biển vùng Caribean” quyết định đóng 3 con tàu vỏ sắt với hình dạng, kích thước và khối lượng hoàn toàn giống nhau. Con tàu thứ nhất tham gia hành trình trên vùng biển lạnh ở Bắc Băng Dương ; con tàu thứ hai tham gia hành trình trên vùng biển nóng ở Đạ Tây Dương ; con tàu thứ ba được thu nhỏ lại, cất trong chai thủy tinh chứa không khí khô rồi đậy nắp chặt bằng nút phòng khi một trong hai con tàu trên bị hỏng sẽ lấy ra sử dụng. Vài tuần sau đó, Jack quan sát sự han rỉ trên các con tàu của mình.
a. Cho biết con tàu nào dễ bị han rỉ, tốc độ han rỉ ở con tàu nào nhanh hơn.
b. Sự han rỉ trên các con tàu phụ thuộc vào những yếu tố nào.
3. Chất rắn Y có thành phần gồm 3 nguyên tố với thành phần % về khối lượng như sau : Fe chiếm 52,09% ; O chiếm 14,88% ; còn lại là nguyên tố X. Biết trong hợp chất này Fe có số oxi hóa +3.
a. Lập luận tìm công thức phân tử của chất rắn Y.
b. Khi đun nóng FeCl3.6H2O phân hủy tạo thành chất rắn Y ; H2O và HCl. Khi tăng nhiệt độ tới 3500C thì chất rắn Y sẽ tiếp tục phân hủy tạo thành FeX3 và Fe2O3 , lúc này FeX3 ở dạng hơi và bay ra. Đun nóng 2,752g FeCl3.6H2O trong không khí đến 3500C thu được 0,898g bã rắn. Xác định số mol của các chất trong bã rắn.
Quảng cáo
1.
a) Lý thuyết luyện gang thép trong lò cao. SGK
Trong 1,6 tấn quặng chứa :
mmanhetit = ?
mlimonit = ?
Áp dụng qui tắc tam suất ta có :
- Cứ 232 g Fe3O4 có 168g Fe => ?
- Cứ 160 g Fe2O3 có 112g Fe => ?
=> mFe (lý thuyết) = ?
=> mFe (Thực tế) = mFe (LT) . H% = ?
=> mthép = mFe(thực) .= ?
2.
a)Tính chất của ăn mòn điện hóa trong các môi trường : nồng độ chất điện lý khác nhau, môi trừng khác nhau. HS lý luận và so sánh.
b) Sự han rỉ phụ thuộc vào : sự tiếp xúc với môi trường điện ly, nồng độ các chất điện ly
3.
a) Tìm công thức hợp chất dựa vào tỉ lẹ các nguyên tố trong hợp chất
%Fe : %O : %X = x : y : z => Công thức tổng quát
Định luật bảo toàn điện tích : (dựa vào số oxi hóa của Fe : +3, O : -2, X : x
+) Xét 2 trường hợp Nếu x > 0 và x < 0 => Biểu thức liên hệ
=> x và t
=> MX
b) Đánh giá xem có chất dư hay không ?
Giả sử các phản ứng đều xảy ra hoàn toàn
Ta có sơ đồ phản ứng sau :
3FeCl3.6H2O 3FeClO
Fe2O3 + FeCl3 ↑
Mol ? ?
=> mrắn so sánh với đề bài
=> như vậy kết luận là phản ứng hoàn toàn hay không
+) Nếu giai đoạn FeCl3.6H2O FeOCl là hoàn toàn
=> Tương tự
=> Các chất trong bã.
>> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com Đầy đủ khoá học các bộ sách: Kết nối tri thức với cuộc sống; Chân trời sáng tạo; Cánh diều. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. PH/HS tham khảo chi tiết khoá học tại: Link
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com



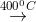 2Fe3O4 + CO2
2Fe3O4 + CO2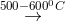 3FeO + CO2
3FeO + CO2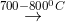 Fe + CO2
Fe + CO2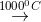 CaO + CO2
CaO + CO2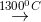 CaSiO3
CaSiO3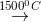 2CO
2CO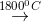 CO2
CO2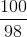 = 805,6 kg
= 805,6 kg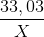 = 1 : 1 :
= 1 : 1 : 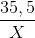 = 1 : 1 : t
= 1 : 1 : t 3FeClO
3FeClO  x
x







