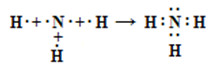a) Biết 20Ca, 9F, 7N, 1H và độ âm điện của Ca = 1,0; F = 3,98; N = 3,04; H = 2,2. Hãy biểu diễn sự
a) Biết 20Ca, 9F, 7N, 1H và độ âm điện của Ca = 1,0; F = 3,98; N = 3,04; H = 2,2. Hãy biểu diễn sự hình thành liên kết trong các phân tử CaF2, NH3.
b) Xác định chất oxi hóa, chất khử, quá trình oxi hóa, quá trình khử và cân bằng các phản ứng sau:
(1) H2S + Cl2 + H2O → H2SO4 + HCl
(2) KMnO4 + HCl → KCl + MnCl2 + Cl2 + H2O
Quảng cáo
a) Xác định loại liên kết trong phân tử CaF2 và NH3 dựa vào hiệu độ âm điện của 2 nguyên tử. Từ đó biểu diễn sự hình thành liên kết trong các phân tử trên.
b)
- Xác định số oxi hóa của các nguyên tố để tìm chất oxi hoá và chất khử.:
+ Chất khử là chất cho e.
+ Chất oxi hóa là chất nhận e.
- Viết quá trình oxi hóa và quá trình khử:
+ Quá trình khử là quá trình nhận e.
+ Quá trình oxi hóa là quá trình nhường e.
- Cân bằng phản ứng oxi hóa - khử bằng phương pháp thăng bằng electron.
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com