(3 điểm): a. Cho 16,05 gam Fe(OH)3 tác dụng vừa đủ với V ml dung dịch HNO3 1M, thu được dung
(3 điểm):
a. Cho 16,05 gam Fe(OH)3 tác dụng vừa đủ với V ml dung dịch HNO3 1M, thu được dung dịch chứa a gam muối. Viết phương trình phản ứng xảy ra, tìm các giá trị V và a.
b. Hòa tan hoàn toàn 10,08 gam kim loại Mg vào dung dịch HNO3 loãng, dư, thấy thoát ra 4,48 lít khí NO (ở đktc và là khí thoát ra duy nhất), tính khối lượng muối tan có trong dung dịch sau phản ứng.
Quảng cáo
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com



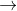 Fe(NO3)3 + 3H2O
Fe(NO3)3 + 3H2O
















