Quá trình điện phân để mạ đồng (Cu) lên một chiếc chìa khoá
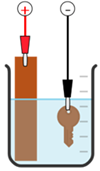
Quá trình điện phân để mạ đồng (Cu) lên một chiếc chìa khoá được làm từ thép không gỉ, được mô tả ở hình vẽ (cathode là chìa khóa, anode là đồng thô, dung dịch điện phân là CuSO4). Biết cường độ dòng điện không đổi là 10A, thời gian điện phân là 16 phút 5 giây, Cu có khối lượng riêng là 8,9 gam/cm³, nguyên tử khối của Cu là 64; F = 96500 C/mol; hiệu suất điện phân 100%. Sơ đồ điện phân mạ đồng lên chìa khoá:
| Đúng | Sai | |
|---|---|---|
| a) Anode xảy ra quá trình khử ion Cu2+. | ||
| b) Trong quá trình điện phân, điện cực anode tan dần. | ||
| c) Trong quá trình điện phân, số mol muối CuSO4 không thay đổi. | ||
| d) Nếu chiếc chìa khóa có tổng diện tích cần mạ là 20 cm² thì bề dày lớp đồng bám đều trên chiếc chìa khóa là 0,006 cm (làm tròn đến hàng phần nghìn). |
Đáp án đúng là: S; Đ; Đ; S
Quảng cáo
Trong điện phân: anode (cực dương) xảy ra quá trình oxi hóa (nhường electron); cathode (cực âm) xảy ra quá trình khử (nhận electron).
Công thức Faraday: mCu = \(\dfrac{{{\rm{64}}.{\rm{I}}{\rm{.t}}}}{{2{\rm{F}}}}\)
⟶ Độ dày lớp mạ = \(\dfrac{{{{\rm{m}}_{{\rm{Cu}}}}}}{{{{\rm{V}}_{{\rm{chia khoa}}}}.{\rm{D}}}}\)
Đáp án cần chọn là: S; Đ; Đ; S
>> 2K8 Chú ý! Lộ Trình Sun 2026 - 3IN1 - 1 lộ trình ôn 3 kì thi (Luyện thi 26+ TN THPT, 90+ ĐGNL HN, 900+ ĐGNL HCM, 70+ ĐGTD - Click xem ngay) tại Tuyensinh247.com.Đầy đủ theo 3 đầu sách, Thầy Cô giáo giỏi, luyện thi theo 3 giai đoạn: Nền tảng lớp 12, Luyện thi chuyên sâu, Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











