Hydrogen là nhiên liệu xanh và thân thiện với môi trường nhất, được
Hydrogen là nhiên liệu xanh và thân thiện với môi trường nhất, được đánh giá có tiềm năng cung cấp phần lớn năng lượng cho thế giới trong tương lai, thay thế cơ sở hạ tầng năng lượng hiện tại dựa trên nhiên liệu hóa thạch. Hydrogen được kỳ vọng sẽ giải quyết vấn đề thiếu hụt năng lượng trong tương lai gần, đặc biệt là ở các khu vực địa lý phức tạp (đồi núi, cao nguyên khô cằn, v.v.) và khí hậu khắc nghiệt. Hiện nay, việc sản xuất hydrogen công nghiệp chủ yếu thông qua quá trình oxi hóa – khử như reforming CH₄ hoặc điện phân nước. Vì vậy, cần đánh giá lợi ích – rủi ro khi sử dụng H₂.
Biết khối lượng riêng xăng (xấp xỉ C₈H₁₈) là 0,703 g·cm⁻³
a) Viết phương trình phản ứng xảy ra đốt cháy hoàn toàn nhiên liệu hydrogen và xăng (thành phần chính (thành phần chính là C8H18).
b) Gọi k là phần trăm năng lượng tỏa ra khi đốt cháy hoàn toàn 1 L khí H₂ (dkc) so với 1 lít xăng. Giá trị của k bằng bao nhiêu? Làm tròn kết quả đến hai chữ số sau dấu phẩy.
c) Tại sao hydrogen được dùng làm nhiên liệu phải được nén ở áp suất cao hoặc hoá lỏng?
Quảng cáo
a) Viết phương trình phản ứng chảy của H2 và C8H18.
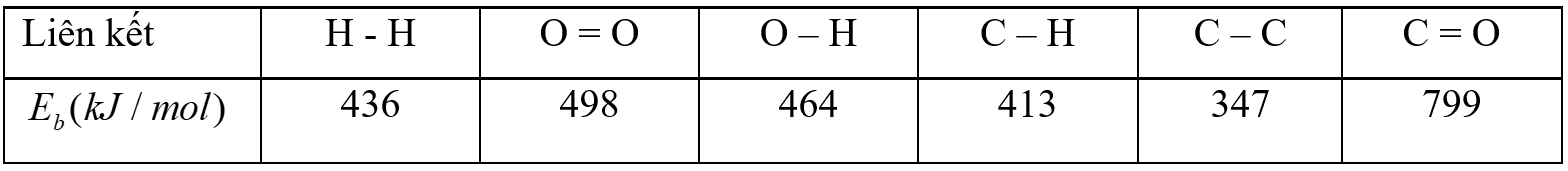
b) Biến thiên enthalpy của phản ứng theo năng lượng liên kết.
$\Delta_{r}H_{298}^{o} = {\sum{E_{b}(cd)}} - {\sum{E_{b}(sp)}}$
Khối lượng riêng: $d = \dfrac{m}{V}$
c) Hoá học và vấn đề môi trường.
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











