Khi một phân tử nhỏ tương tác và gắn vào protein, hệ sẽ xảy ra sự thay đổi về năng
Khi một phân tử nhỏ tương tác và gắn vào protein, hệ sẽ xảy ra sự thay đổi về năng lượng. Để đánh giá xem quá trình gắn kết có tự xảy ra hay không và bền đến mức nào, người ta dùng đại lượng năng lượng tự do Gibbs (ΔG°) theo công thức: $\text{Δ}_{\text{r}}\text{G}_{}^{\text{o}} = \text{Δ}_{\text{r}}\text{H}_{}^{\text{o}} - \text{T}.\text{Δ}_{\text{r}}\text{S}_{}^{\text{o}}$. Trong đó: ΔH° là biến thiên enthalpy của phản ứng, ΔS° là biến thiên entropy và T là nhiệt độ.
Tuy nhiên, khi các nhà khoa học thay đổi cấu trúc của phân tử nhỏ để giúp nó gắn tốt hơn vào protein, giá trị ΔG° lại thường không giảm nhiều như mong đợi. Nguyên nhân của hiện tượng này nằm ở quy luật bù trừ enthalpy – entropy (EEC).
Quy luật EEC cho biết: khi phân tử nhỏ được chỉnh sửa để tạo ra nhiều tương tác tỏa nhiệt hơn với protein, ΔH° sẽ âm hơn, tức là có lợi cho sự gắn kết. Nhưng cùng lúc đó, hệ lại trở nên trật tự hơn vì các phân tử bị “giữ chặt”, làm ΔS° giảm xuống. Khi tính theo biểu thức TΔS°, thành phần này cũng âm hơn và trở thành yếu tố bất lợi cho quá trình gắn kết. Hai đại lượng ΔH° và TΔS° biến thiên ngược chiều và bù trừ lẫn nhau, khiến kết quả tổng hợp là ΔG° chỉ thay đổi rất ít.
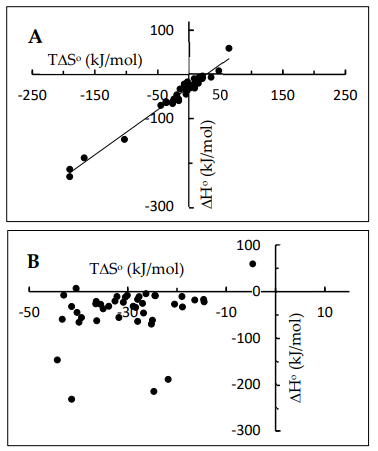
Hình 1. Đồ thị tuyến tính giữa enthalpy (ΔH°) và entropy (TΔS°) trong dữ liệu tương tác protein–phân tử nhỏ.
Điều này được quan sát trên một lượng dữ liệu lớn từ các thí nghiệm đo nhiệt động lực học của tương tác protein – phân tử nhỏ. Dù ΔH° và entropy thay đổi đáng kể khi tối ưu cấu trúc, năng lượng Gibbs cuối cùng vẫn chỉ dao động trong một dải hẹp. Điều đó cho thấy trong các hệ sinh học, tự nhiên luôn duy trì một sự cân bằng để protein gắn đủ bền nhưng vẫn linh hoạt nhằm đảm bảo chức năng hoạt động của nó.
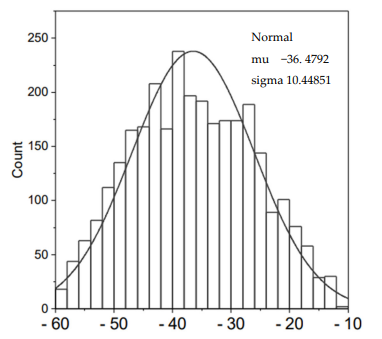
Hình 2: Biểu đồ phân bố Gaussian của ΔG° từ hơn 3000 tương tác protein – phân tử nhỏ.
Đa số giá trị nằm trong một vùng hẹp, cho thấy ΔG° không phân tán rộng mà tập trung quanh một dải năng lượng nhất định.
Trả lời cho các câu 1, 2, 3, 4, 5, 6, 7 dưới đây:
Đồ thị Hình 1 dốc lên nên ΔH âm hơn thì ΔG âm hơn theo đúng tỉ lệ 1:1.
Đáp án đúng là: B
Dựa vào thông tin bài đọc.
Đáp án cần chọn là: B
Trong hiện tượng bù trừ enthalpy–entropy (EEC):
| Đúng | Sai | |
|---|---|---|
| a) Khi ΔH âm hơn thì entropy của hệ chắc chắn tăng. | ||
| b) Khi ΔH âm hơn thì TΔS thường cũng âm hơn theo xu hướng tuyến tính. | ||
| c) ΔH và entropy luôn triệt tiêu nhau bằng phép cộng đại số. | ||
| d) ΔG không phụ thuộc ΔH và entropy trong các hệ phức tạp. |
Đáp án đúng là: S; Đ; S; S
Dựa vào thông tin có trong bài đọc.
Đáp án cần chọn là: S; Đ; S; S
Trên đồ thị (ΔH°; TΔS°) của EEC, độ dốc dương cho thấy hai đại lượng này có xu hướng biến thiên _______ dấu với nhau, phản ánh tính bù trừ năng lượng trong hệ.
Đáp án đúng là: cùng
Quan sát đồ thị ở hình 1.
Đáp án cần điền là: cùng
Một phản ứng có ΔH° = −120 kJ/mol. Ở 298 K, đồ thị EEC cho thấy quá trình có mức bù trừ TΔS° ≈ 0,82·ΔH°. Giá trị ΔG° của phản ứng ở 298 K gần nhất với:
Đáp án đúng là: A
Áp dụng công thức: $\text{Δ}_{\text{r}}\text{G}_{}^{\text{o}} = \text{Δ}_{\text{r}}\text{H}_{}^{\text{o}} - \text{T}.\text{Δ}_{\text{r}}\text{S}_{}^{\text{o}}$
Đáp án cần chọn là: A
Cho phản ứng có ΔH° < 0 và ΔS° < 0. Sắp xếp các nhiệt độ sau theo mức độ tự xảy ra giảm dần của phản ứng:
Đáp án đúng là:
Dựa vào công thức: $\text{Δ}_{\text{r}}\text{G}_{}^{\text{o}} = \text{Δ}_{\text{r}}\text{H}_{}^{\text{o}} - \text{T}.\text{Δ}_{\text{r}}\text{S}_{}^{\text{o}}$
Đáp án cần chọn là:
Theo hình 2, giá trị ΔG° có tần suất cao nhất trên biểu đồ nằm gần khoảng:
Đáp án đúng là: C
Quan sát hình 2, đưa ra nhận xét.
Đáp án cần chọn là: C
Một quá trình có ΔH° = −180 kJ/mol và ΔS° = −0,40 kJ/mol.K. Nhiệt độ tối đa để quá trình tự xảy ra (ΔG° < 0) là gần nhất với:
Đáp án đúng là: D
Dựa vào công thức: $\text{Δ}_{\text{r}}\text{G}_{}^{\text{o}} = \text{Δ}_{\text{r}}\text{H}_{}^{\text{o}} - \text{T}.\text{Δ}_{\text{r}}\text{S}_{}^{\text{o}}$
Đáp án cần chọn là: D
Quảng cáo
>> Học trực tuyến Lớp 10 cùng thầy cô giáo giỏi tại Tuyensinh247.com, (Xem ngay) Cam kết giúp học sinh học tốt, bứt phá điểm 9,10 chỉ sau 3 tháng, làm quen kiến thức, định hướng luyện thi TN THPT, ĐGNL, ĐGTD ngay từ lớp 10
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











