Trong sản xuất sulfuric acid (H2SO4) công nghiệp, một số nhà máy sử dụng quặng pyrite (FeS2) làm
Trong sản xuất sulfuric acid (H2SO4) công nghiệp, một số nhà máy sử dụng quặng pyrite (FeS2) làm nguyên liệu chính. Tuy nhiên một số hợp chất hoặc đơn chất lưu huỳnh cũng có thể được sử dụng ở giai đoạn 1. Quy trình tiếp xúc được diễn ra theo các giai đoạn sau:
- Giai đoạn 1: Rang quặng pyrite – quá trình oxi hóa với không khí để thu được sulfur dioxide.
4FeS2 + 11O2 ⟶ 2Fe2O3 + 8SO2
- Giai đoạn 2: Chuyển hóa sulfur dioxide thành sulfur trioxide với xúc tác V2O5 ở điều kiện 450oC; 1 – 2 atm.
2SO2 + O2 ⟶ 2SO3 $\Delta_{r}H_{298}^{o} = - 197,8kJ$
- Giai đoạn 3: Hấp thụ SO3 bằng dung dịch H2SO4 đặc tạo oleum.
nSO3 + H2SO4 ⟶ H2SO4.nSO3
- Giai đoạn 4: Pha loãng oleum.
H2SO4.nSO3+nH2O ⟶ (n + 1)H2SO4
Tại giai đoạn 3, người ta không hấp thụ SO3 trực tiếp vào nước do tạo sương acid khó thu hồi và gây ăn mòn.
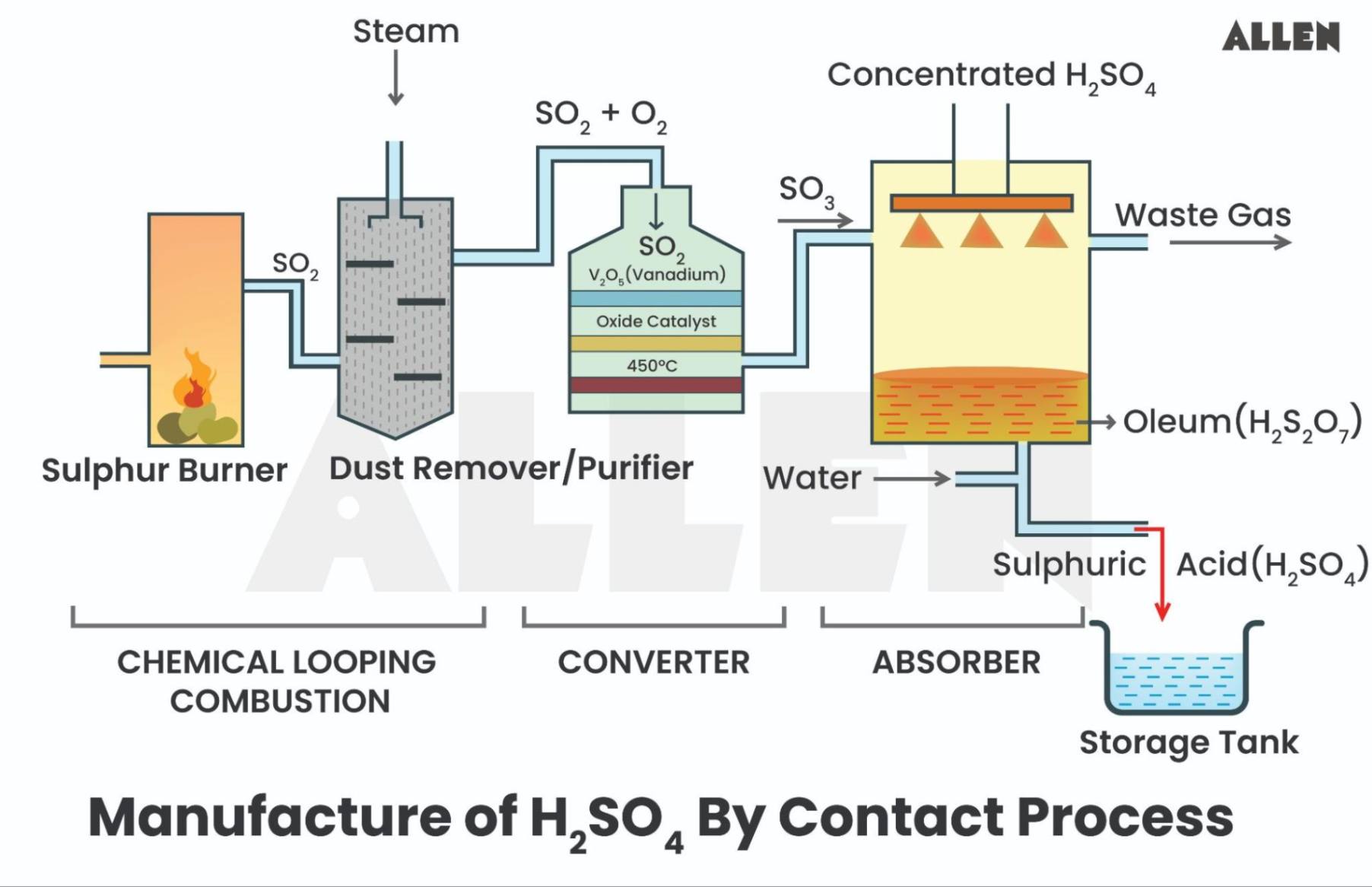
Trả lời cho các câu 1, 2 dưới đây:
Một nhà máy xử lí 5,0 tấn quặng pyrite (FeS2 chiếm 78,6% về khối lượng) mỗi ngày. Hiệu suất chung của toàn bộ quá trình là 90% và giá trị của n trong công thức oleum bằng 1. Khối lượng (tấn) dung dịch sulfuric acid 98% thu được trong mỗi ngày có giá trị gần nhất với
Đáp án đúng là: D
Sơ đồ tổng hợp: $Fe{{S}_{2}}\xrightarrow{+{{O}_{2}}}2S{{O}_{2}}\xrightarrow{+{{O}_{2}}}2S{{O}_{3}}\xrightarrow{+{{H}_{2}}S{{O}_{4}}}2{{H}_{2}}S{{O}_{4}}.S{{O}_{3}}\to 4{{H}_{2}}S{{O}_{4}}$
Tính theo sơ đồ phản ứng.
Đáp án cần chọn là: D
Cho các phát biểu sau:
(a) Xúc tác V2O5 giúp tăng tốc độ chuyển hóa SO2 thành SO3.
(b) Do phản ứng chuyển hóa SO2 thành SO3 là tỏa nhiệt, do đó cần sử dụng nhiệt độ cao để tăng hiệu suất phản ứng.
(c) Có thể sử dụng nước thay thế cho dung dịch H2SO4 đặc ở giai đoạn 3 để thu được sản phẩm với hiệu quả tương đương.
(d) Trong quá trình sản xuất, SO2 có thể được điều chế từ nhiều nguồn khác nhau như đốt lưu huỳnh nguyên chất.
(e) Để giảm ô nhiễm môi trường, khí SO2 thải ra phải được xử lí trước khi xả vào khí quyển.
Số phát biểu đúng là
Đáp án đúng là: C
Quá trình sản xuất H2SO4.
Các yếu tố ảnh hưởng tới cân bằng phản ứng: nồng độ, nhiệt độ, áp suất.
Đáp án cần chọn là: C
Quảng cáo
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











