Trong công nghiệp, aluminium (nhôm) được sản xuất từ quặng bauxite (có thành phần chính là
Trong công nghiệp, aluminium (nhôm) được sản xuất từ quặng bauxite (có thành phần chính là Al2O3.2H2O) theo hai giai đoạn chính:
Giai đoạn 1: Tinh chế quặng bauxite.
Giai đoạn 2: Điện phân Al2O3 nóng chảy.
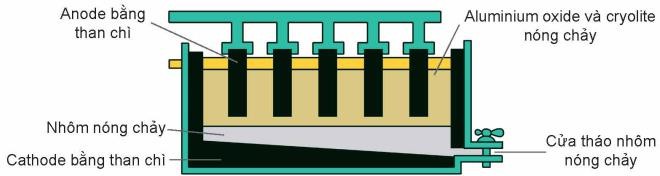
Trong quá trình sản xuất nhôm bằng phương pháp điện phân nóng chảy aluminium oxide, điện cực dương bằng
than chì bị ăn mòn liên tục do phản ứng giữa carbon và oxygen tạo thành hỗn hợp khí O2, CO, CO2. Giả sử các khí trong hỗn hợp trên có tỉ lệ mol bằng nhau, các phản ứng xảy ra hoàn toàn. Để sản xuất được 2,7 kg nhôm thì khối lượng than chì bị tiêu hao do phản ứng oxi hoá là m gam. Giá trị của m là bao nhiêu? (Kết quả các phép tính trung gian không được làm tròn, chỉ kết quả cuối cùng được làm tròn đến số nguyên).
Đáp án đúng là:
Quảng cáo
$2A{{l}_{2}}{{O}_{3}}\xrightarrow[cryolite]{pnc}4Al+3{{O}_{2}}.$
$\left. \Rightarrow n_{O_{2}} = \dfrac{3}{4}n_{Al}. \right.$
Các khí trong hỗn hợp có tỉ lệ mol bằng nhau, đặt$\left\{ \begin{matrix} {n_{CO_{2}} = k(mol)} \\ {n_{CO} = k(mol)} \\ {n_{O_{2du}} = k(mol)} \end{matrix} \right.$
$C+{{O}_{2}}\xrightarrow[{}]{{{t}^{o}}}C{{O}_{2}}.$
k k k (mol)
$2C+{{O}_{2}}\xrightarrow[{}]{{{t}^{o}}}2CO.$
k 0,5k k (mol)
O2 dư
k (mol)
Ta có $\left. \left\{ \begin{matrix} \left. n_{O_{2}} = k + 0,5k + k = 1,5k\ \Rightarrow\text{k(mol)} \right. \\ {n_{C} = 2k(mol)} \end{matrix} \right.\Rightarrow m_{C} = 12.2k(g). \right.$
Đáp án cần điền là: 720
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











