CẶP OXI HÓA – KHỬ CỦA KIM LOẠI Trong một phản ứng oxi hóa
CẶP OXI HÓA – KHỬ CỦA KIM LOẠI
Trong một phản ứng oxi hóa – khử, luôn có sự tham gia của chất oxi hóa (chất nhận electron) và chất khử (chất nhường electron). Dạng oxi hóa – khử của một nguyên tử hay một nhóm nguyên tử được viết dưới dạng: oxh/kh. Thế điện cực của cặp oxi hóa – khử của kim loại trong điều kiện chuẩn (nồng độ ion kim loại trong dung dịch ở 1M, ở nhiệt độ 25oC) được gọi là thế điện cực chuẩn của kim loại. Thế điện cực chuẩn được kí hiệu được kí hiệu là \(E_{oxh/kh}^o\), đơn vị thường dùng là volt (V).
Các kim loại đều có tính chất hóa học đặc trưng là tính khử. Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính oxi hóa của dạng oxi hóa càng mạnh, tính khử của dạng khử càng yếu và ngược lại. Nguyên tắc chung của phản ứng oxi hóa khử là:

Khi tham gia phản ứng hóa học, so sánh giá trị thế điện cực chuẩn của cặp oxi hóa – khử của các chất tham gia mà người ta có thể dự đoán xu hướng phản ứng và chất sản phẩm của phản ứng hóa học đó.
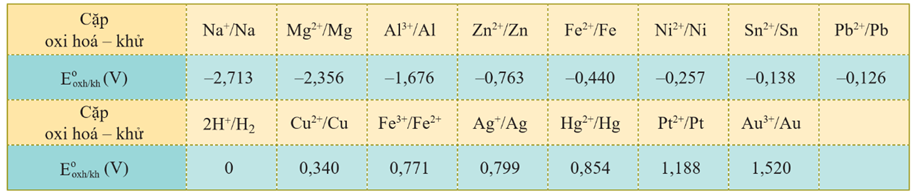
Bảng 1. Bảng giá trị thế điện cực chuẩn của một số cặp oxi hóa – khử của kim loại
Trả lời cho các câu 1, 2, 3, 4, 5, 6, 7 dưới đây:
Cho các cặp oxi hóa – khử:
Cl2/2Cl-, Fe2+/Fe, Cu+/Cu, Fe3+/Fe2+
- Dạng oxi hóa của cặp oxi hóa - khử Cl2/2Cl- là
- Dạng khử của cặp oxi hóa – khử Cu+/Cu là
- vừa là dạng oxi hóa, vừa là dạng khử của cùng một nguyên tố kim loại.
Đáp án đúng là: Cl2; Cu
Dạng oxi hóa – khử của một nguyên tử hay một nhóm nguyên tử được viết dưới dạng: oxh/kh.
Đáp án cần chọn là: Cl2; Cu
Điền từ không quá hai tiếng thích hợp vào chỗ trống?
“Quy tắc alpha” dự đoán chiều phản ứng chiều phản ứng oxi hóa – khử theo thế điện cực chuẩn:
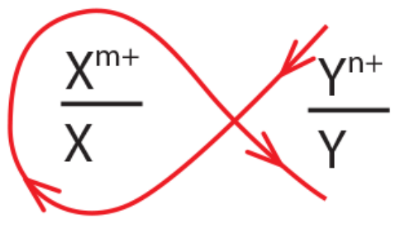
Dựa vào hình trên, ta suy ra được: Giá trị thế điện cực chuẩn của cặp $Y^{n +}/Y$ ___________ giá trị thế điện cực chuẩn của cặp $X^{m +}/X$.
Đáp án đúng là: lớn hơn
Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính oxi hóa của dạng oxi hóa càng mạnh, tính khử của dạng khử càng yếu và ngược lại.
Nguyên tắc chung của phản ứng oxi hóa khử là:

Đáp án cần điền là: lớn hơn
Cho phương trình hóa học của phản ứng chuẩn độ xác định hàm lượng sắt (II) trong một mẫu chất như sau: $\left. \mathbf{10FeS}\mathbf{O}_{\mathbf{4}} + \mathbf{2KMn}\mathbf{O}_{\mathbf{4}}~ + \mathbf{8}\mathbf{H}_{\mathbf{2}}\mathbf{S}\mathbf{O}_{\mathbf{4}}~\rightarrow\mathbf{5F}\mathbf{e}_{\mathbf{2}}\left( {\mathbf{S}\mathbf{O}_{\mathbf{4}}} \right)_{\mathbf{3}}~ + \ \mathbf{K}_{\mathbf{2}}\mathbf{S}\mathbf{O}_{\mathbf{4}}~ + \ \mathbf{2MnS}\mathbf{O}_{\mathbf{4}}~ + \ \mathbf{8}\mathbf{H}_{\mathbf{2}}\mathbf{O} \right.$
Các nhận định dưới đây là đúng hay sai?
| Đúng | Sai | |
|---|---|---|
| a) Chất oxi hóa là $FeSO_{4}$, chất khử là $H_{2}SO_{4}$. | ||
| b) Môi trường thực hiện phản ứng trên có pH < 7. | ||
| c) Từ phản ứng trên ta có: $E_{Fe^{3 +}/Fe^{2 +}}^{o} > E_{MnO_{4}^{-}/Mn^{2 +}}^{o}$. | ||
| d) Phản ứng trên làm mất màu $KMnO_{4}$ nên không cần sử dụng chỉ thị để nhận biết điểm dừng chuẩn độ. |
Đáp án đúng là: S; Đ; S; Đ
Lí thuyết về phản ứng oxi hoá – khử, thế điện cực chuẩn của cặp oxi hoá – khử.
Đáp án cần chọn là: S; Đ; S; Đ
Phản ứng nào sau đây có thể xảy ra ở điều kiện chuẩn?
Lưu ý: s là chất rắn, aq là dung dịch.
Đáp án đúng là: A
Nguyên tắc chung của phản ứng oxi hóa khử là:

Đáp án cần chọn là: A
Thế điện cực chuẩn của cặp $M^{n +}/M$ ($M$ là kim loại) bằng −3,040V. Những phát biểu liên quan đến cặp oxi hóa – khử $M^{n +}/M$ nào sau đây là đúng?
Đáp án đúng là: A; B
Thế điện cực chuẩn của cặp oxi hóa – khử càng lớn thì tính oxi hóa của dạng oxi hóa càng mạnh, tính khử của dạng khử càng yếu và ngược lại.
Đáp án cần chọn là: A; B
Cho phản ứng xảy ra như sau: $\left. Cr_{2}O_{7}^{2 -} + 14H^{+} + 6Fe^{2 +}\rightarrow 2Cr^{3 +} + 6Fe^{3 +} + 7H_{2}O \right.$
Giá trị nào dưới đây có thể là giá trị thế điện cực chuẩn của cặp $Cr_{2}O_{7}^{2 -}/Cr^{3 +}$?
Đáp án đúng là: A
Căn cứ vào giá trị thế điện cực.
Đáp án cần chọn là: A
Sắp xếp sức điện động của các cặp pin theo thứ tự tăng dần.
Đáp án đúng là: 4-2-3-1
Áp dụng công thức tính sức điện động: E0pin = E0cathode – E0anode
Đáp án cần chọn là: 4-2-3-1
Quảng cáo
>> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
 |
 |
 |
 |
 |
 |
 |
 |
Hỗ trợ - Hướng dẫn

-
024.7300.7989
-
1800.6947

(Thời gian hỗ trợ từ 7h đến 22h)
Email: lienhe@tuyensinh247.com











